Вступ
Відомо, що хронічні патологічні процеси у шлунку супроводжуються порушеннями регуляторних механізмів клітинної проліферації та диференціювання, що призводить або до субституції, результатом якої є атрофія головних залоз при атрофічному гастриті, або до патологічної регенерації, відображенням якої є кишкова метаплазія (КМ), а це вже розцінюється як передраковий стан шлунка [1]. Остаточно патогенез КМ залишається нез’ясованим, між тим виникненню та прогресуванню процесу сприяють численні предиктори, впливи яких можуть реалізувати збій нейроендокринної регуляції (APUD-системи), а далі — дисрегуляцію між основними системами організму. Особливостями різноманітних дисрегуляцій при патологічних станах, зокрема при преканцерозах, є зниження адаптації, а також дисфункція найважливіших метаболічних процесів, що проявляється у зниженні їх варіабельності та у стандартизації базисних механізмів обміну, а спрощення системи регуляції — це шлях до дисрегуляції [2, 3].
У сучасному суспільстві дуже актуальним є вплив стресогенних факторів на психіку та здоров’я людини. Дуже широке коло психосоматичних розладів, а також інших наслідків переживання хронічного стресу (депресія, тривожність тощо). З погляду фізіологічних механізмів, переживання як психічного, так і фізіологічного стресу людиною запускає каскад нервових та гормональних реакцій. При стресі активується симпатичний відділ вегетативної нервової системи (ВНС) і посилюється викид гормонів надниркових залоз, що змінює роботу більшості внутрішніх органів із підґрунтям до запуску канцерогенних реакцій [3, 4]. При будь-якій зміні функціонального стану людини — психічного, емоційного або при фізичній напрузі миттєво змінюється тонус ВНС у бік підвищення активності її симпатичного відділу. У спокійному ж стані активніший, як правило, парасимпатичний відділ. У тих галузях знань про людину, де важливим є своєчасне та об’єктивне визначення рівня напруги (психологія, психофізіологія, спортивна наука, медицина), вивчення вегетативного балансу найчастіше здійснюється за допомогою показників варіабельності серцевого ритму (ВСР). Ці показники дозволяють провести диференційовану діагностику вегетативних впливів як на серце, так і на весь організм загалом [5]. ВСР є одним із найперспективніших маркерів функції ВНС [6]. За допомогою компонентів часового домену аналізу ВСР визначають резерви адаптації та серцево-судинні ризики, а за допомогою частотного домену визначають симпатовагальний баланс ВНС [7].
Як відомо, активність усіх систем організму безперервно варіює. Вважається, що менша варіабельність життєво важливих констант спрямована на підтримання лише адекватної для них функції, тоді як більша варіабельність показника призначена для забезпечення кращого пристосування і може розглядатися як фізіологічний резерв регуляторів [8, 9]. Показники ВСР є надійними та об’єктивними індикаторами тонусу ВНС (її симпатичного та парасимпатичного відділів), який, у свою чергу, відображає зміни у психоемоційному стані людини на фоні розвитку стресу або будь-якої напруги. Вегетативна дезадаптація проявляється значним зниженням ВСР, підвищенням активності симпатичної нервової системи, ознаками перенапруги регуляторних систем. Існують реципрокні взаємодії між депресивними розладами та ризиком розвитку тяжкого перебігу гастроентерологічних захворювань з подальшим ризиком ускладнень. Одним з можливих механізмів, що забезпечують цей взаємозв’язок, може бути рівень парасимпатичних (вагальних) впливів. ВСР знижується при депресії та тривозі у пацієнтів з гастроентерологічними захворюваннями. Мабуть, тонус парасимпатичного відділу ВНС одночасно впливає на емоції, настрій та роботу внутрішніх органів [10].
Існує теорія, за якою ВСР може бути маркером здатності впізнавати соціальні знаки, що подаються іншими людьми. Підвищена ВСР пов’язана з кращою здатністю розпізнавати емоції. Програми з управління стресом включають різні релаксаційні техніки і когнітивну поведінкову терапію. Біологічний зворотний зв’язок може полегшити досягнення релаксації, допомагаючи хворому краще усвідомлювати і контролювати свої фізіологічні процеси. У корекції спричинених стресом порушень, у тому числі й порушень травної системи, а також тривожно-депресивних розладів, застосовується методика нейростимуляції, яка є науково доведеним тригером, що використовується для активації окремих ланок ВНС. Технологія Pure Purr поєднує кілька звукових та візуальних стимулів, спрямованих на активацію парасимпатичної нервової системи. Ця технологія заснована на відкриттях у нейрофізіології, медицині, акустиці та комп’ютерній техніці, які використовуються для ініціювання фізіологічного процесу відпочинку, тобто алостазу. Буквально цей термін означає досягнення стабільності через зміни. Це активний механізм, що відіграє роль у нормалізації тонусу ВНС та підтриманні стабільності внутрішнього середовища тіла. Стан, у якому всі наші функції реалізуються повністю та економно залежно від навантаження, а рівень адаптації залишається високим тривалий час. У шоломі, який на 5 хв надягається на голову хворого, використана технологія повного занурення у віртуальну реальність, тобто повністю відсікаються зовнішні подразники. Робота шолома побудована на сенсорній взаємодії людини — візуальній та слуховій. Візуальна взаємодія є елементом емпатичної медітації, ритмічні аудіовізуальні імпульси налаштовуються на частоту фізіологічного дихання та серцебиття та синхронізуються з частотою дельта мозкових хвиль. Рандомізованими дослідженнями був доведений позитивний ефект цього комплексу на когнітивну функцію мозку та систему нейрогуморальної регуляції через синхронне спрацьовування низки стимулів, таких як: візуальна послідовність, посилений ефект віртуальної реальності, гармонійна музика з технологією бінаурального ритму і модифіковане котяче муркотіння [11, 12].
Мета дослідження: оптимізувати лікування хворих на хронічний атрофічний гастрит із вегетативними розладами за допомогою програмно-апаратного комплексу для парасимпатичної активації ВНС.
Матеріали та методи
Обстежено 80 хворих на хронічний атрофічний гастрит. Залежно від поширення, локалізації та гістологічних змін у шлунку хворі були розподілені на групи: I групу становили 10 хворих з атрофічними змінами слизової оболонки шлунка (СОШ) різного ступеня вираженості; до II групи увійшло 20 хворих із кишковою метаплазією в антральному відділі шлунка, III група характеризувалась наявністю у 39 хворих тотальної кишкової метаплазії, яка охоплювала антральний відділ та тіло шлунка; IV група — 11 хворих із дисплазією. Контрольну групу становили 15 осіб.
Оцінку ВСР проводили за результатами PRECISE-діагностики за допомогою електрокардіографа CONTECT 8000GW (Китай) з блютуз-з’єднанням і програмним забезпеченням. Для інтерпретації результатів ЕКГ виконано підключення до веб-сервісу AMAZON [12]. Аналізували наступні показники: симпатовагальний баланс HF/LF для визначення вегетативного тонусу; RMSSD — оцінює рівень адаптації (кількісна оцінка виснаження резервів адаптації); загальну потужність спектра (Total power, TP), що свідчить про можливості функціональних резервів організму; стрес-індекс (Stress index, SI) визначає стресостійкість організму; SDNN — стандартне відхилення всіх NN-інтервалів, що визначає наявність і вираженість серцево-судинного ризику (СС-ризик).
При спектральному аналізі стаціонарних записів визначали наступні параметри ВСР: VLF-потужність у діапазоні дуже низькочастотних коливань (0,003–0,04 Гц), для характеристики активності гуморально-метаболічних та центральних ерготропних механізмів регуляції серцевого ритму; LF-потужність у діапазоні низькочастотних коливань (0,04–0,15 Гц), для оцінки активності симпатичної ланки вегетативної регуляції; HF-потужність у діапазоні високочастотних коливань (0,15–0,40 Гц), що відображує активність парасимпатичної ланки вегетативної регуляції; ТР — загальну потужність спектра (діапазон 0,003–0,4 Гц) як суми вищезазначених показників, що відтворює сумарний ефект впливу на серцевий ритм усіх рівнів регуляції; симпатико-парасимпатикотонічний баланс — LF/HF. Таким чином, комплексна оцінка ВСР передбачає діагностику функціональних станів ВНС. Зміни вегетативного балансу у вигляді активації симпатикотонічної ланки ВНС розглядаються як неспецифічний компонент адаптаційної реакції у відповідь на різні стресорні впливи. Тому серед обстежених хворих за результатами PRECISE-діагностики були виділені пацієнти із превалюванням симпатикотонічного відділу ВНС, яким призначався для лікування Pure Purr — програмно-апаратний комплекс для парасимпатичної активації на основі гарнітури віртуальної реальності з дисплеєм з достатньою роздільною здатністю, вбудованим процесором, пам’ятю та стереодинаміками розширеного діапазону. Програмно-апаратний комплекс Pure Purr призначався курсом на 10 сеансів для відновлення автономної регуляції у складі комплексної терапії порушень адаптації та стресових розладів. Після курсу нейростимуляції у хворих вивчали динаміку показників ВСР за допомогою PRECISE-діагностики.
Результати та обговорення
За аналізом статистичних показників у групі з кишковою метаплазією в антральному відділі шлунка (II група) відзначено зниження окремих статистичних показників (RMSSD: (16,5 ± 1,8) мс2 проти (78,3 ± 2,5) мс2 у хворих I групи, р < 0,05; pNN50: (11,5 ± 1,7) мс2 проти (16,8 ± 1,9) мс2 у хворих I групи, р < 0,05), що обумовлено активацією симпатикотонічної ланки ВНС та зривом адаптації. У той же час відзначалось зниження частотних характеристик за рахунок усіх компонентів спектра, що також відображує підвищення симпатикотонічного впливу на ритм серця у цій групі. Індекс симпатовагальної взаємодії становив (1,5 ± 0,2) ум.од., що свідчило про нормотонію, таким чином, кишкова метаплазія виникає не тільки через домінуючий вплив симпатикотонічного відділу ВНС (табл. 1).
/21.jpg)
У хворих з тотальною КМ (III група) відзначалось вірогідне зниження рівнів RMSSD ((12,7 ± 1,4) мс2 проти (78,3 ± 2,5) мс2 у хворих I групи; p < 0,05), pNN50 ((6,1 ± 4,1) мс2 проти (16,8 ± 1,9) мс2 відповідно, p < 0,05), що свідчить про активацію симпатикотонічного відділу ВНС та зрив адаптації. Спостерігалось зниження також й спектральних показників ВСР. Так, загальна потужність спектра становила (951,6 ± 31,9) мс2 проти (3965,2 ± 27,6) мс2 у хворих I групи (p < 0,01) за рахунок всіх складових, але особливо високочастотних коливань ((4,8 ± 0,3) мс2 проти (6,9 ± 0,8) мс2 у I групі (p < 0,01), що відображує зниження сумарного впливу всіх спектральних компонентів на синусовий ритм. При цьому коефіцієнт LF/HF становив (2,7 ± 0,1) (p < 0,01), що також підтверджує превалювання симпатикотонії. Таким чином, поширення КМ відбувається через дисбаланс у ВНС у бік симпатикотонії та недостатність адаптаційно-компенсаторних реакцій.
У хворих із дисплазією (IV група) відзначається збільшення показника SDNN та показників RMSSD й pNN50 до значень, відповідальних за включення в регуляторний процес вагусних впливів. У цих хворих, на відміну від хворих інших груп, спостерігалось зниження індексу симпатовагальної взаємодії до (0,8 ± 0,2) ум.од., що свідчить про вагусну домінанту із виснаженням функціональних резервів організму і є несприятливою прогностичною ознакою.
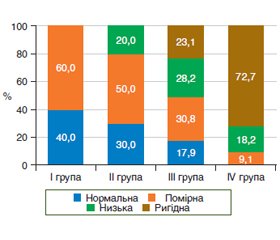
Розподіл рівнів вегетативного тонусу серед обстежених хворих наведено на рис. 1.
Як видно з наведених даних, з поширенням кишкової метаплазії починає превалювати симпатикотонічна ланка регуляції — до 71,8 % хворих III групи, тоді як у більшої кількості хворих з дисплазією (81,8 %) спостерігається парасимпатикотонічний вегетативний тонус.
Градуйовані критерії оцінки ВСР на основі часового та графічних методів наведені в табл. 2.
На рис. 2 відображені ступені зниження ВСР у хворих на атрофічний гастрит.
Слід зазначити, що з поширенням кишкової метаплазії у 51,3 % хворих III групи відзначалась низька та ригідна ВСР проти 20,0 % хворих II групи, що свідчить про несприятливий перебіг захворювання у цих хворих. У 60,0 % хворих II групи зустрічалась помірно знижена ВСР. Більша кількість хворих із дисплазією (72,7 %) знаходилась на рівні ригідної ВСР, що у сукупності з ваготонією апроксіювала обтяження хвороби.
Таким чином, з появою кишкової метаплазії у більшості хворих визначається зниження варіабельності серцевого ритму через активацію симпатикотонічного відділу ВНС та недостатню активність її парасимпатикотонічного відділу, що свідчить про зниження інтегрального впливу вегетативних механізмів регуляції та збільшення внеску гуморально-метаболічних впливів у вегетативну регуляцію.
Для лікування було відібрано 42 хворі із вегетативними розладами у вигляді симпатикотонії, 51 хворий із недостатньою стресостійкістю, 45 хворих зі зривом адаптації, 64 хворі із недостатнім функціональним резервом організму та 37 хворих із підвищеним серцево-судинним ризиком (табл. 3).
Після 10 сеансів лікування на програмно-апаратному комплексі Pure Purr у 76,2 % хворих із симпатикотонією збільшувалась парасимпатична активація до (0,90 ± 0,01) ум.од. (p < 0,05), 66,7 % хворих із зривом адаптації переходили в стадію резистентності, при цьому рівень показника RMSSD підвищувався до (28,8 ± 2,1) мс2 (p < 0,05); у 62,2 % хворих зменшувався СС-ризик із збільшенням показника SDNN до (66,4 ± 5,2) мс2 (p < 0,05); функціональний резерв організму нормалізувався у 76,6 % хворих на фоні достатньої стресостійкості із нормальними значеннями показників ТР та SI — (2530,8 ± 34,7) мс2 та (96,5 ± 12,4) мс2 відповідно (p < 0,05) (рис. 3).
Таким чином, у результаті проведеного лікування відзначена позитивна динаміка до значного збільшення варіабельності серцевого ритму шляхом підвищення її компонентів, що обумовлено впливом парасимпатичної нервової системи, запобігає посиленню симпатичних впливів і покращує перебіг захворювання та прогноз завдяки нормалізації адаптації, функціональних резервів та стресостійкості організму хворих на хронічний атрофічний гастрит.
Висновки
1. Вегетативна нервова система у хворих з преканцерозними станами шлунка функціонує у режимі дисбалансу її симпатичної та парасимпатичної ланок. З появою кишкової метаплазії зростає кількість хворих (66,1 %) із симпатикотонією та зривом адаптації. Майже у всіх хворих (81,8 %) із дисплазією спостерігалась ваготонія із виснаженням функціональних резервів організму, що є несприятливою прогностичною ознакою.
2. Зниження варіабельності серцевого ритму прогресувало у 51,3 % хворих із появою та поширенням кишкової метаплазії до низької та ригідної ВСР. Порушення адаптаційних процесів, СС-ризик, недостатність стресостійкості поглиблювались у групах із кишковою метаплазією та дисплазією.
3. Лікування хворих на хронічний атрофічний гастрит із вегетативними розладами повинно бути комплексним, із включенням апаратного комплексу з програмним забезпеченням нейростимуляції, що спрямовано на зниження гіперсимпатикотонії з підвищенням адаптаційного потенціалу організму.
4. Позитивну динаміку показників ВСР можна використовувати як об’єктивний критерій ефективності лікування.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів та власної фінансової зацікавленості при підготовці даної статті.
Інформація про фінансування. Робота виконується відповідно до плану наукових досліджень Державної установи «Інститут гастроентерології НАМН України». Усі пацієнти підписали інформовану згоду на участь у цьому дослідженні.
Внесок авторів у роботу над статтею. Мосійчук Л.М. — концепція та дизайн дослідження, редагування тексту; Зигало Е.В. — аналіз даних PRECISE-діагностики, написання статті; Шевцова О.М. — клінічний відбір пацієнтів; Сердюченко О.М. — проведення лікування хворих на програмно-апаратному комплексі Pure Purr; Петішко О.П. — статистична обробка отриманих даних, редагування статті.
Отримано/Received 10.01.2022
Рецензовано/Revised 22.01.2022
Прийнято до друку/Accepted 30.01.2022
/22_2.jpg)

/21.jpg)
/21_2.jpg)
/22.jpg)
/22_3.jpg)
/23.jpg)