Газета «Новости медицины и фармации» 6 (495) 2014
Вернуться к номеру
Тактика ведения пациентов с неполным ответом на терапию ингибиторами протонной помпы
Авторы: Peter J. Kahrilas, M.D. - профессор, Кафедра гастроэнтерологии и гепатологии, медицинский факультет Северо-Западного университета Фейнберг, Чикаго, Иллинойс, США; Guy Boeckxstaens, M.D. - профессор, Отделение гастроэнтерологии, Научно-исследовательский центр трансляционных исследований заболеваний желудочно-кишечного тракта (TARGID), Университетская клиника Левена, Католический университет Левена, Левен, Бельгия; Andre J.P.M. Smout, M.D. - профессор,
Отделение гастроэнтерологии и гепатологии, Академический медицинский центр, Амстердам, Нидерланды
Рубрики: Семейная медицина/Терапия, Терапия
Разделы: Клинические исследования
Версия для печати
Статья опубликована на с. 6-10 (Мир)
Ингибиторы протонной помпы (ИПП) позволяют удалить большую часть кислоты гастроэзофагеального рефлюксата. Тем не менее ИПП не устраняют рефлюкс сам по себе, а поэтому ответ на терапию ИПП определяется тем, насколько данные симптомы обусловлены воздействием соляной кислоты. По убыванию эффективности ИПП симптомы гастроэзофагеальной рефлюксной болезни (ГЭРБ) могут быть распределены следующим образом: изжога, отрыжка, боль за грудиной и экстраэзофагеальные проявления ГЭРБ. Поэтому при неполном ответе на терапию ИПП тщательный сбор анамнеза, уточнение перечня рефрактерных симптомов и определение их связи с рефлюксом имеют первостепенное значение. Наличие симптомов, несмотря на проводимую терапию ИПП, может быть следствием сохранения эпизодов кислого рефлюкса или обусловлено эпизодами слабокислого рефлюкса. При наличии возможных вариантов применение таких диагностических методов, как рН-мониторинг или рН-импеданс-мониторинг, становится неотъемлемой частью клинической практики. Антирефлюксное оперативное вмешательство представляет собой альтернативный подход для пациентов с установленной четкой взаимосвязью между персистирующими симптомами, в особенности отрыжкой, и рефлюксом. Устранение висцеральной гиперчувствительности может быть эффективным в субпопуляции пациентов с симптомами ГЭРБ, обусловленными данным механизмом.
Терапия ингибиторами протонной помпы во многом изменила клинический облик гастроэзофагеальной рефлюксной болезни. До внедрения в практику ИПП в 1989 г. клиницисты с трудом добивались контроля у пациентов с ГЭРБ имеющимися на то время лекарственными средствами, доминирующее место среди которых занимали антагонисты гистаминовых рецепторов 2-го типа. Пациенты, рефрактерные к терапии, на тот момент без труда выявлялись с использованием эндоскопии, при которой обнаруживались персистирующие эрозии слизистой оболочки, язвы и рецидивирующие стриктуры. Однако данные проблемы были решены путем мощного подавления кислотообразующей функции париетальных клеток желудка, что стало возможным в результате применения ИПП. В настоящее время общепризнано, что проявления ГЭРБ на слизистой оболочке пищевода (за исключением метаплазии Барретта) могут быть на неопределенный срок устранены при непрерывной терапии ИПП [1]. Неудивительно, что вследствие этого использование ИПП в клинической практике значительно расширилось, а терапевтический ассортимент пополнился множеством альтернативных средств.
Последовавшая за этим эйфория, связанная с применением ИПП, усилилась на рубеже столетий, приведя многих врачей к выводу о том, что данные препараты не только чрезвычайно эффективны в лечении ГЭРБ, но и что ответ на терапию ИПП представляет собой метод клинического подтверждения наличия ГЭРБ у пациентов [2]. Если наблюдается уменьшение выраженности симптомов у пациента при терапии ИПП, он страдает ГЭРБ, и наоборот, если терапия ИПП не привела к облегчению симптомов, диагноз ГЭРБ неправомочен. Конечно же, данный вывод был ошибочным, так же как, например, и диагностика ревматоидного артрита на основании улучшения при приеме аспирина [3]. Хотя верно и то, что в большинстве случаев пациенты с ревматоидным артритом ответят на терапию аспирином, как верно и то, что пациенты со многими другими заболеваниями ответят на терапию аспирином. Кроме того, нельзя не учитывать эффект плацебо. Аналогия с ГЭРБ является очевидной.
Широкое применение ИПП, ставшее возможным благодаря их внедрению в практику, способствовало более глубокому пониманию всего спектра ГЭРБ. Была организована международная консенсусная конференция, задачей которой стала разработка современного определения ГЭРБ. Сформулированное Монреальское определение характеризует ГЭРБ как «состояние, которое развивается, когда рефлюкс желудочного содержимого вызывает причиняющие беспокойство симптомы и/или осложнения» [4]. Кроме того, в процессе работы над консенсусом были рассмотрены связанные со здоровьем показатели качества жизни, имеющие отношение к важнейшим симптомам рефлюксной болезни, а именно к изжоге и регургитации, для определения степени причиняемого ими беспокойства. В случае изжоги порог, при котором симптом становится «причиняющим беспокойство», был определен исходя из клинически значимого снижения качества жизни и установлен при наличии симптомов легкой степени выраженности в течение ≥ 2 дней в неделю и наличии симптомов умеренной выраженности ≥ 1 дня в неделю. Не предполагалось определение порогов для других возможных симптомов ГЭРБ ввиду отсутствия соответствующих данных в литературе. И все же неспособность в достаточной мере устранить симптомы ГЭРБ стала одной из наиболее частых причин консультаций гастроэнтерологов в США и странах Западной Европы [5]. В данном фундаментальном обзоре будут рассмотрены многие аспекты данной клинической проблемы и предложен системный подход к ее решению.
Фенотипы неполного ответа на терапию ИПП
По оценкам, у 10–40 % пациентов с ГЭРБ наблюдается неполный ответ на назначаемые ИПП в стандартных дозах или таковой ответ вообще отсутствует [6, 7]. Несмотря на то, что нечувствительность к ИПП может быть использована в качестве объединяющего клинико-диагностического признака, данная группа пациентов представляется чрезвычайно гетерогенной, так как, несмотря на то, что терапия ИПП направлена на угнетение секреции желудочной кислоты, у пациентов с ГЭРБ обычно наблюдается нормальная секреция желудочной кислоты. Более вероятно, что первичная патофизиология ГЭРБ связана с чрезмерными или патологическими эпизодами заброса желудочного содержимого, замедленным пищеводным клиренсом или нарушенной чувствительностью слизистой оболочки пищевода (рис. 1).
Любой из данных механизмов может доминировать в патофизиологии каждого конкретного симптома ГЭРБ. Так, у большинства пациентов, ощущающих изжогу, даже до начала лечения не наблюдается признаков рефлюкс-эзофагита. Кроме того, данное несоответствие становится еще более выраженным у пациентов с атипичными симптомами ГЭРБ. К тому же не найден доминирующий патофизиологический механизм, позволяющий разграничить эзофагит и неэрозивную рефлюксную болезнь (НЭРБ) при большом количестве случаев рефлюкса; скорее замедленный клиренс пищевода от рефлюксата может относиться к последствиям грыжи пищеводного отверстия диафрагмы или слабой перистальтики [9, 10]. Фактически замедленный пищеводный клиренс коррелирует как с тяжестью эзофагита, так и с наличием метаплазии Барретта [11, 12]. Эффективность пищеводного клиренса значительно снижается у пациентов с грыжей пищеводного отверстия диафрагмы, у которых возникает заброс содержимого желудка во время глотательной релаксации в горизонтальном положении [13, 14].
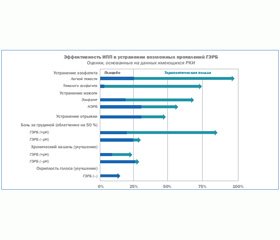
В целом стратегии лечения рефлюкса нацелены на отдельные элементы патофизиологии ГЭРБ, которые отражены на рис. 1. К сожалению, медикаментозная терапия имеет минимальную эффективность в коррекции такого патофизиологического механизма, как нарушение пищеводного клиренса, однако модификация образа жизни, заключающаяся в пребывании в вертикальном положении спустя несколько часов после приема пищи и в приподнимании головного конца кровати во время сна, позволяет успешно корректировать его [1]. Избыточная масса тела признается важным патофизиологическим фактором рефлюкса; кроме того, висцеральная чувствительность также является важным модулятором тяжести симптомов рефлюкса, а в случае рефлюкс-индуцированного кашля является ключевым патофизиологическим механизмом [15]. Тем не менее до сих пор методы лечения, направленные на данный патофизиологический механизм, неспецифичны и находятся на этапе изучения [16]. В то же время губительное воздействие желудочного сока на эпителиальные клетки пищевода, являющееся ключевым элементом в патогенезе эзофагита, оказалось отличной фармакологической мишенью. Однако доминирующая роль кислоты желудочного сока в патогенезе других синдромов, помимо эзофагита, уменьшается. Клинические последствия данного наблюдения представлены на рис. 2, на котором сравнивается эффективность ИПП в лечении ГЭРБ-ассоциированного эзофагита и других симптомов, ассоциированных с ГЭРБ [8]. На рис. 2 видно, что эффективность ИПП в контроле симптомов прогрессивно снижается от эзофагита к симптоматической изжоге, регургитации [18, 19], боли в грудной клетке [20], кашлю [21, 22] и ларингиту [17]. Улучшение терапевтических результатов зависит от поиска альтернативных стратегий лечения, которые обладают большей эффективностью в предотвращении рефлюкса, или же от воздействия на сопутствующие заболеванию факторы, которые, в свою очередь, являются такими же важными, как и данные симптомы.
Даже в сфере типичных симптомов со стороны пищевода (изжога, регургитация, боль в груди) существуют различные фенотипы неполного ответа на терапию ИПП. Нужно также учитывать, что ни один из данных симптомов не является на 100 % специфичным для ГЭРБ. Отсюда следует, что персистирующая изжога, регургитация или боль в грудной клетке могут быть следствием эзофагита иной этиологии (эозинофильной, инфекционной, медикаментозной), тяжелого нарушения моторной функции пищевода (ахалазии), руминации (срыгивание и повторное пережевывание пищи), функциональной изжоги или функциональной боли в грудной клетке. Кроме того, среди больных с ГЭРБ наблюдаются случаи, когда симптомы, ассоциированные с рефлюксом, сохраняются, несмотря на проводимую терапию ИПП. Это может быть результатом недостаточной супрессии кислотообразования при персистирующем рефлюксе или же результатом слабокислого рефлюкса. С учетом такого широкого спектра возможных вариантов, а также того, что не существует терапевтической стратегии, подходящей всем, диагностический процесс является неотъемлемой частью ведения данных пациентов.
Диагностические методы
Сбор анамнеза и опрос больного
В случае неполного ответа на проводимую терапию ИПП крайне важно пересмотреть симптомы, имеющиеся у пациента. Какие из них, предположительно, обусловлены рефлюксом и какие не полностью разрешились при терапии ИПП? Изжога, определяющаяся как болезненное ощущение жжения за грудиной сравнительно небольшой продолжительности, является наиболее характерным симптомом рефлюкса и лучше остальных отвечает на кислотоугнетение. Регургитация, определяемая как заброс желудочного содержимого в пищевод или ротовую полость, также является характерным симптомом рефлюкса, но данный симптом, как известно, менее чувствителен к терапии ИПП [18, 19]. Наименее вероятно устранение с помощью ИПП таких экстраэзофагеальных симптомов, как охриплость, боль в горле, астма и кашель, отчасти это обусловлено тем, что в большинстве случаев рефлюкс не является непосредственной причиной их возникновения [23]. Насколько выраженными были симптомы до начала лечения? Пациенты с тяжелыми симптомами до начала лечения с меньшей вероятностью ответят на терапию ИПП в достаточной степени [24].
Различные опросники были разработаны для оценки степени тяжести и частоты симптомов ГЭРБ. Несмотря на то, что некоторые из них были утверждены и их использование дало воспроизводимые результаты, их применение не повышает точность диагностики ГЭРБ [25]. Это неудивительно, так как высокая степень тяжести диспептических симптомов перед лечением является прогностически неблагоприятным фактором в плане полноты ответа на последующую терапию ИПП [26]. В двух крупных рандомизированных исследованиях с использованием опросника Reflux Disease Questionnaire благоприятный эффект от кислотосупрессии относительно иных сопутствующих симптомов, в особенности боли за грудиной и диспептической боли, был меньшим по сравнению с таковым для симптома жжения за грудиной [27]. Наконец, нет никаких определенных данных, подтверждающих целесообразность клинического использования опросников в качестве диагностических тестов у пациентов с резистентной к терапии ГЭРБ.
Эндоскопическое исследование
Американское общество гастроинтестинальной эндоскопии рекомендует проведение эндоскопического исследования пациентам с «симптомами ГЭРБ, персистирующими или прогрессирующими, несмотря на адекватную медикаментозную терапию» [28]. В таких случаях при эндоскопическом исследовании может быть выявлена альтернативная причина имеющихся симптомов, как, например, эозинофильный, инфекционный или медикаментозный эзофагит или даже ахалазия кардии. Тем не менее при эндоскопии может быть выявлен и рефлюкс-эзофагит, несмотря на то, что общепризнанной является низкая вероятность нахождения его у пациента, получающего терапию ИПП в полной дозе и с высоким уровнем приверженности к терапии. Так, в исследовании с участием 105 пациентов с сохраняющейся симптоматикой, несмотря на проводимую терапию ИПП, эрозивные изменения (степени А или В по классификации Los Angeles) были обнаружены лишь у 6,7 % из них [29]. В другом недавно проведенном исследовании, в которое были включены только пациенты с наличием эзофагита, у 31,4 % пациентов с неполным ответом на терапию ИПП был выявлен эрозивный гастрит степени А или В по классификации Los Angeles [30]. К другим возможным эндоскопическим находкам, подтверждающим диагноз ГЭРБ, относятся пептический стеноз, метаплазия Барретта и грыжа пищеводного отверстия диафрагмы. Однако ни одно из этих состояний достоверно не свидетельствует в пользу того, что имеющиеся у пациента симптомы обусловлены рефлюксом.
Гистологическое исследование
При исследовании биоптатов слизистой оболочки пищевода, полученных у пациентов с ГЭРБ, может быть выявлено удлинение сосочков и гиперплазия клеток базального слоя с расширенными межклеточными пространствами [31–33]. Поэтому хотя и сообщается, что обнаружение расширенных межклеточных пространств более характерно для пациентов с неполным ответом на терапию ИПП [33], большая вариабельность результатов у разных исследователей, низкие чувствительность и специфичность в значительной мере ограничивают диагностическую значимость гистологического исследования при ГЭРБ. Также не установлено, насколько значимым является обнаружение повышенного числа эозинофилов в слизистой оболочке при лечении пациентов с рефрактерной ГЭРБ. Тем не менее рекомендуется выполнение биопсии пищевода, если предполагается эозинофильный эзофагит, особенно если дисфагия присутствует в настоящий момент как симптом.
Пищеводный рН-мониторинг
Пищеводный рН-мониторинг традиционно проводится в течение 24 ч с использованием портативного регистратора данных и трансназального катетера, на пищеводном конце которого вмонтирован рН-электрод. Во время исследования электрод располагают на 5 см выше верхнего края определенного манометрически нижнего пищеводного сфинктера (НПС). Недавно популярность приобрел дистанционный рН-мониторинг (Bravo). При использовании данного метода капсулу, содержащую рН-электрод и радиопередатчик, прикрепляют к слизистой оболочке пищевода таким образом, чтобы электрод был расположен на 6 см проксимальнее эндоскопически определенной зоны перехода плоского эпителия пищевода в цилиндрический. Преимуществами данной технологии является отсутствие дискомфорта, вызванного пребыванием назопищеводного катетера, и возможность более длительного рН-мониторирования (до 48–96 ч). Однако применение беспроводной технологии рН-мониторинга значительно дороже традиционной методики. Результаты, полученные при использовании двух данных методик, характеризуются достаточной сопоставимостью, но могут быть и неидентичными [34, 35].
Два вида данных о гастроэзофагеальном рефлюксе могут быть получены с использованием рН-мониторинга: 1) количественные данные о величине кислотной экспозиции в пищеводе, обычно выражаемые в виде процента времени с рН < 4; 2) временная взаимосвязь между симптомами пациента и зарегистрированными эпизодами рефлюкса. Симптом считается ассоциированным с рефлюксом в том случае, если он возникает в течение 2 мин от момента начала эпизода рефлюкса. Результаты оценки взаимосвязи могут быть выражены в виде индексов, таких как, например, индекс симптомов или индекс вероятности взаимосвязи симптомов [36, 37]. Важность оценки взаимосвязи симптомов у пациентов с неполным ответом на терапию ИПП заключается в том, что она позволяет отличить рефлюкс-ассоциированные симптомы от функциональной изжоги [38]. Последняя определяется как наличие изжоги при отсутствии свидетельств того, что она вызвана рефлюксом. В ходе обследования пациента с неполным ответом на терапию ИПП идеальным является проведение рН-мониторинга не менее чем через 5 дней после отмены любой кислото-супрессивной терапии, так как основная цель данного исследования заключается в достоверном определении наличия ГЭРБ у пациента, а эпизоды рефлюкса не могут быть достоверно идентифицированы с помощью рН-мониторинга при приеме пациентом ИПП.
Комбинированный рН-импеданс-мониторинг
Учитывая, что рН-мониторинг не позволяет выявлять эпизоды некислого рефлюкса, методика внутрипросветной импедансометрии пищевода позволяет обнаруживать все возможные типы рефлюксов (кислые и слабокислые, рефлюкс жидкости и/или газа) [39]. Так как методика данного исследования предполагает использование массива электродов на протяжении практически всей длины пищевода, становится возможным установить направление движения порций жидкости или газа. Импедансометрия, как правило, комбинируется с рН-мониторингом, что достигается использованием рН-электродов, вмонтированных в катетер для импедансометрии, что также делает возможной оценку кислотности рефлюксата. Регистрация эпизодов не только кислого рефлюкса (рН < 4), но и слабокислого (рН 4–7) является актуальной, поскольку было установлено, что эпизоды слабокислого рефлюкса могут вызывать симптомы, в том числе и изжогу [40]. Использование методики импедансометрии позволяет регистрировать эпизоды гастроэзофагеального рефлюкса у пациентов, продолжающих прием ингибиторов кислотообразования.
Существуют противоположные точки зрения относительно проведения импедансометрии у пациентов с неполным ответом на терапию ингибиторами кислотообразования. С одной стороны, можно утверждать, что целью импедансометрии у данных пациентов является определение того, обусловлены ли симптомы, оставшиеся у пациента, эпизодами рефлюкса или нет, а поэтому данное исследование следует проводить без отмены ИПП. Однако, как и при рН-мониторинге, вероятность установления причинной связи между симптомами рефлюкса и эпизодами рефлюкса при рН-импедансометрии выше при отмене ИПП на время проведения исследования [41]. Поэтому целесообразным является проведение рН-импеданс-мониторинга после отмены ИПП в тех случаях, когда диагноз ГЭРБ окончательно не подтвержден, и проведение исследования без отмены ИПП в тех случаях, когда диагноз ГЭРБ установлен, а основной вопрос заключается в поиске причины неэффективности лечения.
Манометрия
В целом результаты манометрии не обладают достаточно высокой специфичностью и чувствительностью для диагностики ГЭРБ, также отсутствуют и доказательства того, что результаты манометрии у пациентов с неполным ответом на терапию каким-либо образом отличаются от таковых у пациентов с удовлетворительным ответом на терапию. Тем не менее манометрия позволяет правильно определить место для расположения рН-электрода, а также выявить редкие случаи, когда ахалазия кардии ошибочно диагностируется как ГЭРБ [42]. Ошибочный диагноз ГЭРБ у пациентов с ахалазией кардии возможен вследствие того, что изжога наблюдается у 35 % пациентов с ахалазией [43]. И наконец, манометрия может быть полезной в диагностике синдрома руминации. Оптимальным в данном случае является сопутствующее проведение рН-импеданс-мониторинга [44].
Фармакологические возможности
Хотя ИПП, несомненно, и являются наиболее широко применяемыми препаратами в лечении пациентов с ГЭРБ, по-прежнему заслуживает внимания тот факт, что пациенты не всегда получают корректные указания о времени приема ИПП относительно приема пищи. В данном аспекте огромное значение приобретает тот факт, что ИПП селективно взаимодействуют с активно секретирующими протонными помпами и ингибируют лишь их. Отсюда было достоверно установлено, что прием ИПП перед едой, особенно перед завтраком, наиболее эффективно подавляет кислотообразование [45]. Тем не менее недавно проведенный опрос 100 пациентов с ГЭРБ, принимающих ИПП, показал, что лишь у 46 % режим дозирования является оптимальным (то есть за 1 ч до приема пищи) и только 12 % принимали ИПП в режиме, позволяющем достичь максимального подавления кислотообразования (за 15–30 мин до завтрака) [46]. Отсюда следует, что оптимизация режима дозирования ИПП должна быть первым шагом в решении проблемы неполного ответа на проводимую терапию и что она должна предшествовать повышению дозы или смене препарата.
Двойные дозы ИПП
Удвоение дозы ИПП является одной из наиболее распространенных мер, предпринимаемых с целью улучшения контроля над симптомами у пациентов с неполным ответом на терапию ИПП. Однако объективные данные, свидетельствующие в пользу данного подхода, немногочисленны. Так, по результатам нескольких исследований, хотя увеличение дозы ИПП (принимавшихся как 1 раз, так и 2 раза в сутки) и приводило к более полному подавлению кислотообразования в желудке, это не сопровождалось уменьшением экспозиции кислоты в пищеводе и, что более важно, уменьшением симптомов со стороны пищевода (в частности, изжоги) [47]. С целью повышения контроля над симптомами ГЭРБ нередко применяется переход на альтернативный ИПП. Так, в одном из исследований пациенты с персистирующими симптомами, несмотря на прием 30 мг лансопразола в сутки, переводились на терапию лансопразолом в удвоенной дозе (30 мг 2 раза в сутки) или на терапию эзомепразолом в дозе 40 мг/сут на 8 нед. Оба использованных подхода обладали одинаковой эффективностью в контроле над изжогой [48]. И в заключение следует отметить, что появление современных препаратов, обладающих новыми механизмами подавления кислотообразования, не позволяет достичь лучших результатов в контроле симптомов ГЭРБ, чем те, которые достигаются при использовании уже существующих ИПП. Так, например, калий-конкурентный ингибитор кислотообразования AZD0865, обеспечивающий практически полное и немедленное угнетение секреции протонов водорода, не превосходит эзомепразол по эффективности контроля симптомов ГЭРБ у пациентов как с эрозивной, так и с неэрозивной формой [49, 50]. В совокупности эти наблюдения свидетельствуют о том, что достигнуто плато в корреляции между степенью подавления кислотообразования и выраженностью симптомов, то есть дальнейшее подавление кислотообразования не дает возможности более полно контролировать симптомы. С учетом этого более целесообразным представляется изучение альтернативных увеличению дозы ИПП подходов.
Комбинированная терапия ИПП и антагонистами Н2-рецепторов
Секреция кислоты в ночное время, главным образом опосредованная гистамином, в меньшей степени отвечает на терапию ИПП, о чем свидетельствует снижение уровня внутрижелудочного рН в ночное время даже у пациентов, получающих двойные дозы ИПП. Данный феномен назван ночным кислотным прорывом [51]. Результатом данного наблюдения стало предположение о том, что ночной кислотный прорыв является возможной причиной резистентности симптомов ГЭРБ к проводимой терапии. Как следствие этого, были проведены исследования эффективности комбинированного применения ИПП и антагонистов Н2-рецепторов с назначением последних на ночь. В доказательство гипотезы исследования с мониторингом рН продемонстрировали, что кратковременная блокада Н2-рецепторов действительно улучшает контроль уровня внутрижелудочного рН в ночное время и сопровождается уменьшением симптомов ГЭРБ [52]. Однако в последующих исследованиях было установлено, что степень уменьшения симптомов не зависела от исходной выраженности ночного кислотного прорыва, указывая на ограниченную клиническую значимость данного феномена. Кроме того, при длительной терапии (28 дней) не было выявлено различий в показателях контроля желудочной секреции между группой приема ИПП (2 раза в сутки) и группой терапии ИПП в сочетании с антагонистом Н2-рецепторов, что обусловлено развитием резистентности [53]. Это является доводом против добавления антагонистов Н2-рецепторов к ИПП в базисной терапии ГЭРБ.
Комбинированная терапия ИПП и прокинетиками
С учетом того, что более агрессивное подавление кислотообразования не является эффективным в уменьшении симптомов ГЭРБ, улучшение клиренса рефлюксата из пищевода может быть эффективным терапевтическим подходом. Vigneri et al. исследовали эффективность данного подхода у пациентов, страдающих ГЭРБ с эндоскопически подтвержденным эзофагитом [54]. По результатам проведенного 12-месячного исследования, комбинированная терапия цизапридом и ранитидином была более эффективной в уменьшении болевого синдрома, чем монотерапия ранитидином, однако синергизм отсутствовал при добавлении цизаприда к терапии омепразолом. Идентичные результаты получены в недавно проведенном исследовании мосаприда цитрата, прокинетика, являющегося 5-НТ4-агонистом и 5-НТ3-антагонистом [55]. Двести пациентов с НЭРБ были рандомизированы на получение омепразола (10 мг ежедневно) или омепразола и мосаприда (5 мг 3 раза в сутки) на протяжении 4 нед. Не было выявлено отличий в контроле симптомов между двумя группами. В совокупности эти данные не свидетельствуют в пользу целесообразности добавления прокинетика к терапии ИПП у пациентов с ИПП-резистентными симптомами ГЭРБ.
Агенты, образующие альгинатный «плот»
Недавно полученные, представляющие большой интерес данные указывают на то, что гастроэзофагеальный рефлюкс, в особенности постпрандиальный, возникает из-за скопления слоя желудочного сока на поверхности содержимого желудка [56, 57]. Этот «кислотный карман» из вновь образованного желудочного сока не смешивается с пищей и может обнаруживаться в области пищеводно-желудочного соединения в течение 20 мин после приема пищи. Он представляет собой новый объект для терапии, направленной на уменьшение постпрандиальной изжоги [58, 59]. В опытах in vitro было обнаружено, что альгинаты, то есть анионные полисахариды, широко распространенные в клеточной стенке бурых водорослей, образуют плавающий «плот» в присутствии кислоты и ионов кальция. Образующийся «плот», возможно, является физическим барьером для рефлюкса или повышает вязкость рефлюксата, препятствуя тем самым возникновению гастроэзофагеального рефлюкса. В настоящее время альгинаты, нередко в комбинации с антацидами, используются в качестве безрецептурных средств при изжоге и обладают доказанной эффективностью в ее уменьшении, а также достоверно уменьшают время экспозиции кислоты в пищеводе у пациентов с ГЭРБ [60]. В соответствии с данными результатами Rohof et al. недавно продемонстрировали, что при приеме после еды альгинаты скапливаются в «кислотном кармане» и уменьшают количество эпизодов кислого рефлюкса и кислотную экспозицию в пищеводе у пациентов с ГЭРБ более эффективно, чем антациды [61]. Полученные данные свидетельствуют в пользу того, что альгинаты обладают возможностью уменьшать выраженность ИПП-резистентного рефлюкса путем непосредственного воздействия на «кислотный карман». В своем исследовании Manabe et al. рандомизировали 76 пациентов с НЭРБ на прием омепразола в дозе 20 мг/сут или омепразола в сочетании с натрия альгинатом [62]. Полное устранение изжоги не менее чем на 7 дней подряд к окончанию 4-й недели лечения значительно чаще наблюдалось в группе комбинированной терапии (57 %), чем в группе монотерапии омепразолом (26 %). Несмотря на то, что требуется дополнительное подтверждение эффективности данного терапевтического подхода, результаты данного исследования указывают, что альгинаты могут быть эффективны в устранении симптомов ГЭРБ, резистентных к терапии ИПП. На практике же возможно, что пациенты, страдающие ГЭРБ, самостоятельно используют данную терапевтическую стратегию, о чем свидетельствуют результаты опроса, недавно проведенного в США, согласно которым 42 % пациентов, получающих терапию ИПП, используют и другие препараты, в том числе безрецептурные, для контроля симптомов ГЭРБ [63].
Ингибиторы рефлюкса
Несмотря на то, что на фоне терапии ИПП количество эпизодов кислого рефлюкса уменьшается, общее количество эпизодов рефлюкса при этом остается прежним [64]. Таким образом, большинство эпизодов рефлюкса, выявляемых у пациентов с ГЭРБ, находящихся на терапии ИПП, являются слабокислыми [65]. С учетом того, что и эпизоды слабокислого рефлюкса являются причиной симптомов при ГЭРБ, в идеале терапия ГЭРБ должна быть направлена на устранение эпизодов как кислого, так и слабокислого рефлюкса. Одной из стратегий достижения данной цели является воздействие на основной механизм, лежащий в основе гастроэзофагеального рефлюкса, а именно на транзиторные релаксации нижнего пищеводного сфинктера (ТРНПС). ТРНПС представляют собой пролонгированные релаксации НПС, сопровождаемые расслаблением ножек диафрагмы и укорочением пищевода, что способствует возникновению рефлюкса. Следует отметить, что описанный процесс является физиологическим механизмом отрыжки. Интересно, что агонист ГАМК-В-рецепторов баклофен не только уменьшает количество ТРНПС как у животных, так и у людей, но и уменьшает количество эпизодов кислого и слабокислого рефлюкса у здоровых волонтеров и у пациентов, страдающих ГЭРБ [8]. С учетом того, что терапия баклофеном может провоцировать развитие головокружения и сонливости, были разработаны более мощные агонисты ГАМК-В-рецепторов периферического действия, или пролекарства баклофена, с целью избежать ГАМК-опосредованных побочных эффектов со стороны центральной нервной системы (ЦНС). Но, к сожалению, хотя данные препараты и снижают количество ТРНПС приблизительно на 30–40 %, их низкая клиническая эффективность и побочные эффекты (гепатотоксичность, побочные эффекты со стороны ЦНС) привели к прекращению их использования в клинической практике [8, 66, 67], а также к прекращению разработки новых ингибиторов рефлюкса. Тем не менее при условии хорошей переносимости добавление баклофена к ИПП остается ценным терапевтическим подходом в устранении ИПП-резистентных симптомов ГЭРБ [68].
Низкие дозы антидепрессантов
Антидепрессанты обладают способностью модулировать чувствительность пищевода на уровне центральной нервной системы и/или на уровне периферического афферентного звена и, следовательно, потенциальной пользой в контроле симптомов ГЭРБ. Более конкретно, в одном из исследований низкие дозы трициклических антидепрессантов были эффективны в устранении загрудинной боли, которая лишь частично облегчалась приемом ИПП [69]. Аналогичным образом тразодон, ингибитор обратного захвата серотонина, превосходил по эффективности плацебо в облегчении симптомов со стороны пищевода (боль за грудиной, дисфагия, изжога и/или отрыжка), ассоциированных с нарушением моторной функции пищевода [70]. Циталопрам, другой селективный ингибитор обратного захвата серотонина, значительно повышал порог восприятия боли и дискомфорта после баллонной дилатации у здоровых волонтеров [71].
Немедикаментозные методы
Акупунктура и гипнотерапия также были предложены в качестве терапевтических альтернатив для лечения пациентов, страдающих ГЭРБ. В одной серии наблюдений включение в терапию иглоукалывания 30 пациентам (без контрольной группы) с неполным ответом на терапию ИПП по эффективности значительно превосходило удвоение дозы ИПП в контроле таких симптомов, как отрыжка кислым и изжога [72]. Ответ на терапию ИПП в немалой степени зависит от психологического состояния пациента [73]. Поэтому коррекция психологических нарушений может быть целесообразной в популяции пациентов с неполным ответом на терапию ИПП. Гипнотерапия была предложена в качестве альтернативной терапии, в особенности для пациентов с атипичными симптомами ГЭРБ. В рандомизированном клиническом исследовании с участием 28 пациентов с загрудинной болью некардиального генеза в группе гипнотерапии было отмечено значительно более частое разрешение данного симптома, чем в контрольной группе (80 и 23 % соответственно). Аналогичным образом в серии случаев у пациентов с ощущением комка за грудиной была отмечена эффективность гипнотерапии [74]. Тем не менее эффективность данных альтернативных методов предстоит определить в более крупных когортах пациентов с ГЭРБ-ассоциированными симптомами.
Хирургическая фундопликация
Доказательства высокого качества эффективности антирефлюксных оперативных вмешательств имеются лишь в отношении эзофагита и/или избыточного воздействия кислоты желудочного сока на дистальные отделы пищевода (по результатам рН-мониторинга) при условии, что терапия ИПП не проводилась. При этом в контролируемых клинических исследованиях было продемонстрировано, что антирефлюксные оперативные вмешательства обладают эффективностью, по меньшей мере сравнимой с таковой ИПП, в контроле изжоги и кислых регургитаций. Наилучшим примером этого являются результаты недавно опубликованного масштабного рандомизированного клинического исследования LOTUS, проведенного на территории Европы, целью которого было сравнение оперативного лапароскопического и медикаментозного (эзомепразол) подходов в лечении пациентов с хронической ГЭРБ [75]. Диагноз ГЭРБ устанавливался на основании типичных симптомов и эндоскопического выявления характерных изменений слизистой оболочки пищевода и/или патологических отклонений по результатам рН-мониторинга. В исследование рандомизировали только пациентов с клиническим ответом на терапию эзомепразолом на протяжении вводного периода длительностью 3 мес. К концу 3-летнего периода наблюдения оба подхода характеризовались сопоставимой эффективностью в достижении полной симптоматической ремиссии. Через 5 лет частота сохраняющейся ремиссии была выше в группе эзомепразола, чем в группе выполненной лапароскопической фундопликации (92 и 85 %, р = 0,048) [76]. При анализе по отдельным симптомам также были выявлены отличия между группами. Так, регургитация наблюдалась значительно чаще в группе медикаментозного лечения, чем в группе хирургического вмешательства (13 и 2 % соответственно, p < 0,001), в то время как не было выявлено отличий в частоте изжоги между двумя группами. Дисфагия, вздутие живота и метеоризм были значительно более распространены в группе фундопликации по сравнению с группой терапии ИПП. Поэтому потенциальная польза антирефлюксного оперативного вмешательства должна быть противопоставлена появлению новых симптомов после оперативного вмешательства, таких как дисфагия, метеоризм, неспособность к отрыжке и симптомы со стороны кишечника.
Другим практическим ограничением антирефлюксных оперативных вмешательств является высокая зависимость их эффективности от опытности выполняющего их хирурга. Данные относительно эффективности, полученные в условиях реальной клинической практики [77], значительно отличаются от результатов исследования LOTUS. Так, около 30 % пациентов возобновляют прием ИПП на протяжении первых пяти лет после оперативного вмешательства. В некоторых специализированных центрах повторные фундопликации составляют до 50 % оперативных вмешательств, выполняемых по данному поводу [78]. Учитывая это, следует с определенной степенью осторожности рекомендовать пациентам антирефлюксное оперативное вмешательство. Вероятность получения пользы в результате антирефлюксного оперативного вмешательства выше у пациентов с эзофагитом и отсутствующим эффектом от терапии ИПП. И наоборот, вероятно, что пациенты с эзофагитом с хорошим ответом на терапию ИПП не получат пользы от антирефлюксного оперативного вмешательства, а дополнительный риск повышается. У пациентов с эзофагеальными симптомами ГЭРБ, которые плохо контролируются приемом ИПП, оперативное вмешательство может принести пользу, в особенности при наличии персистирующей отрыжки. Учитывая это, необходимо тщательно оценивать соотношение пользы от оперативного вмешательства и возможного риска, а также информировать пациентов о возможном развитии дисфагии, неспособности к отрыжке, метеоризма и симптомов со стороны кишечника.
Выводы
Рефлюксная болезнь обусловлена физиологической дисфункцией пищеводно-желудочного соединения, что приводит к избыточному рефлюксу содержимого желудка в пищевод. Прямым следствием этого может быть развитие эзофагита. Поэтому уменьшение кислотности желудочного сока, достигаемое назначением ИПП, является весьма эффективным в лечении эзофагита. Тем не менее ИПП не устраняют эпизоды рефлюкса, а ответ на терапию ИПП зависит от того, насколько данные симптомы были обусловлены воздействием соляной кислоты желудочного сока. Таким образом, неудивительно, что ИПП обладают большей эффективностью в устранении изжоги и в значительно меньшей степени помогают устранить отрыжку, боль за грудиной и экстраэзофагеальные проявления ГЭРБ. Даже в отношении изжоги эффективность ИПП значительно уступает таковой в устранении эзофагита. Таким образом, в случае неполного ответа на терапию ИПП основной вопрос заключается в том, являются ли оставшиеся у пациента симптомы следствием рефлюкса или нет. Тщательный сбор анамнеза, уточнение рефрактерных симптомов, а также установление связи этих симптомов с ГЭРБ имеют первостепенное значение. Так, даже при типичных для ГЭРБ симптомах со стороны пищевода стойкая изжога, отрыжка или боль за грудиной могут быть следствием эзофагита иной этиологии (эозинофильной, инфекционной, медикаментозной), нарушения моторной функции пищевода, руминации, функциональной изжоги или функциональной боли за грудиной. Однако следует учитывать, что симптомы, характерные для ГЭРБ и не устраняющиеся терапией ИПП, могут быть также обусловлены сохраняющимся кислым рефлюксом и эпизодами слабокислого рефлюкса. Учитывая такой широкий спектр возможностей и то, что на данный момент нет терапевтической стратегии, подходящей всем, такие диагностические методы, как рН-мониторинг или рН-импеданс-мониторинг, в настоящее время становятся неотъемлемыми инструментами в клинической практике. У пациентов с сохраняющейся отрыжкой, несмотря на проводимую терапию ИПП, уменьшение частоты эпизодов рефлюкса может быть важной терапевтической мишенью. Антирефлюксное оперативное вмешательство является основной альтернативой для этих больных при условии, что установлена четкая причинная связь между сохраняющимися симптомами, в частности отрыжкой, и рефлюксом. И наконец, устранение висцеральной гиперчувствительности может быть эффективным в субпопуляции пациентов с симптомами ГЭРБ, обусловленными данным механизмом. На рис. 3 представлен алгоритм ведения пациентов с ИПП-рефрактерными симптомами.
Практические моменты
— У пациентов с неполным ответом на терапию ИПП сохраняющиеся симптомы могут быть обусловлены персистирующим рефлюксом или причинами, не связанными с рефлюксной болезнью.
— Тщательный сбор анамнеза с целью уточнения симптомов и определения их связи с ГЭРБ имеет первостепенное значение.
— Применение диагностических методов (рН-мониторинг и рН-импеданс-мониторинг) имеет крайне важное значение в разделении пациентов, имеющих персистирующие симптомы, на группы пациентов с рефрактерными симптомами рефлюкса, с функциональными симптомами и с висцеральной гиперчувствительностью.
Потребность в исследованиях
— Понимание, определение и лечение пищеводной гиперчувствительности.
— Определение роли рефлюкса в генезе экстраэзофагеальных синдромов.
— Лечение функциональной изжоги и функциональной диспепсии.
Список литературы находится в редакции

/8_m/8_m.jpg)
/8_m/8_m2.jpg)
/10_m/10_m.jpg)