Международный эндокринологический журнал Том 20, №4, 2024
Вернуться к номеру
Асоціація поліморфізмів генів β1-, β2-адренорецепторів з ризиком розвитку серцевої недостатності у хворих на цукровий діабет 2-го типу
Авторы: Кулаєць Н.М.
Івано-Франківський національний медичний університет, м. Івано-Франківськ, Україна
Рубрики: Эндокринология
Разделы: Клинические исследования
Версия для печати
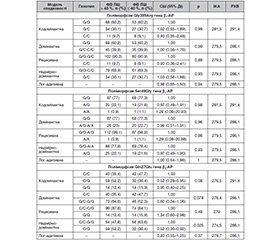
Актуальність. Серцева недостатність (СН) є найпоширенішою причиною госпіталізації та смерті хворих з патологією серцево-судинної системи. Відомо, що з перебігом СН, її прогресуванням пов’язані супутні захворювання і динаміка цілої низки біомаркерів, гормонів і генетичних чинників. Поліморфізми генів β1- і β2-адренорецепторів (β1- і β2-АР), імовірно, відіграють важливу роль у виникненні, прогресуванні СН і формуванні відповіді на терапію β-адреноблокаторами. Проведення комплексного аналізу може додати аргументів на користь причинно-наслідкового зв’язку поліморфізму і фенотипів захворювання. Це спонукає до проведення нових досліджень у цьому напрямку. Мета: вивчити взаємозв’язок поліморфізмів генів β1- і β2-адренорецепторів з ризиком розвитку серцевої недостатності. Матеріали та методи. Включено 201 хворого з СН на фоні післяінфарктного кардіосклерозу. Контрольна група — 43 здорових особи порівнянного віку і статі. Проводилось генотипування за трьома поліморфізмами (Gly389Arg гена β1-АР, Ser49Gly гена β1-АР, Gln27Glu гена β2-АР) за допомогою полімеразної ланцюгової реакції. Виконували ехокардіографію. Статистичний аналіз проводили за допомогою програм SPSS і SNPStats. Результати. Алель А (A/G-A/A) поліморфізму Ser49Gly гена β1-АР асоціюється зі зниженням ризику розвитку СН (СШ = 0,45 (0,23–0,91), р = 0,029, домінантна модель спадковості). Дані про зниження ризику СН за наявності алелі А поліморфізму Ser49Gly гена β1-АР підтверджуються й у кодомінантній (СШ = 0,43 (0,22–0,87), р = 0,048), надмірно-домінантній (СШ = 0,43 (0,21–0,86), р = 0,02) і на рівні тенденції — у лог-адитивній (СШ = 0,51 (0,27–0,99), р = 0,051) моделях спадковості. Під час проведення порівняльного аналізу розподілу алелей поліморфізму Ser49Gly (c.145A>G) гена β1-АР виявлено тенденцію до зменшення частоти алелі А у хворих із СН порівняно з групою контролю (11,9 %, проти 19,7 % відповідно; χ2 = 3,759; р = 0,053). Серед хворих із СН гетерозиготний генотип (G/A) зустрічався у 21,9 % проти 39,5 % у групі контролю (χ2 = 6,163; р = 0,046). Алель А (A/G-A/A) поліморфізму Ser49Gly гена β1-АР асоціюється зі зменшенням ризику зниження фракції викиду лівого шлуночка (ФВ ЛШ) ≤ 40 % (СШ = 0,43 (0,19–0,95), р = 0,048 у домінантній моделі та СШ = 0,42 (0,19–0,93), р = 0,033 у надмірно-домінантній моделі спадковості). Ризик зниження ФВ ЛШ у хворих із СН є нижчим у носіїв алелі G поліморфного локусу Gln27Glu гена β2-АР (СШ = 0,52 (0,30–0,92), р = 0,025). Висновки. Ризик розвитку серцевої недостатності та її фенотип асоціюється з генетичними відмінностями β-адренорецепторів. Алель А поліморфізму Ser49Gly гена β1-адренорецепторів асоціюється зі зниженням ризику розвитку серцевої недостатності (СШ = 0,45; р = 0,029, домінантна модель спадковості) і зниженням величини фракції викиду лівого шлуночка ≤ 40 % (СШ = 0,43; р = 0,048, домінантна модель). Ризик зниження фракції викиду лівого шлуночка у хворих із серцевою недостатністю є нижчим у носіїв алелі G поліморфного локусу Gln27Glu гена β2-адренорецепторів (СШ = 0,52, р = 0,025, надмірно-домінантна модель спадковості).
Background. Heart failure (HF) is the most common cause of hospitalization and mortality in patients with cardiovascular diseases. It is known that concomitant diseases and the dynamics of some biomarkers, hormones and genetic factors are associated with the course of HF and its progression. Gene polymorphisms of β1- and β2-adrenergic receptors (β1- and β2-AR) probably play an important role in the occurrence, progression of HF and the formation of response to therapy with β-adrenergic blockers. Conducting a comprehensive analysis can add arguments in favor of a cause-and-effect relationship between polymorphisms and disease phenotypes. This encourages new research in this direction. The purpose was to study the correlation between β1- and β2-adrenergic receptor gene polymorphisms and the risk of developing heart failure. Materials and methods. Two hundred and one patients with HF on the background of post-infarction cardiosclerosis were included. Control group consisted of 43 healthy persons of comparable age and sex. Genotyping was carried out for 3 polymorphisms (Gly389Arg of the β1-AR gene, Ser49Gly of the β1-AR gene, Gln27Glu of the β2-AR gene) using the polymerase chain reaction. Echocardiography was performed. Statistical analysis was done using SPSS and SNPStats programs. Results. The A allele (A/G-A/A) of the Ser49Gly polymorphism of the β1-AR gene is associated with a reduced risk of heart failure (odds ratio (OR) = 0.45 (0.23–0.91), p = 0.029, dominant model of inheritance). Data on a decreased risk of HF in the presence of the A allele of the Ser49Gly polymorphism of the β1-AR gene are also confirmed in codominant (OR = 0.43 (0.22–0.87), p = 0.048), overdominant (OR = 0.43 (0.21–0.86), p = 0.02) and log-additive (OR = 0.51 (0.27–0.99), p = 0.051) inheritance models. During a comparative analysis of the distribution of the Ser49Gly (c.145A>G) polymorphism alleles of the β1-AR gene, a tendency towards a decrease in the frequency of the A allele in patients with HF was revealed compared to the control group (11.9 against 19.7 %, respectively; χ2 = 3.759; p = 0.053). Among patients with HF, a heterozygous genotype (G/A) occurred in 21.9 % of cases against 39.5 % in the control group (χ2 = 6.163; p = 0.046). The A allele (A/G-A/A) of the Ser49Gly polymorphism of the β1-AR gene is associated with a decreased risk of reduced left ventricular ejection fraction ≤ 40 % (OR = 0.43 (0.19–0.95), p = 0.048 in the dominant model, and OR = 0.42 (0.19–0.93), p = 0.033 in the overdominant model of inheritance). The risk of a decrease in left ventricular ejection fraction among patients with HF is lower among carriers of the G allele of the Gln27Glu polymorphic locus of the β2-AR gene (OR = 0.52 (0.30–0.92), p = 0.025). Conclusions. The risk of developing heart failure and its phenotype are associated with genetic differences in β-adrenergic receptors. The A allele of the Ser49Gly polymorphism of the β1-adrenergic receptor gene is associated with a reduced risk of developing heart failure (OR = 0.45; p = 0.029, dominant model of inheritance), and a decrease in the left ventricular ejection fraction ≤ 40 % (OR = 0.43; p = 0.048 in the dominant model). The risk of reduced left ventricular ejection fraction in patients with heart failure is lower in carriers of the G allele of the Gln27Glu polymorphic locus of the β2-adrenergic receptor gene (OR = 0.52, p = 0.025, overdominant inheritance model).
цукровий діабет; β1-адренорецептори; β2-адренорецептори; серцева недостатність; поліморфізм; ген; фракція викиду лівого шлуночка
type 2 diabetes; β1-adrenergic receptors; β2-adrenergic receptors; heart failure; polymorphism; gene; left ventricular ejection fraction
Для ознакомления с полным содержанием статьи необходимо оформить подписку на журнал.
- Covolo L, Gelatti U, Metra M, Nodari S, Piccichè A, Pezzali N, Zani C, et al. Role of beta1- and beta2-adrenoceptor polymorphisms in heart failure: a case-control study. Eur Heart J. 2004 Sep;25(17):1534-41. doi: 10.1016/j.ehj.2004.06.015. PMID: 15342173.
- Dayem Ullah AZ, Lemoine NR, Chelala C. SNPnexus: a web server for functional annotation of novel and publicly known genetic variants (2012 update). Nucleic Acids Res. 2012 Jul;40(Web Server issue):W65-70. doi: 10.1093/nar/gks364. Epub 2012 Apr 28. PMID: 22544707; PMCID: PMC3394262.
- Dorn GW 2nd, Liggett SB. Mechanisms of pharmacogenomic effects of genetic variation within the cardiac adrenergic network in heart failure. Mol Pharmacol. 2009 Sep;76(3):466-80. doi: 10.1124/mol.109.056572. Epub 2009 Jun 2. PMID: 19491328; PMCID: PMC2730380.
- Kamyshna I, Pavlovych L, Pankiv I, Pankiv V, Kamyshnyi A. Eva–luation of the influence of single-nucleotide polymorphisms of vitamin D receptor (rs2228570), BDNF (rs6265), and NMDA (rs4880213) genes on gene expression in different tissues. International Journal of Endocrinology (Ukraine). 2023;19(2):83-88. https://doi.org/10.22141/2224-0721.19.2.2023.1250.
- Nechay O, Kvitka D, Lishchynsky P, Mazur O, Palamar–chuk V. Molecular genetic studies in the diagnosis of differentiated thyroid cancer: literature review. International Journal of Endocrino–logy (Ukraine). 2020;16(4):355-360. https://doi.org/10.22141/2224-0721.16.4.2020.208490.
- Jensen BC, O’Connell TD, Simpson PC. Alpha-1-adrenergic receptors in heart failure: the adaptive arm of the cardiac response to chronic catecholamine stimulation. J Cardiovasc Pharmacol. 2014 Apr;63(4):291-301. doi: 10.1097/FJC.0000000000000032. PMID: 24145181; PMCID: PMC3980029.
- Kaviarasan V, Mohammed V, Veerabathiran R. Genetic predisposition study of heart failure and its association with cardiomyopathy. Egypt Heart J. 2022 Jan 21;74(1):5. doi: 10.1186/s43044-022-00240-6. PMID: 35061126; PMCID: PMC8782994.
- Levin MC, Marullo S, Muntaner O, Andersson B, Magnusson Y. The myocardium-protective Gly-49 variant of the beta 1-adre–ner–gic receptor exhibits constitutive activity and increased desensitization and down-regulation. J Biol Chem. 2002 Aug 23;277(34):30429-35. doi: 10.1074/jbc.M200681200. Epub 2002 May 28; PMID: 12034720.
- Matkovich SJ, Van Booven DJ, Hindes A, Kang MY, Druley TE, Vallania FL, Mitra RD, et al. Cardiac signaling genes exhibit unexpected sequence diversity in sporadic cardiomyopathy, revealing HSPB7 polymorphisms associated with disease. J Clin Invest. 2010 Jan;120(1):280-9. doi: 10.1172/JCI39085. Epub 2009 Dec 14. PMID: 20038796; PMCID: PMC2798680.
- McDonagh TA, Metra M, Adamo M, Gardner RS, Baumbach A, Böhm M, Burri H, et al; ESC Scientific Document Group. 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart fai–lure. Eur Heart J. 2021 Sep 21;42(36):3599-3726. doi: 10.1093/eurheartj/ehab368. Erratum in: Eur Heart J. 2021 Oct 14; PMID: 34447992.
- Ponikowski P, Voors AA, Anker SD, Bueno H, Cleland JGF, Coats AJS, Falk V, et al; ESC Scientific Document Group. 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure: The Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC) Developed with the special contribution of the Heart Failure Association (HFA) of the ESC. Eur Heart J. 2016 Jul 14;37(27):2129-2200. doi: 10.1093/eurheartj/ehw128. Epub 2016 May 20. Erratum in: Eur Heart J. 2016 Dec 30; PMID: 27206819.
- Golkowski F, Krzentowska-Korek A, Baldys-Waligorska A, Hubalewska-Dydejczyk A. Goiter, cardiovascular and metabolic disorders in patients with acromegaly. Endocr Regul. 2011 Oct;45(4):191-7. doi: 10.4149/endo_2011_04_191; PMID: 22073948.
- Rathz DA, Gregory KN, Fang Y, Brown KM, Liggett SB. Hie–rarchy of polymorphic variation and desensitization permutations rela–tive to beta 1- and beta 2-adrenergic receptor signaling. J Biol Chem. 2003 Mar 21;278(12):10784-9. doi: 10.1074/jbc.M206054200. Epub 2003 Jan 13; PMID: 12525504.
- Sole X, Guino E, Valls J, Iniesta R, Moreno V. SNPStats: a web tool for the analysis of association studies Bioinformatics. 2006.22:1928-1929. doi: 10.1093/bioinformatics/btl268.
- Yuzhalin AE, Kutikhin AG. Integrative systems of genomic risk markers for cancer and other diseases: future of predictive medicine. Cancer Manag Res. 2012;4:131-5. doi: 10.2147/CMAR.S30855. Epub 2012 May 23. PMID: 22740773; PMCID: PMC3379855.
- Romeo FJ, Mavropoulos SA, Ishikawa K. Progress in Clini–cal Gene Therapy for Cardiac Disorders. Mol Diagn Ther. 2023 Mar;27(2):179-191. doi: 10.1007/s40291-022-00632-z. Epub 2023 Jan 15. Erratum in: Mol Diagn Ther. 2023 Jul;27(4):551-552. PMID: 36641770; PMCID: PMC10023344.
- Jordan E, Peterson L, Ai T, Asatryan B, Bronicki L, Brown E, Celeg–hin R, et al. Evidence-Based Assessment of Genes in Dilated Cardiomyopathy. Circulation. 2021 Jul 6;144(1):7-19. doi: 10.1161/CIRCULATIONAHA. 120.053033. Epub 2021 May 5. PMID: 33947203; PMCID: PMC8247549.
- Tada H, Fujino N, Hayashi K, Kawashiri MA, Takamura M. Human genetics and its impact on cardiovascular disease. J Cardiol. 2022 Feb;79(2):233-239. doi: 10.1016/j.jjcc.2021.09.005. Epub 2021 Oct 20. PMID: 34551866.