Перед розглядом основної теми цієї роботи слід нагадати деякі положення, що є ключовими для розуміння мети та завдань клініциста щодо курації таких пацієнтів. Хірургія фармакорезистентної епілепсії не є рутинною в Україні, але з кожним роком збільшується кількість оперативних втручань за показанням «фармакорезистентність епілепсії». За період 2014–2018 років 320 пацієнтів отримали хірургічне лікування епілепсії, за 2019 рік — 109 пацієнтів. Тобто кількість таких хворих зростає, а досвіду їх курації після завершення всіх процедур нейрохірургічного лікування немає.
Фармакорезистентна епілепсія — це невдача адекватного лікування двома переносимими, відповідно обраними і використаними лікарськими засобами. Водночас може йтися лише про адекватні препарати або їх комбінації в адекватних дозах. При цьому успішним лікування вважається тоді, коли повністю припиняються напади впродовж одного року або трикратного найдовшого міжнападного інтервалу під час активної фази епілепсії [1–3]. Тобто коли ми скеровуємо пацієнта на хірургічне лікування, ми бажаємо досягти в нашій клінічній практиці ступеня успішного лікування для конкретного пацієнта, і, як буде зрозуміло пізніше, дуже важливим є саме розуміння цих часових інтервалів.
Безумовно, вкрай важливим є стійке розуміння клініцистами того, що фармакорезистентна епілепсія є показанням для нейрохірургічного втручання, а для цього є необхідним адекватне розуміння визначення фармакорезистентності при скеруванні на хірургічне лікування. Але, на нашу думку, ще важливішим є чітке розуміння того, що метою хірургічного лікування хворих із фармакорезистентною епілепсією є саме подолання фармакорезистентності, а не повне одужання відразу після виписки з нейрохірургічного стаціонару.
Питання менеджменту хворих, які були прооперовані з приводу фармакорезистентності, не є розробленим не тільки в Україні, а й у всьому світі. Але такі хворі існують, їх кількість зростає, і неврологам, які їх спостерігають, потрібно розуміння цього процесу.
На сьогодні недостатньо доказової бази для обґрунтування раціональних рекомендацій щодо тактики післяхірургічного медикаментозного лікування. Тому дані щодо лікування після оперативного втручання дуже неоднорідні та часто суперечать одне одному. Є досить багато робіт, що аналізують терапію протиепілептичними препаратами (ПЕП) після хірургічного втручання або віддалені результати такого втручання [4].
З огляду на те, що значна частка пацієнтів досягає контролю нападів після резекційного хірургічного лікування, аспекти післяопераційного фармакологічного лікування є вкрай важливими. При аналізі літературних джерел за останні 30 років з цього питання було виявлено тільки одне, яке містило главу, спеціально присвячену проблемі фармакологічного лікування хірургічного пацієнта після оперативного лікування [5]. Автори дали дуже розумні рекомендації, засновані на їх враженнях і досвіді. Вони рекомендували монотерапію, коли це було можливо, і обговорювали можливість того, що деякі пацієнти в кінцевому підсумку стануть вільними від ліків. Незважаючи на те, що з моменту написання цієї роботи минуло багато років, сьогодні, як і тоді, бракує літератури та доказів у цій галузі, і вона потребує добре розроблених доказових досліджень.
У кількох спостережних дослідженнях розглядалося фармакологічне лікування пацієнтів до і відразу після операції, а також зміни медикаментозного лікування з плином часу після операції. У багатоцентровому дослідженні було показано, що перед операцією приблизно одна чверть пацієнтів приймала один препарат, близько половини — два, а ще чверть — три і більше ПЕП. При виписці, відразу після операції, 31 % пацієнтів приймали один, 57 % — два і 12 % — три або більше ПЕП. В інших дослідженнях наводяться дані про значні зміни у прийомі ПЕП до і після оперативного лікування: лише одна чверть пацієнтів отримувала монотерапію до операції проти 55 % після операції, і ще 9 % не приймали ПЕП [6–8].
Wieser та Häne у 2003 р. вивчали терапію ПЕП у великій когорті відібраних пацієнтів з амігдалогіпокампектомією від доопераційного періоду до 15 років після операції. До операції менше 40 % пацієнтів отримували монотерапію, приблизно 35 % — два ПЕП, а решта, приблизно 25 %, — три і більше ПЕП. Через 5 років після операції приблизно 35 % пацієнтів зовсім не прий-мали ПЕП, ще 35 % отримували монотерапію, близько 20 % приймали два препарати, і тільки 10 % приймали три або більше препарати [9].
Всі ці дослідження відображають дуже схожі дані. До операції лікарське навантаження було високим і значною мірою порівнянним серед пацієнтів, які брали участь у цих дослідженнях. Всі дослідження показали значне скорочення використання медикаментів після операції, причому значна частка пацієнтів в кінцевому підсумку припинила прийом всіх ліків. Яким чином ці скорочення відповідають клінічній ситуації або впливають на клінічну картину епілепсії, з цих досліджень залишається неясним. Також слід відзначити, що ці дослідження не можуть бути настановою у клінічній практиці і залишають питання алгоритму лікування таких хворих відкритим.
Значна частка пацієнтів після хірургічного лікування мають довготривалі ремісії з контролем нападів, але також значна частка може мати подальші рецидиви. Тема розвитку рецидивів після тривалої ремісії, що настала внаслідок оперативного втручання, висвітлена недостатньо, але вдалося знайти декілька доказових досліджень із цього питання.
Найбільш значна та вірогідна інформація про ремісії та рецидиви епілепсії після проведеної амігдалогіпокампектомії наведена Wieser et al. (2003) і стала важливою складовою підґрунтя для рекомендацій Міжнародної ліги з боротьби з епілепсією (ILAE) щодо класифікації результатів хірургічного лікування епілепсії (2004) [10–12].
Протягом року відразу після операції приблизно у 55 % пацієнтів повністю були відсутні напади й аура, що безумовно та обґрунтовано враховувалося як найкращій можливий результат. Протягом наступних кількох років у цій групі найкращих результатів відбувались рецидиви, і до 10 років після операції тільки близько 35 % все ще перебували в цій категорії і мали повний контроль нападів. Таким чином, приблизно у двох третин із тих, хто мав найкращий результат відразу після операції, стався рецидив.
Через 10 років після операції приблизно 55 % пацієнтів мали ремісію, однак це були не ті ж 55 %, у яких почалася ремісія відразу після операції.
В дослідженні H.H. Yoon et al. (2003) ретроспективно вивчалися результати лікування 175 пацієнтів, у яких були повністю відсутні напади протягом року відразу після операції. Всі пацієнти перебували під наглядом мінімум 3 роки (медіана — 8 років). Ризик рецидиву становив 17, 28 і 44 % через 3, 5 і 10 років після операції відповідно. Із 65 осіб, у яких стався рецидив, в 9 (13 %) це трапилося після того, як вони повністю припинили прийом всіх ліків, а в 33 (51 %) — після зниження дози або кількості прийнятих ПЕП [13].
Результати вивчення австралійської когорти вказують на значний ризик пізнього рецидиву в пацієнтів, які відразу ж після операції були вільні від нападів протягом принаймні 2 років, що становить приблизно половину когорти. У цій групі зі спочатку хорошим результатом приблизно в однієї четвертої пацієнтів рецидив настав більш ніж через 2 роки після операції [14].
Розглянуті дослідження мали ретроспективний характер. S.S. Spencer et al. провели проспективне багатоцентрове дослідження. Було виявлено, що рецидиви після однорічної ремісії трапляються приблизно у однієї третини пацієнтів. Навіть після дворічної ремісії рецидиви виникали в однієї четвертої пацієнтів. Майже половина рецидивів відбувалася у зв’язку зі зменшенням або припиненням прийому ПЕП [15].
Тобто слід відзначити, що саме зміна схеми ПЕП є фактором, який призводить до зриву компенсації епілепсії, що була досягнута внаслідок хірургічного лікування. Для розуміння терапевтичної тактики в пацієнтів після хірургічного втручання ми вважаємо за доцільне розглянути різні класифікаційні аспекти результатів хірургічного лікування щодо епілептичних нападів саме з позиції оцінки рівня ремісії у хворого, що дасть змогу розробити рекомендації щодо медикаментозного лікування.
Є дві загальновживані класифікації результатів хірургічного лікування епілепсії. Це класифікація ILAE [10] (табл. 1) та класифікація, яку раніше запропонував J. Engel Jr [16].
Класифікація післяопераційних результатів J. Engel Jr:
Клас I. Без інвалідизуючих нападів (відсутність нападів або тільки аури).
А. Повністю вільний від нападів після операції.
B. Тільки неінвалідизуючі прості парціальні напади після операції.
С. Наявність рідких інвалідизуючих нападів після операції, але відсутність таких нападів протягом не менше 2 років.
D. Генералізовані судомні напади тільки при припиненні прийому ПЕП.
Клас II. Вкрай рідкі інвалідизуючі напади (майже без нападів).
A. Спочатку вільний від інвалідизуючих нападів, але тепер має дуже рідкі напади.
В. Рідкі інвалідизуючі напади зразу після операції.
С. Поодинокі інвалідизуючі напади після операції та рідкі судомні напади протягом останніх 2 років.
D. Тільки нічні напади.
Клас III. Незначне поліпшення (незначне або помірне зменшення частоти нападів).
A. Помірне зменшення частоти нападів.
B. Зменшення інтервалів між нападами щонайменше у два рази протягом не менше 2 років.
Клас IV. Відсутність покращення (збереження нападів або збільшення частоти нападів).
A. Деяке значуще скорочення частоти нападів.
B. Ніяких значущих змін.
С. Частота нападів та/або тяжкість нападів зросла.
Незважаючи на те, що ці класифікації мають дуже багато рубрик, що свідчать про покращення стану хворих і можливе покращення якості їх життя, вільними від нападів (контроль нападів) можна вважати лише тих хворих, стан яких відповідає кваліфікаційному пункту 1 згідно з класифікацією ILAE або ІА згідно з класифікацією Engel, і тільки тих, які відповідають цим критеріям протягом не менше одного року. Це розуміння є дуже важливим для подальшого вибору терапевтичної тактики. Безумовно, багато інших пунктів свідчать про покращення стану пацієнтів та можуть бути розцінені як показники успішності хірургічного лікування, але тільки вищезазначений пункт відповідає критерію успішності лікування, що пропонує ILAE. Таким чином, пацієнти, які мають наслідки оперативного лікування, що відповідають пункту 1 згідно з класифікацією ILAE або ІА згідно з класифікацією Engel, можуть вважатися хворими, які досягли ремісії та, відповідно, потребують підходів, що визначені для хворих з контролем нападів, всі інші мають розглядатися як пацієнти, які мають ту чи іншу динаміку епілепсії (зазвичай позитивну), але не мають контролю нападів, і згідно з цим мають бути визначені відповідні особливості їх курації.
Зазвичай після успішного оперативного втручання постає питання про зниження дози ПЕП. Перед обговоренням такої можливості та наслідків такого кроку слід зупинитися на постулаті про мету оперативного втручання, а метою є саме подолання резистентності епілептичного процесу до терапії ПЕП, тобто наслідком оперативного лікування має бути успішне медикаментозне лікування епілепсії, а не відміна або значне скорочення об’єму терапії.
Корисно розрізняти два різних, хоча і пов’язаних між собою питання:
а) чи є скорочення доз та кількості ПЕП зразу після оперативного лікування раціональним та безпечним;
б) чи можливо зменшити і в кінцевому рахунку відмінити ПЕП у пацієнтів, які довготривало не мають епілептичних нападів; які є ризики і які фактори впливають на ці ризики?
Ми маємо результати клінічних досліджень, що стосуються цих питань.
R. Kuzniecky et al. (1992) провели рандомізоване клінічне дослідження, що порівнювало пацієнтів зі скроневою лобектомією, рандомізованих на монотерапію, з пацієнтами з політерапією після операції, і не виявили жодних доказів того, що політерапія забезпечує кращий контроль нападів, ніж монотерапія, у цій конкретній ситуації. Пацієнти, які отримували політерапію, мали більше побічних ефектів, ніж ті, які отримували монотерапію. Слід відзначити явні недоліки цього дослідження — невключення пацієнтів із тривалою відсутністю нападів і недостатнє урахування схеми ПЕП до операції [17].
Дані про ризики, пов’язані з припиненням або зменшенням дозування ПЕП у післяопераційних пацієнтів без нападів, також обмежені. В метааналізі, що провели D. Schmidt et al. (2004), проаналізовані результати 6 досліджень; ризик рецидиву становив приблизно одну третину після припинення прийому ПЕП [18]. Всі дослідження були ретроспективними. Наймасштабніше із цих досліджень довело, що 7 % пацієнтів, які не мали ніяких змін в прийомі ПЕП, мали рецидиви нападів порівняно з 26 % тих, які повністю припинили прийом ПЕП, і 14 % тих, які мали рецидив внаслідок зменшення дозування ПЕП [19].
В дослідженні, що було проведене А.М. McIntosh et al. (2005), показано, що в пацієнтів, які були вільними від нападів протягом 2 років і після цього, відбувалося контрольоване лікарем припинення прийому ПЕП, частота рецидивів була практично такою ж, як і в тих, які продовжували приймати ПЕП [14].
Слід відзначити, що результати цих та інших досліджень не дають змоги надати чіткі рекомендації щодо зміни схеми прийому ПЕП після оперативного втручання, і їх дані треба інтерпретувати з великою обережністю [20, 21].
Порівняння хворих після оперативного лікування, які мали стійку ремісію після хірургічного втручання, а потім рецидив внаслідок зниження дозування або повного припинення терапії ПЕП, з хворими з добре контрольованою епілепсією без хірургічного лікування, які мали рецидив після припинення прийому ПЕП, виявило майже однакові і дуже високі шанси на довготривалу ремісію після відновлення прийому ПЕП [22, 23], що підтверджує тезу, що оперативне втручання саме долає резистентність.
Клінічна та соціальна ситуація для пацієнтів, які були прооперовані та мають стійку ремісію, практично така ж сама, як і в осіб, які мають стійкий контроль нападів внаслідок успішного лікування ПЕП без оперативного втручання. В обох випадках немає чітких рекомендацій щодо зменшення дозування або відміни препаратів. Безумовно, рішення має прийматися з урахуванням можливості розвитку рецидиву, клінічних і соціальних наслідків рецидиву, терапевтичної (можливо, ще й соціальної) тактики в разі настання рецидиву, наявності можливих предикторів рецидиву і ще багатьох факторів, індивідуальних для пацієнта.
Для розуміння підходів до зниження та припинення ПЕП необхідне проведення обсерваційних досліджень з дизайнами, що можуть бути співставлені. Такі дослідження також повинні розглядати ризик рецидиву після припинення прийому ліків, а також виявити пре-диктори рецидиву. З огляду на поширення хірургічного лікування епілепсії може знадобитися великомасштабне рандомізоване клінічне дослідження, щоб забезпечити надійні докази, на яких можна було б засновувати загальні та індивідуальні рекомендації щодо зниження та відміни ПЕП у вільних від нападів післяопераційних пацієнтів. На сьогодні, на жаль, ми не маємо таких досліджень.
Таким чином, можна з впевненістю стверджувати, що немає достатньої доказової бази, яка б дозволила розробити специфічні рекомендації щодо медикаментозного лікування хворих на епілепсію після оперативного втручання з приводу фармакорезистентності. На нашу думку, найбільш доцільним є використання терапевтичних підходів, що розроблені взагалі для хворих на епілепсію. Казати про досягнуту внаслідок хірургічного лікування ремісію можна тільки через рік після оперативного втручання (ILAE — не менше року), при цьому слід відзначити, що майже в усіх клінічних випадках оцінити успішність хірургічного лікування можна раніше. Протягом цього року зміна схеми ПЕП недоцільна при контролі нападів, за винятком таких клінічних ситуацій: прийом більше 3 ПЕП, наявність побічних дій ПЕП, що погіршують якість життя пацієнта. Але слід відзначити, що ці клінічні ситуації є підставою для корекції схеми прийому ПЕП і в пацієнтів, які не отримували хірургічного лікування. Через рік повного контролю нападів тактика має бути така ж сама, як і в пацієнтів зі стійкою ремісією, але у випадках політерапії можливо переглянути питання про зниження дозування одного з ПЕП з можливою його відміною раніше у хворого, який не був оперований, оскільки ми маємо розглядати такого пацієнта як такого, який не має фармакорезистентності.
При появі епілептичних нападів відразу після оперативного втручання не слід змінювати схему прийому ПЕП. Слід дочекатися повного загоєння, закінчення формування післяопераційних змін у головному мозку, і тільки тоді оцінювати ефективність хірургічного лікування і вибору терапевтичної тактики відповідно до ступеня ефективності.
Якщо пацієнт має напади, навіть якщо вони стали значно рідшими, або тільки нетяжкі фокальні напади, які розцінюються як аури, в деяких випадках доцільно переглянути схему лікування для досягнення повного контролю нападів, що може бути можливим, оскільки пацієнт був прооперований і вже може не бути фармакорезистентним.
Тобто якщо пацієнт має напади, які стали більш рідкими, відзначена їх позитивна трансформація, стан пацієнта покращився, лікар повинен обговорити з ним можливість корекції схеми терапії ПЕП, яка у даному випадку є необов’язковою, але бажаною, оскільки є шанс звільнити пацієнта від нападів. Якщо після оперативного втручання стан пацієнта не змінився або погіршився, слід розглянути питання про наявність у хворого неепілептичних нападів, питання комплаєнтності пацієнта та всі питання, що мають бути розглянуті у фармакорезистентного пацієнта з епілепсією, який не має показань до хірургічного лікування.
Але у клінічних випадках, коли пацієнт має стійку ремісію епілепсії внаслідок хірургічного лікування, перед клініцистом постає питання зниження дозування ПЕП з подальшою можливою відміною. На наш погляд, вирішення цього питання у хворих, які досягли компенсації захворювання внаслідок хірургічного втручання, не має відрізнятися від аналогічного клінічного завдання в пацієнтів, які досягли компенсації завдяки застосуванню ПЕП.
Питання відміни ПЕП є вкрай складним клінічним завданням, яке можливо вирішувати тільки у високо-спеціалізованому закладі. Перед прийняттям рішення про можливу відміну ПЕП треба обстежити хворого з обов’язковим довготривалим ЕЕГ-дослідженням (краще провести відео-ЕЕГ-моніторинг не менш ніж 24 години), також доцільним є повтор МРТ-дослідження з використанням апарату з максимальними діагностичними можливостями.
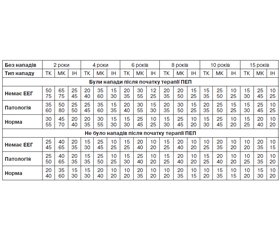
При оцінці можливості рецидиву, крім даних ЕЕГ та МРТ, слід враховувати кількість ПЕП, що приймає пацієнт, тривалість ремісії, тип нападу та наявність нападів після призначення ПЕП. Імовірність поновлення нападів наведена в табл. 2 та 3 за даними рекомендацій NICE (Великобританія, 2020) [24]. Перед вирішенням питання про відміну прийому ПЕП лікар має оцінити ризики появи нападів, а також обговорити з пацієнтом та/або його представниками таку ймовірність і потім вже сумісно приймати рішення про відміну ПЕП. На нашу думку, є неприпустимим самостійне вирішення лікарем цього питання (наприклад, «ви не маєте нападів протягом 3 років, будемо відміняти ПЕП…» або щось подібне). Якщо дорослий пацієнт має довготривалу ремісію, з ним необхідно провести відповідну бесіду про ризики зниження дозування та можливої відміни ПЕП, якщо дитина — то з дитиною та її батьками. При цьому крім даних, наведених в табл. 2 та 3, слід враховувати, що збіг морфологічного та епілептогенного вогнищ ставить під сумнів можливість і доцільність відміни ПЕП у пацієнта.
/38.jpg)
Тривалість ремісії повинна становити не менше 2 років, але, на нашу думку, питання зниження дози ПЕП для його подальшої відміни доцільно ставити через 3–5 років контролю нападів і лише за відсутності інших симптомів епілепсії. При цьому слід зазначити, що ні рекомендації ILAE, ні жодні національні рекомендації не мають чітких показань для відміни ПЕП, а також алгоритму такої відміни. Зменшення дози та відміну ПЕП слід проводити під контролем ЕЕГ-дослідження. У випадку погіршення показників при ЕЕГ-дослідженні в процесі відміни лікування її необхідно призупинити.
З пацієнтом обов’язково узгоджуєтеся план, згідно з яким у разі рецидиву нападів слід скасувати останнє зниження дози та звернутися за медичною допомогою. При відновленні нападів вже після відміни ПЕП необхідно відновити лікування — призначити ті ж самі дози, які пацієнт приймав до відміни, але слід бути готовим до того, що не у всіх клінічних випадках така терапевтична тактика буде ефективною, тобто може знадобитися подальший підбір схеми прийому ПЕП.
Підбиваючи підсумки, слід зазначити, що, на жаль, немає чітких протоколів для лікування ПЕП пацієнтів з епілепсією, які були прооперовані за показанням «фармакорезистентність». З огляду на те, що внаслідок хірургічного лікування фармакорезистентність має бути подолана, подальше медикаментозне лікування має проводитися так само, як і у хворих без фармакорезистентної епілепсії. Кількість і дозування ПЕП у цих хворих можуть бути більшими за потрібні, тому можливо ставити питання про зменшення дозування раніше, але після впевненості в успішності лікування (через 1 рік, згідно з наявним положенням). Якщо після оперативного лікування залишаються напади, навіть на тлі значного покращення, можлива корекція схеми ПЕП відповідно до загальноприйнятих рекомендацій. Відміна ПЕП у таких хворих має відбуватися за участю фахівця-епілептолога і потребує виконання всіх вимог п. 1.9.18 адаптованої клінічної настанови «Епілепсія» [25], але потребує ще більшої обережності, оскільки ці пацієнти вже мали фармакорезистентність.
Питання менеджменту хворих на епілепсію, які отримали хірургічне лікування у зв’язку з фармакорезистентністю, потребує подальшої розробки, особливо в умовах збільшення кількості таких хворих.
Всі питання та положення, що були викладені вище, мають дискусійний характер і можуть бути кореговані залежно від клінічної ситуації.
Конфлікт інтересів. Не заявлений.
Отримано/Received 05.02.2021
Рецензовано/Revised 22.02.2021
Прийнято до друку/Accepted 02.03.2021
Список литературы
1. URL: https://dec.gov.ua/wp-content/uploads/images/dodatki/2014_276_Epilepsii/2014_276_YKPMD_epilepsiya_dorosli.pdf (дата звернення: 20.03.2021).
2. URL: https://onlinelibrary.wiley.com/doi/full/10.1111/j.1528-1167.2009.02397.x (дата звернення: 20.03.2021).
3. URL: https://www.ilae.org/guidelines/definition-and-classification/definition-of-epilepsy-2014 (дата звернення: 20.03.2021).
4. McIntosh A.M., Wilson S.J., Berkovic S.F. Seizure outcome after temporal lobectomy: current research practice and findings. Epilepsia. 2001. № 42. Р. 1288-1307.
5. Andermann F., Bourgeois B.F., Leppik I.E., Ojemann L.M., Sherwin A.L. Postoperative pharmacotherapy and discontinuation of antiepileptic drugs. In: Engel J., ed. Surgical treatment of the epilepsies. New York: Raven Press, 1993. Р. 679-684.
6. Bien C.G., Kurthern M., Baron K., Lux S., Helmstaedter C., Schramm J., Elger C.E. Long-term outcome and antiepileptic drug treatment in surgically controlled temporal lobe epilepsy patients: a controlled study. Epilepsia. 2001. № 42. Р. 1416-1421.
7. Mathern G., Giza C.C., Yudovin S., Vinters H.V., Peacock W.J., Shewmon D.A., Shields W.D. Postoperative seizure control and antiepileptic drug use in pediatric epilepsy surgery patients: the UCLA experience, 1986–1997. Epilepsia. 1999. № 40. Р. 1740-1749.
8. Wieser H.G., Ortega M., Friedman A., Yonekawa Y. Long-term seizure outcome following amygdalohippocampectomy. J. Neurosurg. 2003. № 98. Р. 751-763.
9. Wieser H.G., Häne A. Antiepileptic drug treatment before and after selective amygdalohippocampectomy. Epilepsy Res. 2003. № 55. Р. 211-223.
10. Wieser H.G., Blume W.T., Fish D. Proposal for a New Classification of Outcome with Respect to Epileptic Seizures Following Epilepsy Surgery. Epilepsia. 2001. № 42(2). Р. 282-286.
11. URL: https://www.ilae.org/files/dmfile/Epigraph-2016-2_Snead-4-full-report-epil-surg.pdf (дата звернення: 20.03.2021).
12. Rosenov F., Bast T., Czech T., Feucht M. et al. Revised version of quality guidelines for presurgical epilepsy evaluation and surgical epilepsy therapy issued by the Austrian, German, and Swiss working group on presurgical epilepsy diagnosis and operative epilepsy treatment. Epilepsia. 2016. Vol. 57. Issue 8. Р. 1215-1220.
13. Yoon H.H., Kwon H.L., Mattson R.H., Spencer D.D., Spencer S.S. Long-term seizure outcome in patients initially seizure-free after resective epilepsy surgery. Neurology. 2003. № 61(4). P. 67-73.
14. McIntosh A.M., Kalnins R.M., Mitchell R.A., Fabinyi G.C.A., Briellmann R.S., Berkovic S.F. Temporal lobectomy: long-term seizure outcome, late recurrence and risks for seizure recurrence. Brain. 2004 Sept. Vol. 127. Issue 9. P. 2018-2030.
15. Spencer S.S., Berg A.T., Vickrey B.G., Sperling M.R., Bazil C.W., Shinnar S., Langfitt J.T., Walczak T.S., Pacia S.V., Fro-bish D. Predicting seizure outcome of anteromedial temporal lobectomy: the multicenter study of epilepsy surgery. Epilepsia. 2003. № 44(suppl. 9). Р. 337-338.
16. Engel J. Jr, Van Ness P.C., Rasmussen T.B., Ojemann L.M. Outcome with respect to epileptic seizures. In: Engel J. Jr, ed. Surgical treatment of the epilepsies. New York: Raven Press, 1993. Р. 609-21.
17. Kuzniecky R., Rubin Z.K., Faught E., Morawetz R. Antiepileptic drug treatment after temporal lobe epilepsy surgery: a rando-mized study comparing carbamazepine and polytherapy. Epilepsia. 1992. № 33. Р. 908-912.
18. Schmidt D., Baumgartner C., Loscher W. Seizure recurrences after planned discontinuation of antiepileptic drugs in seizure-free patients following epilepsy surgery: a review of current clinical experience. Epilepsia. 2004. № 45. Р. 179-186.
19. Schiller Y., Cascino G.D., So E.L., Marsh W.R. Discontinuation of antiepileptic drugs after successful epilepsy surgery. Neurology. 2000. № 54. Р. 346-349.
20. Sackett D.L. Bias in analytic research. J. Chron. Dis. 1979. № 32. Р. 51-63.
21. Anne T. Berg Postsurgical Treatment of Epilepsy. Epilepsy Curr. 2004 Jul. № 4(4). Р. 127-130.
22. Schmidt D., Baumgartner C., Loscher W. Seizure recurrences after planned discontinuation of antiepileptic drugs in seizure-free patients following epilepsy surgery: a review of current clinical experience. Epilepsia. 2004. № 45. Р. 179-186.
23. Chadwick D. Drug withdrawal and epilepsy: when and how? Drugs. 1988. № 35. Р. 579-583.
24. URL: https://www.nice.org.uk/guidance/cg137/chapter/Introduction#pharmacological-treatment (дата звернення: 20.03.2021).
25. URL: https://dec.gov.ua/wp-content/uploads/images/dodatki/2014_276_Epilepsii/2014_276_AKN_epilepsiya.pdf (дата звернення: 20.03.2021).UA-LEVI-PUB-042021-065

/37.jpg)
/38.jpg)