Вступ
Медична практика за останні кілька місяців змінилася більше, ніж за останні кілька десятиліть. Це сталося через пандемію коронавірусної хвороби (COVID-19). COVID-19 поширилася принаймні в 124 країнах і територіях і стала глобальною загрозою здоров’ю. З огляду на ситуацію, що склалася, розуміння вірусу, його епідеміології, передачі й значення для офтальмології постійно розвивається. Причиною COVID-19 є недавно виявлений вірус, названий коронавірусом тяжкого гострого респіраторного синдрому (SARS-CoV-2). Коронавіруси стали відомими в суспільстві після спалаху коронавірусу тяжкого гострого респіраторного синдрому (SARS-CoV-1) у 2003 році й коронавірусу близькосхідного респіраторного синдрому (MERS-CoV) у 2012 році. Коронавіруси належать до підродини Coronavirinae в сімействі Coronaviridae ряду Nidovirales з чотирма відомими родами: Alphacoronavirus, Betacoronavirus, Gammacoronavirus і Deltacoronavirus. Назва коронавірусу є похідною від латинського слова corona, що описує характерну структуру виступів на поверхні вірусної оболонки, які надають йому вигляду корони. SARS-CoV-2 являє собою вірус з одинарною позитивною смисловою одноланцюговою РНК з геномом довжиною близько 30 т.п.н., що робить його найбільшим з відомих РНК-вірусів [5]. Показано, що послідовність SARS-CoV-2 на 75–80 % ідентична SARS-CoV-1 і на 40 % ідентична MERS-CoV.
SARS-CoV-2 і SARS-CoV-1 мають один і той же рецептор хазяїна — людський ангіотензинперетворюючий фермент (АПФ) 2 (ACE2), що є основною мішенню вірусу. На поверхні клітин епітелію дихальних шляхів і шлунково-кишкового тракту шипоподібний S-білок оболонки вірусу зв’язується з ACE2 з подальшим розвитком цитопатичних реакцій, що лежать в основі клінічних проявів COVID-19 або безсимптомного перебігу [9]. Клітини очної поверхні, включно з кон’юнктивою, можуть бути сприйнятливими щодо SARS-CoV-2 і служити вхідним порталом і резервуаром передачі вірусу від людини до людини. У всіх зразках, отриманих з очей посмертно, під час операцій або рефракційної хірургії, імуногістохімічно виявлена експресія ACE2 (рецептор SARS-CoV-2) і TMPRSS2 (фермент, що активує SARS-CoV-2) у кон’юнктиві, лімбі й рогівці, особливо в епітелії і substantia propria. Рецептор ACE2 широко експресується в багатьох органах, включно із сітківкою, що є продовженням центральної нервової системи. Рецептор ACE2 бере участь у патогенезі системних судинних захворювань, що викликають очні прояви, таких як діабетична й гіпертонічна ретинопатія [20].
Коронавіруси в цілому можуть викликати гетерогенні стани очей у тварин, такі як кон’юнктивіт, передній увеїт, ретиніт і неврит зорового нерва. Однак це відбувається за допомогою механізмів, які сильно відрізняються від тих, що в даний час спостерігаються в коронавірусів людини [1]. Очні симптоми у хворих з SARS-CoV-2 були найбільш тяжкими в пацієнтів з тяжкою пневмонією. Вірус був виявлений у 18 % пацієнтів, яким брали мазки з кон’юнктиви (2 з 11). У більшому ретроспективному дослідженні були зібрані дані про 1099 випадків захворювання за перші два місяці спалаху COVID-19 в Ухані, у результаті чого було виявлено, що «зацікавленість кон’юнктиви» була зареєстрована в 0,8 % пацієнтів [37]. Ретроспективні дослідження показують, що менше за 1 % пацієнтів страждають від кон’юнктивіту, пов’язаного з COVID-19. Однак проспективні дослідження показують, що цей показник є вищим і становить приблизно 6 %. Точна частота кон’юнктивіту в пацієнтів з COVID-19 досі не визначена й коливається від 0,8 до 31,6 % [9, 30, 34]. На думку D.M. Dockery і співавт. (2020), дані про ураженні очей при COVID-19 занижені, тому що лікарі швидкої допомоги й стаціонарів, як правило, не звертають увагу на очні симптоми, які на тлі загального стану пацієнта здаються незначними, і не фіксують їх. Вірусна РНК була виявлена в сльозах і секреті кон’юнктиви в пацієнтів з активним кон’юнктивітом, а також у безсимптомних випадках. У цілому мазки з кон’юнктиви позитивні в 2,5 % випадків. Зразки, взяті на ранній стадії захворювання, з більшою ймовірністю будуть позитивні щодо вірусу. Вищезазначені дослідження підтверджують, що SARS-CoV-2 може бути в сльозах або кон’юнктивальному мішку, але зараження SARS-CoV-2 через очі залишається невизначеним. Передача вірусу через тканини ока не підтверджена [39].
Механізм появи вірусу в сльозах залишається неясним, і питання про можливість передачі вірусу через інфіковану тканину ока або рідину залишається суперечливим. Одна з гіпотез полягає в тому, що носослізна система діє як канал, яким віруси переміщуються з верхніх дихальних шляхів в очі. Але є й інша точка зору. Епітелій кон’юнктиви піддається безпосередньому впливу зовнішнього середовища, що може включати аерозолі, які містять вірусні частки. Пряма інокуляція кон’юнктиви з інфікованих крапель призводить до деякої абсорбції рогівкою, кон’юнктивою і, в кінцевому підсумку, склерою, але більша частина стікає в носослізну систему, а слізний проток транспортує сльози до нижнього ходу носа або в носоглотку. Отже, очна тканина й рідина можуть являти собою потенційне джерело і шлях зараження COVID-19, хоча роль кон’юнктиви в передачі вірусу в даний час залишається неясною [3, 9]. Ще один теоретичний шлях, яким SARS-CoV-2 може проникати через тканини ока, — рецептори ACE2. SARS-CoV-2 вимагає доступу до клітин-хазяїв через рецептор ACE2. Рецептор ACE2 був ідентифікований на поверхні ока як частина локальної автокринної функції ренін-ангіотензинової системи. Крім того, рецептор ACE2 був виявлений у водянистій волозі й сітківці. Однак на сьогодні експресія ACE2 у таких тканинах, як кон’юнктива або рогівка, повністю не вивчена. Отже, незважаючи на підтверджену присутність рецепторів ACE2 у тканинах ока, не встановлено, чи забезпечує цей шлях реплікацію вірусу. На сьогодні недостатньо даних, що дозволяють визначити вплив системних інгібіторів АПФ на ризик зараження для пацієнтів [16, 33, 35].
Ознаки кон’юнктивіту COVID-19 аналогічні проявам інших вірусних форм. У пацієнтів зазвичай спостерігаються двостороння гіперемія кон’юнктиви, хемоз, фолікулярна реакція кон’юнктиви, епіфора, водянисті виділення, легкий набряк повік і збільшення передвушних і підщелепних лімфатичних вузлів. L. Chen і співавт. (2020) при обстеженні 534 пацієнтів з COVID-19 виявили кон’юнктивальну гіперемію в 4,7 %, у 12 % з них це була найбільш рання клінічна ознака. Гіперемія зберігалася протягом приблизно 5 днів і з інтервалом 2–10 днів асоціювалася із симптомами сухого ока (21 %), затуманенням зору (13 %) і відчуттям стороннього предмета (12 %). У більшості пацієнтів очні скарги поєднувалися з гарячкою і респіраторними симптомами, включно із сухим кашлем і задишкою. У літературі описаний тільки один випадок, коли монолатеральний кератокон’юнктивіт був відзначений як перший прояв COVID-19. В одного хворого були виявлені псевдодендрити в нижній частині рогівки, невеликі субепітеліальні інфільтрати й дефекти епітелію. Є роботи, що свідчать про незначне зниження чутливості рогівки у хворих на COVID-19. З огляду на вищенаведені факти у хворих часто виникають питання до офтальмологів. Д-р Анні Нгуєн, доцент клінічної офтальмології і помічник директора з рефракційної хірургії в очному інституті USC Roski, спробувала відповісти на найбільш поширені питання щодо того, чи вразливі наші очі для нового коронавірусу. Ось частина цих відповідей.
Якщо краплі COVID-19 потрапили вам в око, чи схильні ви до інфекції?
Докази окулярної передачі вивчені недостатньо. Однак слизові оболонки, що вистилають багато порожнин і органів тіла, включно з дихальними шляхами, найбільш сприйнятливі до нового коронавірусу й вірусів у цілому. Поверхня очей і внутрішня поверхня повік також вистелені слизовою оболонкою. Отже, якщо інфіковані краплі потрапляють вам в око, ви, можливо, сприйнятливі до інфекції. Вважається, що передача COVID-19 в основному відбувається через респіраторні краплі від людини до людини. Однак вірус також може жити на поверхні до декількох днів; тому дотик до інфікованої поверхні, а потім дотик до очей, носа або рота без миття рук може призвести до зараження.
Чи може промивання очей водою або безрецептурними краплями знизити ймовірність зараження?
Якщо з’являється подразнення очей, використання безрецептурних штучних сліз може допомогти полегшити ваші симптоми. Якщо симптоми не зникнуть, зверніться до офтальмолога.
Чи правда, що в користувачів контактних лінз більш високий ризик зараження COVID-19?
При дотриманні правил гігієни немає доказів того, що носіння контактних лінз саме по собі збільшує ризик зараження COVID-19. Однак люди, які носять контактні лінзи, торкаються очей частіше, ніж звичайні люди. Якщо ви схильні доторкатися до очей або терти їх, можливо, краще тимчасово перейти на окуляри через ризик передачі інфекції через тертя без належної гігієни рук. Крім того, окуляри мінімізують ризик подразнення від носіння контактних лінз, а також служать бар’єром, який змушує вас зупинитися, перш ніж доторкнутися до очей. Хоча це й не найкращий захист, окуляри також можуть служити частковим захистом від крапель з дихальних шляхів. Якщо ви продовжуєте носити контактні лінзи, ретельно дотримуйтесь правил гігієни й мийте руки. Якщо у вас з’явилося почервоніння або подразнення, припиніть носити контактні лінзи й зверніться до окуліста.
Передбачається, що, як і у випадку з іншими вірусними інфекціями, очні прояви COVID-19 минають самостійно й можуть контролюватися за допомогою симптоматичної терапії, що включає сльозозамінники. Перевагу слід віддати препаратам безконсервантним, що містять гіалуронову кислоту, а також біопротектор і осмопротектор (трегалозу). Усім цим параметрам відповідає Теалоз® Дуо (Laboratoires Thea). Застосовується по 1 краплі за необхідності. Іноді при приєднанні бактеріальної інфекції доводиться вдаватися до інстиляції крапель, що містять антибіотики. У даному аспекті загальним визнанням при застосуванні у хворих з COVID-19 користується азитроміцин. У вигляді очних крапель азитроміцин в Україні представлений препаратом Азитер® (Azyter®) з дуже зручною схемою застосування — всього по 1 краплі 2 рази на день 3 дні, і він випускається в унідозах без консервантів.
Висока ймовірність ураження заднього відрізка ока, і особливо сітківки, спонукала низку офтальмологів провести відповідні дослідження. Тим більше що рецептор ACE2 є не тільки мішенню для первинного впливу COVID-19, але й первинним ферментом вазопротекторної осі ренін-ангіотензинової системи. А діабетична ретинопатія пов’язана з порушенням балансу ретинальної осі «ренін — ангіотензин — альдостерон». Пригнічення ACE2 може відігравати важливу роль в індукції розвитку ішемії сітківки й навіть діяти як маркер ендотеліального захворювання.
Для того, щоб з’ясувати взаємини SARS-CoV2 і сітківки ока, були проведені дослідження в померлих пацієнтів з підтвердженим коронавірусним захворюванням (COVID-19). 14 очей 14 померлих пацієнтів з підтвердженим COVID-19 були енуклейовані при розтині. Була проведена ланцюгова реакція зворотної транскриптази-полімерази (ЗТ-ПЦР) у реальному часі для виявлення трьох різних вірусних послідовностей РНК (ген RdRp, ген E і ген Orf1) SARS-CoV-2. Результати: у трьох із 14 очей вірусна РНК SARS-CoV-2 була виявлена в сітківці померлих пацієнтів з COVID-19. Оскільки аналіз трьох різних послідовностей (ген RdRp, ген E і ген Orf1) показав позитивні результати в ЗТ-ПЦР, існування вірусної РНК SARS-CoV-2 у сітківці ока людини доведено відповідно до стандартів Всесвітньої організації охорони здоров’я [4].
Крім того, на підставі нещодавніх даних припускають, що COVID-19 може пов’язуватись зі змінами в імунній і коагуляційній системах і можливим поширенням вірусу через гематоенцефалічний бар’єр. Однак наслідки цих змін на оці, особливо щодо залучення заднього сегмента, повністю не з’ясовані [29]. Недавня стаття Zhang et al. передбачає, що провідним фактором патогенезу мікроциркулярного ураження в пацієнтів з COVID-19 є опосередкована комплементом тромботична мікроангіопатія. Описано, що активація системи комплементу безпосередньо відповідальна за пошкодження очних судин, з рідкісними випадками атипового гемолітико-уремічного синдрому, що призводить до оклюзії артерій і вен сітківки. Також варто враховувати, що високі рівні фактора комплементу С3 у сироватці також пов’язані з підвищеним ризиком розвитку діабетичної ретинопатії, нефропатії і нейропатії через ендотеліальну дисфункцію і тромбоз.
Імуногістохімічний аналіз, проведений на людському оці, показав, що циліарне тіло, судинна оболонка, сітківка і пігментний епітелій сітківки експресують значущі рівні рецепторів АПФ.
Оскільки COVID-19 здатний впливати на перицити судин, що експресують ACE2, вірусна інфекція може призводити до дисфункції ендотеліальних клітин, опосередкованої комплементом, пошкодження мікросудин і, отже, залучення очного кровообігу [38].
Коагулопатія, пов’язана з COVID-19, може сприяти цілій низці тромбоемболічних подій. Описано численні випадки тромбозу глибоких вен, тромбоемболії легеневої артерії і ішемічного інсульту великих судин у пацієнтів з COVID-19.
На даний час був опублікований тільки один випадок ізольованої оклюзії центральної артерії сітківки, вторинної щодо COVID-19, у той час як про підвищення частоти оклюзії вен сітківки не повідомлялося. Майбутні дослідження можуть виявити можливий вплив COVID-19 на судинну патологію сітківки й збільшення частоти оклюзій судин сітківки під час пандемії COVID-19 [12, 27, 32, 38].
Виходячи з цих передумов, логічно було припустити наявність ретинальних змін у хворих з COVID-19. Нещодавній звіт передбачає зміни сітківки, пов’язані з COVID-19. Серія випадків з 11 пацієнтів, яким було виконано оптичну когерентну томографію (ОКТ), продемонструвала, що в усіх пацієнтів спостерігалися гіперрефлективні ураження на рівні гангліозних клітин і внутрішніх плексиформних шарів, більш виражені в папіломакулярному пучку обох очей. Це не було пов’язано з будь-якою зоровою дисфункцією або змінами в ОКТ-ангіографії або комплексному аналізі гангліозних клітин. У чотирьох пацієнтів спостерігалися ватоподібні вогнища й мікрокрововиливи уздовж аркади сітківки (рис. 1). З 54 пацієнтів, включених в аналіз, 50 (92,5 %) мали зображення доброї якості на обох очах, у той час як чотири (7,5 %) оцінювалися на єдиному доступному оці. Крововиливи в сітківку були виявлені як мінімум в одному оці в п’яти пацієнтів (9,25 %), ватоподібні вогнища були виявлені в чотирьох пацієнтів (7,4 %), друзи спостерігалися в шести пацієнтів (11,1 %).
/37.jpg)
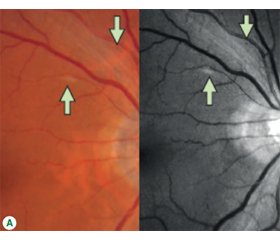
При огляді очного дна розширені вени спостерігались у 15 пацієнтів (27,7 %), звиті судини — у 7 пацієнтів (12,9 %) [19] (рис. 2). Середній діаметр артерій становив 98,3 ± 15,3 мкм у пацієнтів з COVID-19 і 91,9 ± 11,7 мкм у суб’єктів без вірусного ураження. При цьому різниця була статистично значущою (p = 0,006). Аналогічно середній діаметр вен був більшим у пацієнтів з COVID-19 (138,5 ± 21,5 мкм) порівняно зі здоровими суб’єктами (123,2 ± 13,0 мкм), і різниця була статистично значущою. Слід зазначити, що лікування, яке включає різні типи подачі кисню, а також системні препарати (антикоагулянти, антиагреганти, гідроксихлорохін, ремдесивір, лопінавір/ритонавір, тоцилізумаб, стероїди), не справило значного впливу на діаметр ретинальних артерій і вен. З огляду на вищесказане фармакологічна підтримка сітківки у хворих на COVID-19 буде корисна при легких і середніх формах цього захворювання. Згідно з результатами сучасних наукових досліджень і даними публікацій, саме нутрицевтики мають властивості, що покращують морфологічний і функціональний стан пігментного епітелію сітківки. Найбільш визнаними у світі нутрицевтичними компонентами, що застосовуються з цією метою, є антиоксиданти формули AREDS, каротиноїди, омега-3 жирні кислоти, ресвератрол, вітамін D. Ресвератрол і омега-3 жирні кислоти мають додаткові корисні судинні властивості — вони покращують тонус судин, реологію крові, знижують згортання й тромбоутворення, мають протиішемічну дію. Тому доцільне застосування Нутроф® Форте (Laboratoires Thea), що містить усі ці компоненти, для профілактики ретинальних порушень у хворих на COVID-19. Особливо важливе застосування цього препарату в людей старшої вікової групи.
/38.jpg)
У літературі описаний 67-річний пацієнт з хоріоретинітом, госпіталізований до відділення інтенсивної терапії з приводу COVID-19, у якого було відзначено помутніння склоподібного тіла й хоріоретинальне вогнище значних розмірів. Відповідно до стандартного протоколу була проведена етіологічна діагностика для виключення можливих патогенів, у тому числі SARS-CoV-2. Крім підтвердження SARS-CoV-2, був поставлений діагноз імовірного грибкового ретиніту, і до лікування була додана системна протигрибкова терапія з внутрішньовенним введенням амфотерицину. Незважаючи на тяжкий перебіг SARS-CoV-2, запальні зміни на сітківці поступово зменшувалися. Очікуваної активізації хоріоретиніту на тлі COVID-19 не виявлено.
Нейроофтальмологічні ускладнення
Неврологічні ускладнення COVID-19 включають поліневрит, синдром Гієна — Барре, менінгіт, енцефаломієліт і енцефалопатії. У літературі є повідомлення про пацієнтів, яким був поставлений діагноз COVID-19 після виявлення диплопії і офтальмопарезу, а також аномальних результатів магнітно-резонансної томографії периневральних або черепних нервів. Параліч окорухового нерва може бути викликаний прямою вірусною інвазією або запальними факторами, пов’язаними з вірусною інфекцією, або може бути вторинним щодо неврологічних ускладнень. Хоча експериментальні моделі припускають, що ураження очей можуть включати неврит зорового нерва, у літературі поки не повідомляється про підвищення частоти випадків ішемічної або запальної нейропатії зорового нерва, пов’язаної з COVID-19 [8].
Поширеність гострого респіраторного дистрес-синдрому (ГРДС) серед пацієнтів з COVID-19 становить 17 %. ГРДС — це небезпечний для життя стан, що вимагає респіраторної підтримки у відділенні інтенсивної терапії (ВІТ). У нещодавно опублікованому дослідженні 1591 пацієнта з COVID-19, госпіталізованого у відділення інтенсивної терапії регіону Ломбардія (Італія), показник госпіталізації становить 9 %, у той час як інші дослідження повідомляють про ще більш високі показники — до 32 %. Слід зазначити, що ті пацієнти, які потребують респіраторної підтримки у відділенні інтенсивної терапії, мають високу схильність до розвитку очних ускладнень. Частота очних ускладнень у пацієнтів у ВІТ у різних дослідженнях коливається від 3 до 60 %. Найбільш частими проявами є порушення очної поверхні, підвищення внутрішньоочного тиску (ВОТ), а також порушення переднього й заднього сегментів [18, 22, 28].
Пацієнти відділення інтенсивної терапії мають кілька факторів ризику поверхневих захворювань, деякі з яких пов’язані з лікуванням, а інші — із самим навколишнім середовищем у ВІТ. Наприклад, це вплив багатьох потенційно мультирезистентних бактерій. Дані про захворюваність на інфекційний кератит і кон’юнктивіт у пацієнтів на штучній вентиляції легенів відсутні. Проте дослідження 134 пацієнтів без раніше існуючих захворювань очної поверхні, яким проводилися седація і респіраторна підтримка, показує, що 77 % пацієнтів були колонізовані принаймні одним видом бактерій, відмінних від нормальної флори, і 40 % — декількома видами. Найбільш поширеними ізолятами були Pseudomonas aeruginosa, Acinetobacter spp. і Staphylococcus [22]. У пацієнтів з механічною вентиляцією легенів порушені основні захисні механізми очної поверхні. Міорелаксанти й седативні засоби зменшують тонічне скорочення orbicularis oculi, що призводить до лагофтальму. Крім того, вони пригнічують рефлекс моргання і феномен Белла, а також зменшують вироблення сльози. У результаті може розвинутися експозиційна кератопатія різного ступеня тяжкості [23]. Експозиційна кератопатія вражає до 42 % пацієнтів інтенсивної терапії і 60 % пацієнтів, які перебувають під седативною дією понад 48 годин. Крім прямого ушкодження, експозиційна кератопатія може також призвести до вторинних інфекцій, таких як кон’юнктивіт і кератит. На додаток до цього постійний тиск у дихальних шляхах і кисневі маски сушать поверхню ока. Сьогодні доведено, що неправильно підібрані маски Вентурі можуть викликати ерозії рогівки при терті очей [14, 15]. Хемоз кон’юнктиви зазвичай спостерігається в пацієнтів у відділенні інтенсивної терапії, і в особливо тяжких випадках він може сприяти розвитку лагофтальму й зниженню змащування поверхні ока. Фактори ризику розвитку хемозу кон’юнктиви включають зниження венозного відтоку з ока (через вентиляцію з позитивним тиском або щільну перев’язку ендотрахеальної трубки) і підвищення гідростатичного тиску (в основному через тривале лежання, особливо на животі). При лікуванні тяжкої форми COVID-19 доведено, що положення лежачи на животі знижує смертність у пацієнтів з ГРДС, і деякі автори рекомендують його мінімум 12 годин на день. Оскільки воно збільшує венозний тиск у голові, теоретично воно також може викликати субкон’юнктивальний крововилив — стан зазвичай абсолютно доброякісний, хоча він може привести до поверхневих порушень. У пацієнтів з механічною вентиляцією легенів позитивний тиск у кінці видиху може також привести до субкон’юнктивального крововиливу через підвищення внутрішньогрудного тиску і, як наслідок, центрального венозного тиску [11, 13]. Вентиляція в положенні лежачи на животі рідко може приводити до гострої ішемічної оптичної нейропатії, що викликає необоротну втрату зору. Відомо, що перфузія ока залежить від рівня очного кровообігу, який, у свою чергу, залежить від артеріального й венозного тиску, а також від судинного опору. Положення лежачи може істотно знизити перфузію ока, діючи з двох причин. З одного боку, це збільшує венозний тиск, а з іншого — збільшує ВОТ. ВОТ у положенні вниз головою може значно підвищуватися й досягати цифр 40 мм рт.ст. після 320 хвилин у положенні лежачи. Крім того, системні стани, такі як діабет, артеріальна гіпертензія і атеросклероз, можуть визначати підвищення судинного опору, тим самим додатково знижуючи очний кровотік. Звідси випливає, що пацієнти, які потрапляють у відділення інтенсивної терапії з приводу COVID-19 через супутні захворювання, також мають більш високий ризик розвитку гіпоперфузії очей [2, 6, 24].
Потенційно небезпечним для зору ускладненням у пацієнтів у ВІТ може бути офтальмогіпертензія і декомпенсація відкритокутової глаукоми, тому що ВОТ у положенні вниз головою може значно підвищуватися — до 40 мм рт.ст. після 320 хвилин. При визначенні в анамнезі глаукоми хворим необхідно продовжити інстиляції гіпотензивних крапель і проконтролювати виконання призначень. Для зниження внутрішньоочного тиску доцільно використовувати препарати, що дозволяють ефективно контролювати ВОТ протягом доби. Аналоги простагландину максимально й найбільш стабільно зменшують ВОТ протягом 24-годинного циклу. Як показали дослідження, простагландини забезпечують кращий 24-годинний контроль за всіма параметрами, за ними йдуть інгібітори карбоангідрази, потім альфа-агоністи і, нарешті, бета-блокатори. Латанопрост викликає значне збільшення перфузійного тиску ока в усіх 24-годинних тимчасових точках порівняно з вихідним рівнем. Латанопрост не дає системних ускладнень, його інстилюють всього 1 раз, що дуже зручно за даних клінічних умов. З урахуванням ураження очної поверхні, збільшення частоти і тяжкості сухого ока при COVID-19, слід віддавати перевагу безконсервантним препаратам. У цій ситуації викликає інтерес використання Монопрост — безконсервантної форми латанопросту, до складу якої входить карбомер з функцією зволоження. Особливо небезпечна глаукома з можливістю розвитку гострого нападу в положенні вниз головою. Ризик розвитку гострого нападу глаукоми може бути підсилений застосуванням системних препаратів, таких як холінолітики (атропін, іпратропію бромід, трициклічні антидепресанти й антигістамінні препарати), симпатоміметики (адреналін, норадреналін, дофамін, ефедрин, сальбутамол, тербуталін) та інші (похідні сульфонамідів і топірамат) [26, 31].
Ретинопатія Вальсальви — це стан, що характеризується раптовим початком односторонніх або двосторонніх макулярних преретинальних кровотеч у результаті розриву дрібних поверхневих капілярів через підвищений венозний тиск. Зазвичай це пов’язано з діяльністю, що викликає раптове підвищення внутрішньогрудного або внутрішньочеревного тиску. Повідомлялося, що ретинопатія Вальсальви також може виникати через інтубацію або високий позитивний тиск у кінці видиху [10, 17].
Інтенсивна терапія, і особливо інвазивна штучна вентиляція легенів, може бути пов’язана з декількома очними ускладненнями. Персонал інтенсивної терапії повинен знати про них і за необхідності направляти хворого до офтальмолога. Ускладнення, загрозливі щодо зору, зустрічаються рідко, але дуже важливо їх діагностувати й лікувати до того, як відбудеться необоротне погіршення. З іншого боку, порушення очної поверхні надзвичайно поширені, і кілька досліджень показали, що застосування належного протоколу може значно знизити їх частоту. Французька академія офтальмології (CNPО-AFO) і Французьке товариство офтальмології (SFO) опублікували рекомендації з догляду за очима пацієнтів з COVID-19 у стаціонарі. Перед перевертанням на живіт рекомендується закапати в обидва ока антисептик, наприклад піклоксидин. У нашому випадку препаратом вибору може стати азитроміцин Азитер® (Azyter®) з огляду на його широку антибактеріальну дію. Як сльозозамінник рекомендується безконсервантна пролонгована форма — Теалоз® Дуо, що містить як гіалуронову кислоту, так і біопротектор і осмопротектор трегалозу. Крім того, цей препарат має додаткову протизапальну дію і прискорює регенерацію. Після обробки ока при незмиканні повік рекомендується заклеїти повіки вертикальною смужкою гіпоалергенного пластиру. Слід уникати компресії очних яблук для профілактики гострої ішемічної оптиконейропатії. При повороті на спину необхідно зняти лейкопластир, рясно промити очі фізіологічним розчином з одноразового флакона й очистити повіки нетканою серветкою або одноразовою стерильною серветкою Блефаклін®, повторно закапати антисептик, сльозозамінник і при незмиканні повік знову заклеїти їх гіпоалергенним пластиром.
Висновки
— Пандемія коронавірусної хвороби (COVID-19) стала глобальною загрозою здоров’ю. Розуміння вірусу, його епідеміології, передачі й значення для офтальмології постійно розвивається.
— Точна частота кон’юнктивіту в пацієнтів з COVID-19 досі не з’ясована, вона коливається від 0,8 до 31,6 %. Однак дані про ураження очей при COVID-19 занижені, тому що лікарі швидкої допомоги і стаціонарів, як правило, не звертають увагу на очні симптоми, які на тлі загального стану пацієнта здаються незначними, і не фіксують їх.
— Дослідження підтверджують, що SARS-CoV-2 може бути в сльозах або кон’юнктивальному мішку, але зараження SARS-CoV-2 через очі залишається невизначеним. Передача вірусу через тканини ока не підтверджена.
— Клінічно в пацієнтів з COVID-19 виявляється кон’юнктивальна гіперемія в 4,7 %, у 12 % — це була найбільш рання клінічна ознака. Гіперемія зберігається у середньому протягом 5 днів (від 2 до 10 днів) і асоційована із симптомами сухого ока (21 %), затуманюванням зору (13 %) і відчуттям стороннього предмета (12 %). У більшості пацієнтів очні скарги поєднувалися з гарячкою і респіраторними симптомами.
— Лікування кон’юнктивіту проводиться за допомогою симптоматичної терапії, що включає гігієну повік (Блефаклін®), сльозозамінники. Перевагу слід віддати препаратам безконсервантним, що містять гіалуронову кислоту в комбінації з біопротектором і осмопротектором (Теалоз® Дуо).
— Серед топічних антибіотиків загальним визнанням при застосуванні у хворих з COVID-19 користується азитроміцин (Азитер®)
— Ретинальні зміни у хворих з COVID-19 включають, за даними ОКТ, наявність гіперрефлективних уражень на рівні гангліозних клітин і внутрішніх плексиформних шарів, більш виражені в папіломакулярному пучку обох очей. Офтальмоскопічно виявляються ватоподібні вогнища й мікрокрововиливи уздовж аркади сітківки.
— При легких і середніх формах цього захворювання буде корисна фармакологічна підтримка сітківки. Доцільне застосування Нутроф® Форте для профілактики ретинальних порушень у хворих на COVID-19. Особливо важливе застосування цього препарату в людей старшої вікової групи.
— Пацієнти з гострим респіраторним дистрес-синдромом мають високу схильність до розвитку очних ускладнень. Частота очних ускладнень у цих пацієнтів коливається від 3 до 60 %. Найбільш частими проявами є порушення очної поверхні, підвищення внутрішньоочного тиску.
— Персонал інтенсивної терапії повинен знати про очні ускладнення й за необхідності проводити консультацію з офтальмологом. Ускладнення, загрозливі щодо зору, зустрічаються рідко, але дуже важливо їх діагностувати і лікувати до того, як відбудеться необоротне погіршення.
— Для зниження внутрішньоочного тиску у хворих з ГРДС доцільно використовувати препарати, що дозволяють ефективно контролювати ВОТ протягом доби. Аналоги простагландину максимально і найбільш стабільно зменшують ВОТ протягом 24-годинного циклу. Безконсервантні препарати, такі як Монопрост, — це кращий вибір.
— Для корекції порушень очної поверхні у хворих із ГРДС як сльозозамінники рекомендується застосовувати безконсервантні препарати, що містять трегалозу з осмо- і біопротекторними властивостями в поєднанні з гіалуроновою кислотою (Теалоз® Дуо), антибіотик азитроміцин (Азитер®). Гігієну повік проводити серветками Блефаклін®.
— З огляду на патогенетичні особливості дії SARS-CoV-2 у постковідний період слід очікувати на гаму специфічних і неспецифічних офтальмологічних порушень, які потребують своїх рішень. Але це буде крок 2.
Отримано/Received 29.01.2021
Рецензовано/Revised 10.02.2021
Прийнято до друку/Accepted 21.02.2021

/37.jpg)
/38.jpg)