Резюме
Заочеревинний (ретроперитонеальний) фіброз (РПФ) — рідкісне захворювання, що характеризується розростанням запальної та фіброзної тканини в заочеревинному просторі. Зазвичай ці розростання локалізуються навколо інфраренальної частини черевної аорти та клубових артерій, часто покриваючи сечоводи або інші органи черевної порожнини. Ідіопатичні захворювання становлять 70 % випадків. РПФ може бути асоційований з імуноглобуліном G4 (IgG4), що є причиною двох третин випадків ідіопатичного РПФ. Вторинний РПФ може розвинутись унаслідок інфекцій, злоякісних новоутворень, прийому лікарських препаратів, заочеревинної кровотечі або інших захворювань. Описано клінічний випадок ідіопатичного РПФ, імовірно, асоційованого з IgG4, у пацієнта, який пройшов симптоматичне оперативне лікування в урологічній клініці та продовжив лікування в ревматолога патогенетичною терапією (метилпреднізолон і мофетилу мікофенолат) зі значним поліпшенням. Для ревматологів дана патологія, безумовно, має клінічний інтерес, оскільки в основі цих змін лежать процеси, аналогічні таким при системних захворюваннях сполучної тканини, і з огляду на низьку захворюваність, що становить від 0,1 до 1,3 випадку на 100 000 людей на рік. Однак частіше такі пацієнти відразу потрапляють на прийом до лікарів суміжних спеціальностей (урологів, нефрологів, хірургів, судинних хірургів), що підкреслює важливість розгляду цього клінічного випадку.
Забрюшинный (ретроперитонеальный) фиброз (РПФ) — редкое заболевание, характеризующееся разрастанием воспалительной и фиброзной ткани в забрюшинном пространстве. Обычно эти разрастания локализуются вокруг инфраренальной части брюшной аорты и подвздошных артерий, часто покрывая мочеточники или другие органы брюшной полости. Идиопатические заболевания составляют 70 % случаев. РПФ может быть ассоциирован с иммуноглобулином G4 (IgG4), что является причиной двух третей случаев идиопатического РПФ. Вторичный РПФ может развиться вследствие инфекций, злокачественных новообразований, приема лекарственных препаратов, забрюшинного кровотечения или других заболеваний. Описан клинический случай идиопатического РПФ, вероятно, ассоциированного с IgG4, у пациента, прошедшего симптоматическое оперативное лечение в урологической клинике и продолжившего лечение у ревматолога патогенетической терапией (метилпреднизолон и мофетила микофенолат) со значительным улучшением. Для ревматологов данная патология представляет безусловный клинический интерес, поскольку, с одной стороны, в основе данных изменений лежат процессы, аналогичные таковым при системных заболеваниях соединительной ткани, а с другой стороны — это редкая патология, встречаемость РПФ составляет от 0,1 до 1,3 случая на 100 000 человек в год. Однако чаще такие пациенты сразу попадают на прием к врачам смежных специальностей (урологам, нефрологам, хирургам, сосудистым хирургам), что подчеркивает важность разбора такого клинического случая.
Retroperitoneal fibrosis (RPF) is a rare disease characterized by the proliferation of inflammatory and fibrous tissue in the retroperitoneum. These masses are commonly localized around the infrarenal part of the abdominal aorta and iliac arteries, often covering the ureters or other organs of the abdominal cavity; idiopathic diseases accounting for 70 % of cases. RPF may be associated with immunoglobulin G4 (IgG4), which accounts for two-thirds of idiopathic RPF cases. Secondary RPF may develop due to infections, malignant neoplasms, medication, retroperitoneal bleeding, or various other diseases. A clinical case of idiopathic RPF, probably associated with IgG4, was described in a patient who had undergone a symptomatic surgical treatment in an urological clinic and continued being treated by a rheumatologist, given pathogenetic therapy (methylprednisolone and mycophenolate mofetil) with a significant improvement. For rheumatologists, this pathology is of an undoubted clinical interest, since these changes are based on processes similar to those occurring in systemic diseases of the connective tissue, and the RPF is extremely rare, ranging from 0.1 to 1.3 cases per 100,000 patients per year. However, more often than not, such patients are referred to the doctors of ancillary specialties (urologists, nephrologists, surgeons, vascular surgeons). All of the abovementioned facts emphasize the importance of analyzing such a clinical case.
Введение
Забрюшинный (ретроперитонеальный) фиброз (РПФ) — редкое заболевание, характеризующееся разрастанием воспалительной и фиброзной ткани в забрюшинном пространстве. Обычно эти разрастания локализуются вокруг инфраренальной части брюшной аорты и подвздошных артерий, часто покрывая мочеточники или другие органы брюшной полости [1]. Заболевание впервые было описано J.K. Ormond в 1948 году и названо его именем [2], можно встретить другие названия данной патологии: фиброзный периуретрит, пластический периуретрит, хронический периуретрит и фиброзный ретроперитонит. Различают первичный (идиопатический) и вторичный РПФ. Идиопатические заболевания составляют около 70 % случаев. РПФ может быть ассоциирован с иммуноглобулином G4 (IgG4), что является причиной до двух третей случаев идиопатического РПФ [3]. Вторичный РПФ может развиться вследствие инфекций, злокачественных новообразований, приема лекарственных препаратов, забрюшинного кровотечения или различных других заболеваний.
РПФ — это достаточно редкое заболевание. По данным разных авторов, частота идиопатических (первичных) заболеваний колеблется от 0,1 до 1,3 случая на 100 000 человек в год [4], чаще болеют лица в возрасте от 40 до 60 лет с преобладанием мужчин от 2 : 1 до 3 : 1. Некоторые авторы [5] пишут об увеличении риска развития РПФ под влиянием табачного дыма и асбеста.
Частота вторичного РПФ неизвестна. Более 70 % случаев приходится на идиопатический РПФ, который является иммуноопосредованным заболеванием и может развиваться как самостоятельно, так и в рамках IgG4-ассоциированного заболевания. Среди факторов патогенеза выделяют генетические ассоциации с системой HLA-DRB1 антигенов, которые под влиянием факторов окружающей среды (асбест, курение) воздействуют на CD4+ Т-клетки аорты и забрюшинного пространства, повышая их способность к размножению и секреции интерлейкина (ИЛ) 6, который, в свою очередь, активирует B-клетки и фибробласты [6]. Также CD4+ Т-клетки секретируют ИЛ-4, ИЛ-10, ИЛ-13 и трансформирующий фактор роста β (TGF-β), которые стимулируют пролиферацию и созревание В-клеток в плазматические клетки и, таким образом, могут приводить к преимущественному увеличению плазматических клеток, продуцирующих IgG4 [7].
Для ревматологов данная патология может представлять клинический интерес, поскольку в основе данных изменений лежат процессы, аналогичные таковым при системных заболеваниях соединительной ткани. В связи с этим приводим описание случая РПФ у пациента, который прошел симптоматическое оперативное лечение в урологической клинике и был направлен для проведения патогенетической терапии к ревматологу.
Клинический случай
Больной Б., 62 лет, обратился на прием к ревматологу в октябре 2020 года с жалобами на боли в поясничной области без связи с физической нагрузкой, общую слабость, головокружение, тошноту и рвоту после приема пищи и воды, ощущение сухости во рту, снижение веса на 6 кг за последний месяц из-за отсутствия аппетита, эпизоды повышения температуры тела до 37,2–37,5 °С, головную боль и повышение артериального давления до 180/120 мм рт.ст.
Считает себя больным с августа 2020 года, когда постепенно стал отмечать затруднение мочеиспускания, боль в нижних отделах живота и пояснично-крестцовом отделе позвоночника, тошноту и рвоту. Был обследован у семейного врача, который заподозрил патологию почек и направил пациента на консультацию к урологу. Находился на лечении в урологическом отделении с 4.09.2020 по 28.09.2020, где был установлен диагноз: двусторонний уретерогидронефроз, хроническая болезнь почек (ХБП) III–IV стадии, нефрогенная гипертензия, объемное новообразование забрюшинного пространства. Проведена пункционная нефростомия слева 17.09.2020 и справа 29.09.2020 (рис. 1, фото пациента).
Из анамнеза жизни — туберкулез, сахарный диабет, болезнь Боткина отрицает, у отца — инсульт. В 2000 году — аппендэктомия, перитонит, в 2007 году — циркумцизия по поводу фимоза, в 2010 году — герниопластика паховой грыжи слева и справа.
При осмотре — состояние тяжелое, положение вынужденное, передвигается на каталке из-за общей слабости и головокружения. Сознание ясное. Нормостенического телосложения. Периферические лимфоузлы не пальпируются. Периферических отеков нет. Кожные покровы чистые, обычной окраски. Над легкими на всем протяжении перкуторно ясный легочный звук, аускультативно — везикулярное дыхание, хрипов нет. Границы относительной сердечной тупости: правая — в IV межреберье по правому краю грудины, верхняя — в III межреберье по левой парастернальной линии, левая — в V межреберье по левой срединноключичной линии. При аускультации сердца — тоны приглушены, деятельность сердца ритмичная, нерезко выраженный акцент 2-го тона на аорте, артериальное давление 100/60 мм рт.ст. Пульс 88 ударов в 1 минуту, удовлетворительных свойств, ритмичный. Язык сухой, обложен бело-желтым налетом. Живот при пальпации мягкий, безболезненный. Печень пальпаторно у края реберной дуги, селезенка не пальпируется. Симптом Пастернацкого отрицательный с обеих сторон. В области обеих почек установлены нефростомы, в обоих мочеприемниках жидкость светло-желтого цвета (справа 300 мл, слева 1500 мл). Стул обычного цвета и консистенции, без патологических примесей. Результаты лабораторных исследований представлены в табл. 1 и 2.
/49.jpg)
Кроме вышепредставленных, пациенту были проведены следующие лабораторные исследования: 6.10.2020 — С-реактивный белок (СРБ) — 60 мг/л, ревматоидный фактор — 10 МЕ/мл, антинуклеарные антитела — 0,82 ЕД/мл (отрицательный), раково-эмбриональный антиген — 1,64 нг/мл (отрицательный), железо — 16,4 мкмоль/л, общий холестерин — 4,73 ммоль/л, триглицериды — 1,55 ммоль/л, холестерин липопротеидов высокой плотности — 1,46 ммоль/л, холестерин липопротеидов низкой плотности — 2,57 ммоль/л, холестерин липопротеидов очень низкой плотности — 0,7 ммоль/л, коэффициент атерогенности — 2,20; коагулограмма: международное нормализованное отношение — 0,95, протромбин по Квику — 107,4 %, протромбиновое время — 12,7, фибриноген плазмы — 5,6 г/л. С учетом эпидемиологической обстановки пациент был обследован на коронавирусную инфекцию IgM SARS-CoV2 — 0,19 ед. (отрицательный). 13.10.20 полимеразная цепная реакция к SARS-CoV2 — 0,19 ед. (отрицательный). У пациента выявлено повышение IgG — 300 мг/дл (норма — до 100 мг/дл).
Проведены следующие инструментальные исследования: рентгенограмма органов грудной клетки: без инфильтративных и воспалительных изменений; рентгенограмма грудного отдела позвоночника: деформирующий спондилез Th5-Th11, остеохондроз Th7-Th11, поясничного отдела позвоночника: распространенный деформирующий спондилез, спондилоартроз, остеохондроз L1-L3, признаки двустороннего сакроилеита. Магнитно-резонансная томография крестцово-подвздошных сочленений: данных в пользу сакроилеита не выявлено. Фиброгастродуоденоскопия: эрозивная гастропатия, эрозивный бульбит, язва луковицы двенадцатиперстной кишки с признаками налета фибрина. Электрокардиография: синусовая тахикардия, признаки гипертрофии миокарда левого желудочка.
Заключение мультидетекторной (64-срезовой) компьютерной томографии (МСКТ) органов грудной, брюшной полости, забрюшинного пространства и таза с контрастированием (25.09.2020): объемный процесс забрюшинного пространства, средостения на исследуемом уровне, с инвазией мочеточника — признаки ретроперитонеального фиброза. Нижняя полая вена на уровне инфрапеченочной части расположена в толще инфильтративного компонента, просвет неравномерный. Правосторонний гидронефроз, левосторонняя пиелоэктазия, состояние после левосторонней нефротомии. Забрюшинная лимфаденопатия. Гепатомегалия. Левосторонний небольшой гидроторакс. Магнитно-резонансная томография органов грудной, брюшной полости, забрюшинного пространства и таза с контрастированием (в динамике, 02.10.2020): признаки диффузного утолщения стенки аорты на всем протяжении с наличием инфильтративного парааортального компонента с обструкцией мочеточников, вероятно, как проявлений хронического периаортита (рис. 2).
/50.jpg)
При проведении ультразвуковой допплерографии сосудов нижних конечностей вдоль брюшного отдела аорты, преимущественно по передней стенке, определяется новообразование толщиной до 2 см, умеренно васкуляризованное, на 6 см выше бифуркации циркулярно охватывает аорту. Эхокардиография сердца: признаки атеросклеротического аортокардиосклероза и гипертрофии миокарда левого желудочка, расширение грудного отдела аорты, уплотнение створок аортального и митрального клапанов; митральная регургитация 0–1-й ст., трикуспидальная регургитация 0–1-й ст. (среднее давление в легочной артерии 17 мм рт.ст., легочной гипертензии нет). Ультразвуковое исследование (УЗИ) органов брюшной полости и почек: признаки диффузной патологии паренхимы печени, признаки хронического холецистита, панкреатита. Незначительная двусторонняя пиелоэктазия. Признаки диффузной патологии паренхимы почек с признаками двустороннего пиелонефрита. По передней стенке брюшного отдела аорты, на протяжении от мечевидного отростка до пупка, визуализируется эхонеоднородное тканевое образование, расположенное циркулярно, неравномерно утолщенное на всем протяжении от 17 до 23 мм, с кровотоком при цветовом допплеровском картировании (рис. 3).
/51.jpg)
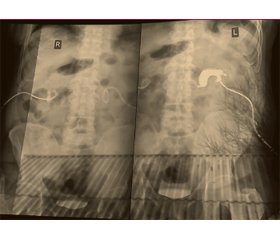
В области проекции нижнего полюса правой почки паранефрально визуализируется аналогичное образование размерами 43 на 35 мм. Данные тканевые образования соответствуют ретроперитонеальному фиброзу. На антеградной пиелографии — правый мочеточник проходим, имеется блок левой почки на уровне верхней трети левого мочеточника (рис. 4).
Больной проконсультирован хирургом и онкоурологом Харьковского онкологического центра — проведение биопсии невозможно в связи с риском для жизни пациента.
/52.jpg)
С учетом данных МСКТ и УЗИ, нарушения функции почек, наличия обструкции мочеточников, периаортита, исключения вторичных причин опухолевидного образования, характерного его расположения пациенту был установлен основной диагноз: идиопатический ретроперитонеальный фиброз (болезнь Ормонда) — примочеточниковый фиброз с обструкцией мочеточников. Двусторонний уретерогидронефроз. Состояние после пункционной нефростомии слева 17.09.2020 и справа 29.09.2020. Осложнения основного диагноза: ХБП IV стадии (скорость клубочковой фильтрации по EPI 31 мл/мин/1,73 м2) с поражением сосудов: периаортит с вовлечением в процесс брюшного отдела аорты, общих подвздошных артерий, верхней и нижней брыжеечных, почечных артерий, с вовлечением в процесс нижней полой вены на уровне инфрапеченочной части (по данным КТ от 25.09.20). Вторичная нефрогенная артериальная гипертензия: стадия 2, степень 2, риск высокий, сердечная недостаточность 1-й стадии. Лимфаденопатия: забрюшинная лимфаденопатия. Сопутствующий диагноз: недостаточность витамина D. Язвенная болезнь, активная фаза, активная язва луковицы двенадцатиперстной кишки. Хронический атрофический гиперпластический эрозивный гастродуоденит с нарушенной кислотообразующей функцией желудка. Диафрагмальная грыжа. Хронический некалькулезный холецистит, вне обострения. Хронический панкреатит, вне обострения. Данному пациенту возможно установление диагноза: вероятное IgG4-ассоциированное заболевание согласно комплексным критериям Н. Umehara и соавт. [8], учитывая наличие ретроперитонеального фиброза и повышение IgG4 более 135 мг/дл. Однако современные критерии ACR/EULAR для выставления диагноза подразумевают наличие 20 баллов и более, а в данном случае имеется только 14 [9]. Биопсия данному пациенту не проведена в связи с техническими сложностями и рисками для жизни, что отражено в заключениях онколога и хирурга. В клинике был проведен тщательный онкологический поиск, и злокачественное новообразование было исключено.
Пациенту было проведено лечение в условиях ревматологического отделения (дексаметазон внутривенно капельно в течение 5 последовательных дней, метилпреднизолон (МПЗ) в таблетках 48 мг в сутки, глюкоза, инсулин, метоклопрамид внутримышечно 1 мл 7 дней, конкор 5 мг в сутки, омепразол 20 мг 2 раза в сутки), а также лечение по поводу язвенной болезни (антибактериальная терапия, препараты висмута) с небольшим положительным эффектом в виде уменьшения одышки, тошноты, уменьшения показателей мочевины и креатинина, рубцевания язвы двенадцатиперстной кишки, однако патогенетическая терапия данного заболевания подразумевает назначение иммуносупрессивной терапии. Согласно данным литературы, глюкокортикоиды (ГК) из расчета 1 мг/кг по преднизолону считаются основой терапии идиопатического забрюшинного фиброза [10]. После выписки пациенту была назначена доза МПЗ 48 мг/д и витамин D 4000 МЕ/д, была достигнута некоторая положительная динамика как со стороны общего самочувствия, так и в плане снижения показателей мочевины и креатинина. Однако в связи с сохранением повышенных показателей азотистого обмена и общей лабораторной активности, отсутствием положительной динамики на МСКТ (сохранение размеров инфильтративного парааортального образования, диффузного утолщения аорты) в ноябре 2020 года пациенту дополнительно был назначен микофенолата мофетил (ММФ) в дозе 2 г/д. Назначение ММФ было основано на недавно опубликованных результатах рандомизированного контролируемого исследования, в котором у 69 пациентов с IgG4-ассоциированным заболеванием и РПФ сравнивали эффективность монотерапии ГК (в стартовой дозе 0,6–0,8 мг/кг) и комбинированной терапии ГК и ММФ в низкой дозе (1,0–1,5 г/д) [11]. Через 1 мес. эффективность двух схем иммуносупрессивной терапии была сопоставимой, однако через 1 год у больных, получавших комбинированную терапию, было отмечено значительное увеличение частоты ремиссии (76,5 против 51,4 %) и снижение кумулятивной частоты рецидивов (20,6 против 40,0 %). Отмечены высокая частота рецидивов РПФ, отдаленные побочные эффекты и невозможность контролировать заболевание на фоне монотерапии ГК, подчеркивается необходимость сочетания ГК с иммуносупрессивными препаратами [12].
При контрольном осмотре 10.12.2020 отмечалось значительное улучшение общего состояния в виде полного исчезновения одышки, тошноты, нормализации общего самочувствия, а также значительного снижения показателей мочевины до 10,0 ммоль/л и креатинина до 151 мкмоль/л, нормализации уровня гемоглобина и показателей воспалительной активности: СОЭ 11 мм/час, СРБ 6 мг/л. Пациент продолжает прием ММФ 2 г/д, дозу МПЗ рекомендовано снижать на 2 мг в неделю под контролем активности процесса, продолжить прием витамина D. Больной направлен на повторную консультацию к урологу для определения дальнейшей тактики лечения. 16.12.2020 проведена антеградная пиелография: отмечается положительная динамика — правый мочеточник стал проходим, но сохраняется блок левой почки на уровне верхней трети левого мочеточника (рис. 4). Рекомендовано продолжить лечение основного заболевания с контролем через 3 месяца.
Обсуждение
Согласно данным литературы [10], мониторинг реакции на медикаментозную терапию следует проводить в течение месяца после начала лечения для оценки улучшения клинической симптоматики, исчезновения боли и разрешения обструкции. В дальнейшем клиническую оценку симптомов и лабораторные показатели, включая СОЭ, СРБ и уровень креатинина, необходимо мониторировать каждые 2–3 месяца. МСКТ проводят через месяц после начала терапии и затем примерно каждые 4–6 месяцев, отслеживая размеры фиброзных масс. В дальнейшем обследование пациента с ретроперитонеальным фиброзом рекомендуется проводить каждые 6–12 месяцев, а МСКТ — каждые 1–2 года. Описаны случаи рецидива заболевания через 10 лет после прекращения терапии [13].
Анализируя данный клинический случай, необходимо акцентировать внимание на следующих моментах.
1. Мы впервые в своей клинической практике столкнулись с очень редкой патологией — ретроперитонеальным фиброзом, частота встречаемости которого составляет от 0,1 до 1,3 случая на 100 000 человек в год, что, безусловно, подчеркивает ценность нашего клинического наблюдения и опыта, приобретенного в период диагностики и продолжающейся курации пациента.
2. Использование только урологической хирургической помощи имеет симптоматическое значение и не модифицирует течение заболевания, не влияет на продолжающееся прогрессирование фиброзных изменений.
3. Безусловно, проведение патогистологического исследования помогло бы в дифференциации изолированного РПФ или IgG4-ассоциированного, но в наших условиях проведение биопсии не всегда выполнимо в связи с техническими трудностями. Кроме того, пациентам с типичной локализацией фиброзной массы и отсутствием клинических или лабораторных показателей злокачественного процесса не требуется открытая биопсия или открытое хирургическое вмешательство, если масса регрессирует в достаточной степени с помощью медикаментозной терапии для снятия обструкции. Лечение же РПФ, ассоциированного с IgG4 или нет, не отличается, что позволило инициировать патогенетическое лечение без патогистологического исследования.
4. Назначение цитостатической патогенетической терапии (МПЗ и ММФ) позволило значительно уменьшить клинические проявления заболевания и улучшить качество жизни пациента.
Таким образом, РПФ, являясь очень редкой и в то же время тяжелой для курации патологией, представляет наибольший интерес как для ревматологов, так и для врачей смежных специальностей (урологов, нефрологов, хирургов, сосудистых хирургов). Это связано, с одной стороны, с редкостью данной патологии. Когда пациенты обращаются к хирургам, нефрологам, урологам, они получают только хирургическую, как в данном случае, помощь. С другой стороны, отсутствие четких методов верификации диагноза, сложность диагностических критериев и трудность принятия решения о системной глюкокортикоидной и цитостатической терапии при наличии обширных фиброзных разрастаний со сдавлением сосудов и внутренних органов различной локализации также откладывает своевременное начало адекватного лечения. Тяжелое поражение внутренних органов, а также склонность к рецидивирующему течению значительно ухудшают качество жизни пациентов и требуют регулярного мониторинга и наблюдения. Обсуждение подобных редких клинических случаев необходимо для повышения информированности врачей и совместного мультидисциплинарного ведения подобных больных ревматологами, урологами, нефрологами, кардиологами и другими специалистами.
Выводы
1. Болезнь Ормонда (ретроперитонеальный фиброз) нуждается в дальнейшем изучении и разработке стандартов ведения пациентов с данной патологией.
2. Иммуносупрессивная терапия должна быть назначена в максимально ранние сроки, что позволит предотвратить развитие необратимого фиброза.
3. При далеко зашедших стадиях болезни лечение должно быть комплексным, включать в себя как медикаментозное воздействие, так и хирургическое вмешательство.
Конфликт интересов. Авторы заявляют об отсутствии какого-либо конфликта интересов и собственной финансовой заинтересованности при подготовке данной статьи.
Источники финансирования — нет.
Вклад каждого автора: Егудина Е.Д., Триполка С.А. — концепция и дизайн исследования; Триполка С.А. — сбор данных; Егудина Е.Д., Триполка С.А. — анализ и интерпретация данных; Егудина Е.Д. — написание статьи; Триполка С.А. — редактирование статьи.
/48.jpg)
/52.jpg)

/49.jpg)
/50.jpg)
/51.jpg)