Важной медицинской проблемой, возникающей вследствие ухудшения экологической ситуации и низкой санитарной культуры населения, является возрастающее количество паразитарных заболеваний [1].
По данным Всемирной организации здравоохранения (ВОЗ), гельминтозы занимают третье место в структуре инфекционных заболеваний человека. А экономический ущерб, наносимый кишечными гельминтозами, занимает четвертое место среди всех болезней и травм [2].
По данным ВОЗ, в мире 5,3 миллиарда человек находятся в группе риска, а 1,5 миллиарда инфицированы по крайней мере одним из гельминтов, передаваемых через почву: нематодным червем Ascaris lumbricoides, нематодами Necator americanus и Ancylostoma duodenale, а также Trichuris trichiura [3]. Несмотря на глобальное снижение инфекций, распространенность остается высокой в Азии, за которой следуют страны Африки к югу от Сахары и Латинская Америка [3]. Инфицированные люди преимущественно живут в плохих условиях в наименее развитых странах, где домохозяйства не имеют надлежащих условий и чистой воды. Заболеваемость коррелирует с количеством гельминтов, передаваемых инфицированными людьми. В то время как легкие инфекции обычно остаются бессимптомными, умеренные и тяжелые инфекции вызывают тяжелую заболеваемость [4], включая задержку роста, интеллектуальные нарушения, когнитивный и образовательный дефицит, недоедание и железодефицитную анемию [4].
По оценкам ВОЗ, в 2015 году глобальное бремя инфекций, вызванных передаваемыми через почву гельминтами (геогельминтозов), составило 3,4 млн DALY (лет жизни с поправкой на инвалидность) [6].
Согласно данным официальной статистики, в Украине регистрируют 300–400 тыс. случаев гельминтозов ежегодно, из них 80 % — у детей [7]. По результатам некоторых эпидемиологических исследований, уровень заболеваемости населения Украины гельминтозами ежегодно составляет 2 млн случаев [8–10], однако паразитологи считают, что реальное число может отличаться.
Рост распространенности паразитозов на территории Украины обусловлен высоким уровнем миграции населения, связанным с активным развитием деловых и культурных связей между странами и народами; изменением климатических условий и улучшением диагностики [11].
Сейчас известно около 300 видов гельминтов, которые могут вызывать заболевания у человека [7]. В Украине существует около 30 таких видов.
Наиболее распространенными заболеваниями являются энтеробиоз, аскаридоз, трематодоз [12–15].
Гельминтозами страдают все без исключения возрастные группы населения. Однако дети несколько чаще заражаются гельминтами, в силу отсутствия у них полноценных гигиенических навыков. Некоторые исследования доказывают большую восприимчивость детского организма к развитию гельминтоза, так как попадание яиц или цист гельминтов в организм взрослого человека не во всех случаях приводит к развитию того или иного гельминтоза. Кроме того, по сравнению со взрослыми проявления гельминтоза у детей имеют более выраженный характер и сопровождаются большим количеством жалоб [16].
По мнению экспертов ВОЗ, во всем мире наблюдается тенденция к недооценке медико-социального значения гельминтозов [17]. Гельминтозы часто являются последним звеном в цепи дифференциальной диагностики [18, 19]. Актуальность проблемы обусловлена прежде всего значительной распространенностью, выраженным негативным воздействием на организм человека, полиморфизмом клинических проявлений, что затрудняет дифференциальную диагностику заболеваний, отсутствием стерильного иммунитета и специфических методов профилактики [7].
Разнообразие возбудителей и циклов их развития обусловливает различную локализацию гельминтов в организме и определяет характер влияния как на орган поражения, так и на организм в целом. При этом клинические проявления не только неспецифичны, но и имеют сходство с большим количеством различных инфекционных и неинфекционных заболеваний, что послужило основанием для изучения клинических масок гельминтозов [19]. Симптоматика гельминтозов подобна клиническим проявлениям всевозможной органной патологии другого генеза, имеет слабовыраженный характер (или полностью отсутствует) независимо от тяжести патологического процесса; гельминтоз часто наслаивается на заболевания непаразитарного генеза [18].
Патологическое воздействие паразитов на организм включает: признаки хронической интоксикации, иммунные дисфункции, аллергизацию организма, диспептические расстройства, легочный синдром, лимфаденопатию, миалгию, железодефицитную анемию, канцерогенез, закупорку желчных протоков и протоков поджелудочной железы, очаги поражения в печени и поджелудочной железе, кишечную непроходимость, перфорацию кишечника, перитонит и др. [19].
В клинической картине гельминтозов нередко преобладают вегетативные и неврологические симптомы. Они зарегистрированы практически при всех широко распространенных глистных инвазиях: энтеробиозе, аскаридозе, трихоцефалезе, анкилостомидозах, гименолепидозе, тениаринхозе, описторхозе и др., что обусловлено патогенетическими особенностями глистной интоксикации. Вегетативные сдвиги нервной системы при наиболее распространенных паразитозах (энтеробиозе, аскаридозе, лямблиозе) проявляются чаще всего в виде изменений дермографизма, повышенного слюноотделения, ночного недержания мочи [21]. Доказано, что энтеробиоз является частой причиной бессонницы, беспокойного сна, скрежетания зубами по ночам, общей слабости, головных болей, головокружения и других проявлений астеноневротического синдрома, который приводит к повышенной раздражительности, рассеянности, снижению успеваемости в школе, умственной и физической работоспособности, формированию вредных привычек, а иногда — к возникновению эпилептиформных припадков [21, 22].
Таким образом, лечение гельминтозов остается актуальной проблемой современной медицины. Целью антигельминтной терапии является эрадикация паразита и ликвидация клинических проявлений инвазии. Применение этиотропного лечения нередко приводит к массивному распаду паразитов и всасыванию продуктов распада в кровь, что может стать причиной усиления интоксикации и сенсибилизации организма. Клиницист должен выбирать тот препарат, который обладает более высокой противопаразитарной активностью, хорошей переносимостью, высоким профилем безопасности.
В арсенале практических врачей сегодня находится более десятка антигельминтных препаратов.
По химическому строению антигельминтные препараты классифицируются:
— на производные бензимидазола (альбендазол, левамизол, мебендазол, тиабендазол, триклабендазол);
— препараты других химических групп: производные пиримидина (пирантела памоат), производные пиперазина (диэтилкарбамазин), производные салициламида (никлозамид), производные изохинолина (празиквантел), полусинтетический макроциклический лактон (ивермектин) [23].
Все антигельминтные средства по механизму действия можно разделить на 2 группы:
— средства, нарушающие функцию нервно-мышечной системы у круглых червей (пирантел, празиквантел, пиперазин, никлозамид, ивермектин);
— средства, действующие преимущественно на энергетические процессы гельминтов (альбендазол, мебендазол; клеточные яды (четыреххлористый этилен).
Основные действующие вещества в лечении гельминтозов: пиперазин, пирантел, левамизол, мебендазол, празиквантел, альбендазол [23].
Несмотря на достаточно широкий выбор антигельминтных средств, далеко не все они отвечают критериям эффективности и безопасности.
Среди известных антигельминтных средств широкого спектра из группы бензимидазола именно альбендазол является одним из самых широко используемых в клинической практике, особенно в современной педиатрии [24].
Альбендазол и мебендазол являются основными противогельминтными средствами, рекомендованными ВОЗ для глобальной дегельминтизации при геогельминтозах [25].
Альбендазол также используется для профилактической химиотерапии в лечении лимфатического филяриоза и онихоцеркоза. Поскольку альбендазол является глистогонным средством широкого спектра действия для лечения различных гельминтозов, а также геогельминтозов, в настоящее время он используется для химиотерапии токсокароза, гнатостомоза, эхинококкоза (кистозный эхинококкоз), тениоза и цистицеркоза [26, 27]. Сегодня оценивается полезность использования альбендазола в противораковой химиотерапии [28, 29].
Альбендазол представляет собой метиловый эфир бензимидазола (5-пропилтио-1H-бензимидазол-2-ил) карбаминовой кислоты, который впервые был одобрен как глистогонное средство для использования у человека в 1982 году [30, 31].
Альбендазол относительно нерастворим в воде и плохо всасывается в кишечнике (< 5 % у людей и 50 % у крупного рогатого скота). Степень всасывания в кишечнике сильно различается у разных видов животных и людей. Употребление жирной пищи значительно увеличивает абсорбцию, что важно для тканевых паразитов. Всасывание происходит быстро у людей и животных; максимальный уровень в крови достигается в течение 2–3 часов.
Фракция альбендазола метаболизируется в слизистой оболочке кишечника во время абсорбции, и альбендазол, который достигает плазмы после абсорбции, быстро метаболизируется в печени, главным образом до сульфоксида альбендазола и, наконец, сульфона альбендазола. Когда человек проглатывает 400 мг альбендазола, максимальная концентрация (Cmax) сульфоксида альбендазола в плазме составляет 0,16 мг/л; у животных уровни намного выше из-за различий в активности оксидаз цитохрома P450 и других флавинсодержащих оксидаз [31]. Сульфоксид альбендазола является терапевтически активной формой, и у человека его период полувыведения составляет 8–12 часов. Однако большая часть сульфоксида альбендазола далее превращается ферментами CYP2C в сульфон альбендазола, который не оказывает противоглистного действия [32].
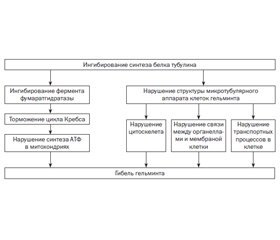
Механизм действия. Высокая терапевтическая эффективность и широкий спектр действия альбендазола обеспечивается благодаря двойному механизму действия (рис. 1):
— угнетение синтеза белка тубулина, что приводит к нарушению цитоскелета паразита;
— угнетение фумаратгидратазы (основного фермента в цикле Кребса паразита), следствием чего является нарушение процессов синтеза и усвоения глюкозы [30].
Альбендазол является единственным препаратом, влияющим на все стадии развития гельминтов (яйца, личинки, взрослые особи).
Очень важным фактом является то, что альбендазол проявляет действие в отношении таких кишечных гельминтов, как:
— нематоды Enterobius vermicularis, Ascaris lumbricoides, Triсhiurus triсhiura, Strongiloides stercoralis, Necator americanus, Cutaneous Larva Migrans Ancylostoma duodenale;
— цестоды Taenia solium, Hymenolepsis nana, Taenia saginata;
— трематоды Clonorchis sinensis и Opisthorhis viverrini;
— простейшие организмы (Giardia lamblia).
Альбендазол также эффективен при тканевых гельминтозах: Echinococcus granulosus — цистный эхинококкоз и Echinococcus multilocularis — альвеолярный эхинококкоз, также эффективен в терапии инвазии личинок T.solium (нейроцистицеркоз) и Gnatostoma spinigerum (капилляриоз).
Таким образом, альбендазол — антигельминтик широкого спектра действия: эффективен при энтеробиозе, анкилостомозе, некаторозе, гименолепидозе, тениозе, стронгилоидозе, аскаридозе, трихинеллезе, клонорхозе, кожных мигрирующих личинках, лямблиозе, капиллярозе, гнатостомозе, токсокарозе.
Альбендазол играет центральную роль в медикаментозной терапии кистозного эхинококкоза — паразитарного заболевания, возникающего из-за личиночной стадии метацестоды Echinococcus granulosus в печени (80 %), легких, почках, селезенке, миокарде [34]. Согласно результатам обзора [35], лечение эхинококковых кист альбендазолом связано с предотвращением рецидивов, уменьшением размеров и гибелью эхинококковых кист.
Отличительная черта альбендазола — его высокая эффективность и безопасность.
Побочные эффекты альбендазола, представленные в инструкции к препаратам на его основе: диарея, боль в области живота, в том числе в эпигастральной области, тошнота, рвота, головная боль, головокружение, реакции гиперчувствительности (кожная сыпь, зуд), повышение активности печеночных ферментов, лейкопения, панцитопения, обратимая алопеция, лихорадка [36].
В клинической практике побочные эффекты альбендазола относительно редки в сравнении с его широким применением для лечения гельминтозов, а серьезные побочные реакции встречаются очень редко, в основном при длительном приеме препарата или при приеме в комбинированной антигельминтной терапии [33, 34, 38].
S.D. Pion и соавторы показали, что массовая химиотерапия однократной дозой альбендазола (400 мг) два раза в год связана только с несколькими случаями жалоб на кратковременный дискомфорт в животе среди 871 и 825 человек, получавших лечение в Конго в 2012 и 2013 годах соответственно [37].
По данным зарубежных исследований, частота побочных эффектов увеличивается при одновременном применении альбендазола с диэтилкарбамазином и/или ивермектином [39]. Более половины пациентов с лимфатическим филяриозом, принимающих препараты, жаловались на симптомы головной боли, боли в суставах, зуд, боли в животе, слабость, головокружение и на некоторые объективные симптомы, такие как лихорадка, лимфаденит, повышение уровня ферментов печени, протеинурия, гематурия и временное снижение артериального давления. Эти побочные эффекты обусловлены не только введением альбендазола и/или комбинаций глистогонных или других препаратов, но и последствиями повышенной противоглистной активности препаратов. Так как мертвые тела филярий и микрофилярий дегенерируют в крови или в лимфе инфицированных хозяев, вместе с лекарствами это может способствовать развитию указанных побочных эффектов [39].
Гепатотоксичность — одна из наиболее частых побочных реакций альбендазола. Показано, что терапия альбендазолом может вызывать преходящее и бессимптомное повышение уровня аминотрансферазы в сыворотке крови почти у 50 % пациентов, получавших лечение более нескольких недель. Эти нарушения быстро нормализуются после прекращения терапии, которая требуется редко, в 4 % случаев. После применения альбендазола могут быть редкие случаи клинически очевидного повреждения печени при нескольких курсах лечения или через 1–2 недели после короткого курса альбендазола (1–3 дня). Характер повышения уровня ферментов сыворотки обычно гепатоцеллюлярный или смешанный. Могут присутствовать аллергические признаки (сыпь, лихорадка, эозинофилия), но они незаметны. Большинство случаев легкие, и после отмены препарата выздоровление происходит быстро. Имеются сообщения о быстром рецидиве с повторным повышением уровня ферментов сыворотки аналогичной степени тяжести [40].
В доступной литературе описан единичный случай с 25-летней латиноамериканской женщиной, поступившей в отделение клинической гепатологии с симптомами острого гепатита неустановленной этиологии. Ей был поставлен диагноз «гранулематозный гепатит, вызванный альбендазолом» после исключения других возможных причин на основании лабораторных исследований, биопсии печени, истории болезни, подробной истории приема лекарств и спонтанного улучшения биохимического профиля ее печени после отмены лекарств. Этот случай заслуживает особого внимания в связи с широким применением альбендазола в мире и распространенной медицинской проблемой гепатотоксичности, связанной с многими лекарственными препаратами [41].
Серьезные побочные реакции. Частота серьезных побочных эффектов немного выше в случае применения альбендазола в высоких дозах в течение длительного времени. Так, рекомендуемая доза альбендазола для лечения эхинококкоза у взрослых составляет 800 мг/день (два приема) в течение 1–2 месяцев. Результаты одного когортного исследования, в котором наблюдали 35 детей с абдоминальным эхинококкозом в Аргентине, свидетельствуют о небольшом повышении уровня ферментов печени и умеренной лейкопении, вызванной приемом альбендазола в дозе 10–15 мг/кг/день в течение одного месяца [42]. Кисты были инактивированы примерно у половины детей после терапии альбендазолом, и исследование показало, что доза была оптимальной для детей. Есть данные и о других серьезных побочных реакциях после комбинированного или длительного лечения, таких как лекарственный психоз, вызванный терапией альбендазолом и ивермектином [43], гемолитическая анемия и травмы почек и головного мозга, вызывающие острую почечную недостаточность в результате внутривенной инъекции альбендазола [44], потеря волос на теле [45] и токсический гепатит [46–48].
Описано сообщение, что один 68-летний мужчина, госпитализированный из-за сепсиса, умер из-за панцитопении, вызванной приемом альбендазола [49] в дозе 400 мг дважды в день в течение 16 дней при лечении эхинококкоза легких. Установлено, что костный мозг был серьезно подавлен, что привело к панцитопении, которую не удалось вылечить в больнице, и пациент умер из-за сильного кровотечения. Пациент страдал циррозом печени и нарушением функции печени, что приводит к снижению метаболизма в этом органе и высокому уровню циркулирующего альбендазола, который может ингибировать деление гемопоэтических клеток костного мозга. Врачу необходимо помнить, что длительное лечение альбендазолом требует обязательного контроля функции печени.
Таким образом, учитывая вышеизложенные данные, врачу при назначении длительной терапии альбендазолом следует контролировать активность печеночных ферментов до начала каждого цикла лечения и (желательно) каждые 2 нед. во время лечения. Если показатель более чем в 2 раза превышает верхнюю границу нормы, лечение альбендазолом следует прервать до полной его нормализации. Длительное лечение альбендазолом пациентов с нарушенной функцией печени, сердца или почек может привести к серьезным побочным эффектам.
Необходимо контролировать количество лейкоцитов в начале и каждые 2 нед. в течение каждого 28-дневного цикла лечения. Применение альбендазола при лейкопении можно продолжать в том случае, если степень снижения незначительная и лейкопения не прогрессирует.
Безопасность альбендазола при беременности. В инструкции к препаратам альбендазола есть особые указания на необходимость избегать его случайного применения в ранние сроки беременности. Женщинам репродуктивного возраста лечение альбендазолом следует начинать на 1-й неделе менструации или при отрицательном результате теста на беременность. Пациенток следует предупредить о необходимости применения эффективных методов контрацепции во время лечения альбендазолом и в течение 1 мес. после его отмены. Эти предостережения основаны на сведениях о тератогенном эффекте альбендазола у животных.
В одном корейском исследовании показано, что прием препарата у 124 женщин на ранних сроках беременности не вызывал опасных исходов [50]. В метаанализе показано отсутствие различий в отношении нескольких параметров клинических исходов среди беременных, получавших альбендазол во втором или третьем триместре [51]. Индийские национальные руководства по дегельминтизации во время беременности рекомендуют именно альбендазол (400 мг) как препарат выбора для дегельминтизации беременных женщин. При этом дегельминтизацию следует проводить после первого триместра беременности (желательно во время второго триместра) [51].
Учитывая, что использование монотерапии альбендазолом безопасно для массового лечения геогельминтозов и лимфатического филяриоза в эндемических районах, ВОЗ одобрила его использование во время беременности, однако длительное лечение альбендазолом недопустимо для беременных женщин.
Возможности применения альбендазола при грудном вскармливании. Показано, что после перорального приема в дозе 400 мг концентрация альбендазола и его метаболита альбендазола сульфоксида в грудном молоке настолько низкая, что вряд ли будет считаться вредной для ребенка, находящегося на грудном вскармливании [53].
Есть ли небезопасные взаимодействия альбендазола с другими препаратами? При одновременном применении альбендазола с циметидином, ингибиторами протонной помпы, дексаметазоном может повышаться концентрация препарата и его метаболитов в сыворотке крови, что может способствовать проявлению токсических эффектов, в частности гепатотоксичности [36]. Учитывая это, врач должен избегать подобных сочетаний.
В целом, анализируя вышеизложенное, можно утверждать, что альбендазол — наиболее эффективный и безопасный антигельминтный препарат, рекомендованный ВОЗ для химиопрофилактики и лечения широкого круга гельминтозов.
Частота побочных явлений при применении альбендазола очень незначительная, зависит от дозы, и неблагоприятные эффекты чаще наблюдаются при длительном применении высоких доз препарата или при сочетанном применении с другими антигельминтными средствами.
Безопасное применение препарата обеспечивает врач на основании знания фармакологических и фармакокинетических свойств лекарственного средства, противопоказаний, возможных взаимодействий, особенностей его применения с учетом индивидуальных отличий пациента и его сопутствующих заболеваний.
Возможности безопасного применения альбендазола обеспечиваются тем, что побочные эффекты препарата хорошо изучены и с точки зрения фармакоэпидемиологических подходов являются прогнозируемыми, т.е. такими, о которых врач осведомлен и может их предусмотреть и предотвратить.
Среди существующих на мировом фармацевтическом рынке антигельминтных препаратов одним из лидеров по потреблению среди препаратов альбендазола является Вормил.
Вормил отвечает всем критериям эффективного и безопасного антигельминтика [24]:
— универсальность и широта спектра действия: уничтожает всех гельминтов на разных стадиях развития и/или различной локализации;
— эффективность и скорость лечения;
— надежность: низкий процент необходимости повторного курса лечения;
— безопасность;
— комплайентность: наличие различных лекарственных форм (жевательные таблетки по 400 мг № 1; № 3; оральная суспензия (200 мг/5 мл — фл. 10 мл) обеспечивает удобство дозирования и применения у взрослых и детей при различных гельминтозах.
Большой, более чем 15-летний, опыт применения препарата Вормил в Украине свидетельствует, что это наиболее популярный, эффективный, безопасный, доступный и комплайентный для больного антигельминтный препарат.
Конфликт интересов. Не заявлен.

/71.jpg)