Резюме
Актуальність. Мозковий інсульт (МІ) та остеопороз — вік-залежні патології, що вражають переважно осіб літнього віку. Метою дослідження було вивчення мінеральної щільності кісткової тканини (МЩКТ), жирової, знежиреної маси та зв’язку між ними в пацієнтів, які перенесли МІ. Матеріали та методи. Було обстежено 84 пацієнти, які перенесли інсульт, та 124 особи відповідного віку та статі без неврологічної патології, які становили групу порівняння. МЩКТ, показники знежиреної та жирової маси визначали за допомогою двофотонної рентгенівської абсорбціометрії. Результати. У чоловіків і жінок, які перенесли МІ, частота остеопорозу була вірогідно вищою, ніж у осіб групи порівняння (12,5 та 1,7 %, 20,5 та 6,0 % відповідно). МЩКТ у жінок після інсульту була вірогідно нижче на рівні всіх обстежених ділянок, у чоловіків відмінності зареєстровані на рівні дистального відділу кісток передпліччя та всього скелета. У чоловіків, які перенесли МІ, виявлено вірогідно нижчі показники знежиреної маси (54,29 ± 1,22 кг та 58,02 ± 0,85 кг; р < 0,05), а у жінок — вірогідно нижчі показники жирової маси як у відсотках (41,96 ± 1,06 % і 44,84 ± 0,59 %; р < 0,05), так і в абсолютних цифрах (32,42 ± 1,92 кг та 36,71 ± 1,15 кг; р < 0,05). У чоловіків обох груп виявлено вірогідно позитивні зв’язки між МЩКТ всього скелета та показниками знежиреної маси. У жінок із МІ зареєстровано позитивні зв’язки помірної сили між показниками знежиреної маси та МЩКТ шийки стегнової кістки, верхніх кінцівок і всього скелета. А також, на відміну від чоловіків, зареєстровано вірогідні зв’язки жирової маси з МЩКТ всіх обстежених регіонів скелета. Висновки. Результати нашого дослідження показують, що МІ є фактором ризику розвитку остеопорозу і підкреслюють роль жирової та знежиреної маси в генезі остеопорозу у пацієнтів, які перенесли інсульт.
Актуальность. Мозговой инсульт (МИ) и остеопороз — возраст-зависимые патологии, поражающие преимущественно лиц пожилого возраста. Целью исследования было изучение минеральной плотности костной ткани (МПКТ), жировой, обезжиренной массы и связи между ними у пациентов, перенесших МИ. Материалы и методы. Было обследовано 84 пациента, перенесших инсульт, и 124 человека соответствующего возраста и пола без неврологической патологии, которые составили группу сравнения. МПКТ, показатели обезжиренной и жировой массы определяли с помощью двухфотонной рентгеновской абсорбциометрии. Результаты. У мужчин и женщин, перенесших МИ, частота остеопороза была достоверно выше, чем у лиц группы сравнения (12,5 и 1,7 %, 20,5 и 6,0 % соответственно). МПКТ у женщин после инсульта была достоверно ниже на уровне всех обследованных участков, у мужчин различия зарегистрированы на уровне дистального отдела костей предплечья и всего скелета. У мужчин, перенесших МИ, выявлены достоверно более низкие показатели обезжиренной массы (54,29 ± 1,22 кг и 58,02 ± 0,85 кг; р < 0,05), а у женщин — достоверно ниже показатели жировой массы как в процентах (41,96 ± 1,06 % и 44,84 ± 0,59 %; р < 0,05), так и в абсолютных цифрах (32,42 ± 1,92 кг и 36,71 ± 1,15 кг; р < 0,05). У мужчин обеих групп выявлены достоверные положительные связи между МПКТ всего скелета и показателями обезжиренной массы. У женщин с МИ зарегистрированы положительные связи умеренной силы между показателями обезжиренной массы и МПКТ шейки бедренной кости, верхних конечностей и всего скелета. А также, в отличие от мужчин, зарегистрированы достоверные связи жировой массы с МПКТ всех обследованных регионов скелета. Выводы. Результаты нашего исследования показывают, что МИ являются фактором риска развития остеопороза и подчеркивают роль жировой и обезжиренной массы в генезе остеопороза у пациентов, перенесших инсульт.
Background. Stroke and osteoporosis is an age-dependent pathology that affects elderly people mostly. The purpose of the study was to evaluated bone mineral density (BMD), fat mass, lean mass and their relationship in stroke patients. Materials and methods. We examined 84 stroke patients and 124 persons of the corresponding age and sex without neurological pathology, who made up the comparison group. BMD, fat mass and lean mass were determined using dual-energy X-ray absorptiometry. Results. The frequency of osteoporosis was significantly higher in stroke men and women than in the comparison group (12.5 versus 1.7 % and 20.5 versus 6.0 %, respectively). BMD in stroke women was significantly lower at all level observed, in men differences were recorded at distal radius and in the total body. The lean mass was significantly lower in stroke men (54.29 ± 1.22 and 58.02 ± 0.85 kg; p < 0.05), and the fat mass was significantly lower (32.42 ± 1.92 and 36.71 ± 1.15 kg; p < 0.05) in stroke women in comparison with control group. The men of both groups showed positive correlation between the BMD of the total body and the lean mass. Stroke women have positive relationships between fat mass and the BMD of the femoral neck, upper limbs, total body and significant correlation between fat mass and all regions of the skeleton. Conclusions. The results of our study show that stroke is a risk factor for the development of osteoporosis and emphasize the role of fat and lean mass in the development of osteoporosis in stroke patients.
Вступ
Порушення мозкового кровообігу та остеопороз — вік-залежні патології, що вражають переважно осіб літнього віку [1–3]. Згідно з даними Всесвітньої організації охорони здоров’я, у світі прогнозується збільшення кількості інсультів, що обумовлено збільшенням тривалості життя та постарінням населення, а також збільшенням поширеності чинників ризику мозкового інсульту (МІ) — гіпертонічної хвороби, цукрового діабету, паління тощо [1]. Наявність рухових, координаторних і зорових порушень внаслідок МІ призводить до збільшення ризику падінь, а також ризику переломів.
У пацієнтів, які перенесли МІ, ризик переломів стегнової кістки в 2–4 рази вище, ніж в популяції [4]. Виживання і відновлення рухової функції після перелому стегнової кістки у постінсультних пацієнтів вірогідно гірше порівняно з тими, хто не переніс МІ.
У 4 % пацієнтів, які перенесли оперативне втручання з приводу перелому стегнової кістки, протягом 1 року розвивається МІ, а у 5 % пацієнтів, які перенесли МІ, протягом 1 року відбувається перелом проксимального відділу стегнової кістки, що акцентує увагу на подібних факторах ризику цих двох станів [5].
Безумовно, велике значення в збільшенні ризику переломів має високий ризик падінь. Понад 80 % переломів викликані падіннями. Більшість літніх пацієнтів (65 років і старше) з переломом стегнової кістки падали на бік на стегно [6]. Пацієнти з геміпарезом падали на уражений бік, що пояснює переважну локалізацію переломів на боці парезу — 82 % [6–8]. Крім того, слабкість трицепса іпсилатеральної руки не дозволяє пом’якшити удар при падінні. Але не тільки збільшення частоти падінь пояснює високий ризик переломів. Основний пре–диктор остеопоротичних переломів — низька мінеральна щільність кісткової тканини (МЩКТ). Зокрема, зниження мінеральної щільності кісткової тканини на рівні проксимального відділу стегнової кістки на 2 SD збільшує ризик перелому при падінні в 7 разів [9]. У жінок у постменопаузальному періоді до чинників ризику розвитку остеопорозу та переломів відносять також низьку жирову та знежирену масу тіла [10, 11]. Подібних даних у пацієнтів, які перенесли інсульт, нами не знайдено.
Метою дослідження стало вивчення МЩКТ, жирової, знежиреної маси та зв’язку між ними в пацієнтів, які перенести МІ.
Матеріали та методи
У відділі клінічної фізіології та патології опорно-рухового апарату ДУ «Інститут геронтології імені Д.Ф. Чеботарьова НАМН України» було проведено обстеження кісткової тканини у 84 пацієнтів (40 чоловіків і 44 жінки), які перенесли МІ. Група порівняння була сформована зі 124 пацієнтів (60 чоловіків і 64 жінки), які звернулись в Український науково-медичний центр проблем остеопорозу, без неврологічної патології.
Пацієнти були стандартизовані за віком і масою тіла (табл. 1).
У дослідження включали чоловіків віком понад 50 років і жінок у постменопаузальному періоді з діагнозом МІ, підтвердженим методами нейровізуалізації (комп’ютерна або магнітно-резонансна томографія), з тривалістю постінсультного періоду від 2 місяців до 10 років.
Середня тривалість постінсультного періоду не відрізнялася у чоловіків і жінок і становила 1,86 ± 0,29 року та 1,66 ± 0,28 року (t = 0,43; р = 0,67) відповідно. У чоловіків і жінок переважав ішемічний тип інсульту (відповідно 93,2 та 72,5 %; р < 0,05). Тяжкість парезу була встановлена за шкалою інсульту NIH [10]. Помірний, середній та тяжкий ступінь парезу спостерігався у 27,5, 45 і 27,5 % чоловіків та 27,3, 47,7 і 25 % жінок. Обов’язковою умовою включення в дослідження була наявність добровільної інформованої згоди на участь пацієнта. У дослідження не включали хворих з наявними в анамнезі чи на момент включення в дослідження будь-якими захворюваннями з доведеним впливом на кісткову тканину та осіб, які приймають будь-які фармацевтичні засоби з подібним впливом, із соматичною патологією у декомпенсованому стані та з вираженою спастичністю, яка заважає проведенню та оцінці результатів двофотонної рентгенівської абсорбціометрії.
Мінеральну щільність кісткової тканини, показники знежиреної та жирової маси визначали за допомогою двофотонної рентгенівської абсорбціометрії (ДРА) на приладі Prodigy, GEНС Lunar (Мадісон, США, 2005). ДРА обстежували такі ділянки скелета: поперековий відділ хребта (L1–L4), проксимальний відділ стегнової кістки, шийку стегнової кістки, дистальний відділ кісток передпліччя та весь скелет. При проведенні ДРА визначали МЩКТ (г/см2), Т-показник, Z-показник. Інтерпретацію даних рентгенівської денситометрії проводили згідно з рекомендаціями Міжнародного товариства клінічної денситометрії (International society for clinical densitometry) [11]. Оцінку МЩКТ у чоловіків віком понад 50 років і жінок у постменопаузальному періоді проводили за значенням Т-показника на рівні поперекового відділу хребта, проксимального відділу стегнової кістки або шийки стегнової кістки (найнижчий показник). Значення Т-показника < –2,5 відповідає остеопорозу, в межах > –2,5 і < –1 — низькій мінеральній щільності кісткової тканини (остеопенії), > –1 — нормальній мінеральній щільності кісткової тканини. Серед показників тілобудови оцінювали жирову масу та знежирену масу всього тіла й апендикулярну знежирену (знежирена маса кінцівок).
Статистичний аналіз проводили із застосуванням програм Statistica 10, MEDCALC. Нормальність розподілу визначали за критерієм Шапіро — Уїлка. Різницю показників між групами та підгрупами встановлювали за допомогою однофакторного дисперсійного аналізу ANOVA, критерію Стьюдента для незалежних вибірок та критерію Манна — Уїтні. Регресійний аналіз показників МЩКТ та віку й антропометричних даних виконаний з використанням лінійної регресії та кореляції Спірмена при непараметричному розподілі. Відмінності розподілу вибірок оцінювали за допомогою критерію χ2. Результати подані як M ± m. Різницю показників вважали вірогідною при р < 0,05.
Результати
У чоловіків і жінок, які перенесли МІ, частота остеопорозу була вірогідно вищою, ніж у осіб групи порівняння (χс2 = 5,9, довірчий інтервал (ДІ) 1,7–25,1, p < 0,05 і χс2 = 5,3, ДІ 1,9–29,0, p < 0,05 відповідно). Серед чоловіків, які перенесли МІ, остеопороз реєструвався у 12,5 %, остеопенія — у 45 %, нормальна МЩКТ — у 42,5 %, у групі порівняння ці показники становили 1,7, 23,7 і 74,6 % відповідно. У жінок, які перенесли МІ, частота остеопорозу — 20,5 %, остеопенії — 47,8 %, нормальної МЩКТ — 31,7 %, а в групі порівняння — 6, 12,2 і 81,8 % відповідно.
Показники МЩКТ розподілялись нормально в обох групах згідно з критерієм Шапіро — Уїлка. МЩКТ у жінок після інсульту була вірогідно нижче на рівні всіх обстежених ділянок (поперековий відділ хребта, шийка і проксимальний відділ стегнової кістки, дистальний відділ кісток передпліччя і весь скелет) порівняно з аналогічними показниками групи порівняння (рис. 1).
На відміну від вищевикладеного у чоловіків вірогідні відмінності МЩКТ були зареєстровані тільки на рівні дистального відділу кісток передпліччя й усього скелета, а на рівні поперекового відділу хребта та шийки стегнової кістки вірогідно не відрізнялися (рис. 2).
При оцінці тілобудови у чоловіків, які перенесли ІМ, виявлено вірогідно нижчі показники знежиреної маси (54,29 ± 1,22 кг та 58,02 ± 0,85 кг; р < 0,05) та апендикулярної знежиреної маси (22,02 ± 0,59 кг і 25,59 ± 0,46 кг; р < 0,05) порівняно з особами групи І (рис. 3). При цьому вміст жирової маси як у відсотках (31,87 ± 1,26 % та 29,78 ± 0,91 %; р > 0,05), так і в абсолютних цифрах обох груп вірогідно не відрізнявся (26,64 ± 1,57 кг та 25,34 ± 1,08 кг; р > 0,05).
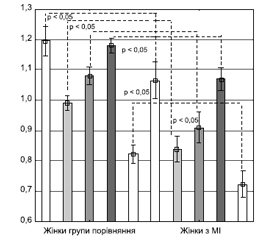
У жінок відмінності тілобудови були іншими (рис. 4). У пацієнток з МІ зареєстровані вірогідно нижчі показники жирової маси як у відсотках (41,96 ± 1,06 % і 44,84 ± 0,59 %; р < 0,05), так і в абсолютних цифрах (32,42 ± 1,92 кг та 36,71 ± 1,15 кг; р < 0,05). Відмінності знежиреної (42,59 ± 0,99 кг і 43,86 ± 0,71 кг; р > 0,05) та апендикулярної знежиреної маси (17,08 ± 0,43 кг та 17,98 ± 0,28 кг; р > 0,05) були невірогідними.
Також у чоловіків і жінок, які перенесли МІ, зареєстровано вірогідно нижчі показники кісткової маси порівняно з особами групи порівняння. У жінок цей показник становив 2,32 ± 0,08 кг і 2,69 ± 0,05 кг (р < 0,05), а у чоловіків — 3,11 ± 0,08 кг і 3,36 ± 0,05 кг (р < 0,05).
Отже, у чоловіків, які перенесли МІ, реєструються вірогідно нижчі показники кісткової маси та знежиреної маси, а у жінок — кісткової та жирової маси при відсутності відмінностей в показниках маси тіла.
Проведення регресійного аналізу показало, що у чоловіків, які перенесли МІ, виявлено вірогідно негативні зв’язки віку та МЩКТ на рівні шийки стегнової кістки (r = –0,36; p < 0,05), проксимального відділу стегнової кістки (r = –0,32; p < 0,05) та всього скелета (r = –0,37; p < 0,05). У чоловіків групи порівняння подібних зв’язків не виявлено. У жінок обох груп зареєстровано вірогідні зв’язки віку та МЩКТ на рівні всього скелета та проксимального відділу стегнової кістки. У жінок, які перенесли МІ, також виявлено зв’язки помірної сили МЩКТ на рівні поперекового відділу хребта (r = –0,42; p < 0,05) та шийки стегнової кістки. На особливу увагу заслуговують відмінності МЩКТ на рівні шийки стегнової кістки (r = –0,49; p < 0,05). У осіб групи порівняння зв’язок віку та МЩКТ цієї ділянки відсутній, а у жінок і чоловіків, які перенесли інсульт, зі збільшенням віку МЩКТ шийки стегнової кістки погіршується.
У чоловіків обох груп виявлено вірогідні позитивні зв’язки середньої сили між МЩКТ всього скелета та показниками знежиреної маси. Будь-яких зв’язків МЩКТ та показників жирової тканини у чоловіків обох груп не знайдено. У чоловіків групи із МІ знайдено зв’язок між МЩКТ нижніх кінцівок і знежиреною масою (r = 0,41; р < 0,05) на відміну від чоловіків групи порівняння. Зв’язків МЩКТ поперекового відділу хребта, проксимального відділу чи шийки стегнової кістки з показниками тілобудови не зареєстровано.
У жінок групи порівняння також не знайдено зв’язків МЩКТ аксіального скелета та показників тілобудови. Зареєстровано позитивні зв’язки помірної сили між показниками знежиреної маси та МЩКТ верхніх кінцівок (r = 0,31; р < 0,05) і всього скелета (r = 0,39; р < 0,05). А також, на відміну від чоловіків, зареєстровано вірогідні зв’язки жирової маси з МЩКТ верхніх кінцівок (r = 0,39; р < 0,05), нижніх кінцівок (r = 0,30; р < 0,05) та всього скелета (r = 0,47; р < 0,05).
У дослідженні не виявлено впливу типу та локалізації інсульту на МЩКТ і показники тілобудови, що обумовлено малою кількістю та гетерогенністю вибірок (більша частина обстежених пацієнтів мали ішемічний тип інсульту).
Проте отримано вірогідні негативні зв’язки між кістковою масою й тривалістю постінсультного періоду у жінок (r = –0,34; р < 0,05) та між кістковою масою і тяжкістю парезу у чоловіків (r = –0,43; р < 0,05).
Обговорення
Результати нашого дослідження показали підвищену частоту остеопорозу (12,5 % у чоловіків та 20,5 % у жінок) та вірогідно нижчі показники МЩКТ у пацієнтів, які перенесли інсульт. Відмінності МЩКТ у жінок були зареєстровані на всіх обстежених ділянках, а в чоловіків — тільки на рівні всього скелета та дистального відділу кісток передпліччя. У літературних джерелах також зареєстровані нижчі показники МЩКТ, але ступінь відмінностей суттєво варіює [6, 12, 13], що, на нашу думку, обумовлено гетерогенністю обстежених. Протягом року після інсульту втрата кісткової маси на рівні паретичних кінцівок зростає до 12–17 % [4], що суттєво перевищує втрату, пов’язану з менопаузою, — 1,5 % на рік [14].
Детермінант втрати кісткової маси після інсульту досить багато: тривалість ліжкового режиму [4], тяжкість геміплегії [6, 15], а також низька маса тіла в доінсультний період [16]. Отже, ділянка обстеження, а також стать, вік, термін постінсультного періоду та ступінь парезу обстежених пацієнтів суттєво впливають на МЩКТ і, відповідно, на частоту остеопорозу.
У нашому дослідженні отримано зменшення знежиреної маси у чоловіків, які перенесли інсульт. Подібні зміни розглядаються в літературі як інсультасоційована саркопенія, яка розвивається більшою мірою в уражених кінцівках [3]. У літературних джерелах пацієнти не розділялись за статевою ознакою, проте більшість включених були чоловіками. Можливо, у жінок подібні зміни виражені меншою мірою, що обумовлено меншим відсотком знежиреної тканини в структурі тілобудови порівняно з чоловіками.
Жирова маса, напроти, більше виражена у жінок. За даними літератури, зниження жирової маси у жінок асоціюється зі збільшенням ризику переломів [17]. У нашому дослідженні у жінок із МІ зареєстрована нижча жирова маса, що також може бути одним із факторів ризику переломів. Крім того, отримано вірогідні зв’язки між показниками тілобудови й МЩКТ, що підкреслює роль параметрів тілобудови в генезі остеопорозу. Для жінок у постменопаузальному періоді показаний зв’язок між зниженням знежиреної маси та підвищенням ризику переломів незалежно від МЩКТ [18]. У нашому дослідженні не отримано відмінностей знежиреної маси у жінок групи порівняння та жінок з МІ, проте зареєстрований вірогідний зв’язок між МЩКТ стегнової кістки та показником знежиреної маси, що може обумовити опосередкований вплив знежиреної маси на ризик переломів.
Наявність значної кількості чинників, що впливають на кісткову тканину (стать, вік, маса тіла тощо), ускладнює визначення ролі одного з них. У нашому дослідженні не виявлено впливу окремих параметрів інсульту, як то локалізація, тип, тривалість на показники кісткової тканини, за винятком зв’язку між кістковою масою й тривалістю посттравматичного періоду у жінок і кістковою масою й ступенем парезу — у чоловіків. У літературі з’явились дані, які розглядають остеопороз як чинник ризику інсульту [19]. Отже, ймовірно, пацієнти, які перенесли МІ, вже мали нижчу МЩКТ та інші чинники ризику остеопорозу до виникнення інсульту. Це може бути одним із пояснень, чому, незважаючи на відмінності показників кісткової, жирової та знежиреної маси, між пацієнтами з МІ та особами групи порівняння не було виявлено впливу окремих параметрів МІ. До інших пояснень можна віднести специфічність вибірки хворих (високий відсоток пацієнтів з легким і помірним неврологічним дефіцитом та з тривалістю посттравматичного періоду до 1 року).
Згідно з даними літератури, медіана часу до настання першого перелому після інсульту в середньому становить 24 місяці [4], що створює досить велике терапевтичне вікно для впливу на кісткову тканину.
Висновки
Результати нашого дослідження показують, що МІ є фактором ризику розвитку остеопорозу, і підкреслюють роль жирової та знежиреної маси в генезі остеопорозу у пацієнтів, які перенесли інсульт.
Конфлікт інтересів. Автор заявляє про відсутність конфлікту інтересів при підготовці даної статті.
Список литературы
1. Мищенко Т.С. Эпидемиология цереброваскулярных заболеваний и организация помощи больным с мозговым инсультом в Украине / Т.С. Мищенко // Український вісник психоневрології. — 2017. — Т. 25, № 1. — С. 22-24.
2. Beaupre G.S. Bone-density changes after stroke / G.S. Beaupre, H.L. Lew // Am. J. Phys. Med. Rehabil. — 2006. — Vol. 85(5). — P. 464-72.
3. Schnitzer T.J. Bone mineral density in patients with stroke: relationship with motor impairment and functional mobility / T.J. Schnitzer, R.L. Harvey, S.H. Nack, P. Supanwanid, L. Maskala-Streff, Е. Roth // Top. Stroke Rehabil. — 2012. — Vol. 19(5). — P. 436-43. — doi: 10.1310/tsr1905-436.
4. Kapral M.K. Risk of fractures after stroke: Results from the Ontario stroke registry / M.K. Kapral, J. Fang, S.M. Alibhai, P. Cram, A.M. Cheung, L.K. Casaubon et al. // Neurology. — 2017. — Vol. 88. — P. 57-64. — doi: 10.1212/WNL.0000000000003457.
5. Wei M. Impact of Bone Fracture on Ischemic Stroke Recovery / M. Wei, L. Haiyian, К. Huo, Н. Su // Int. J. Mol. Sci. — 2018. — Vol. 19(5). — P. 1533. — doi: 10.3390/ijms19051533.
6. Huo K. Impact and risk factors of post-stroke bone fracture / Huo K., Hashim S.I., Yong K., Su Н., Qu Q.M. // World J. Exp. Med. — 2016. — Vol. 20; 6(1). — P. 1-8. — doi: 10.5493/wjem.v6.i1.1.
7. Carda S. Osteoporosis after Stroke: A Review of the Causes and Potential Treatments / S. Carda, C. Cisari, M. Invernizzi, M. Bevilacqua // Cerebrovasc. Dis. — 2009. — Vol. 28. — P. 191-200. — https://doi.org/10.1159/000226578.
8. Pluskiewicz W. Skeletal consequences in patients after stroke / W. Pluskiewicz Wojciech // Endokrynologia Polska/Polish Journal of Endocrinology. — 2011. — Vol. 62. — Numer/Number 1/2011 ISSN 0423–104X.
9. Forster A., Young J. Incidence and consequences of falls due to stroke: a systematic inquiry // BMJ. — 1995. — Vol. 311. — P. 83-86.
10. Moayyeri A. Body fat mass is a predictor of risk of osteoporotic fractures in women but not in men: a prospective population study / A. Moayyeri, R.N. Luben, N.J. Wareham, K.T. Khaw // J. Intern. Med. — 2012. — Vol. 271(5). — P. 472-80. — doi: 10.1111/j.1365-2796.2011.02443.x.
11. Sornay-Rendu E. Muscle mass is associated with incident fracture in postmenopausal women: The OFELY study / E. Sornay-Rendu, F. Duboeuf, S. Boutroy, R.D. Chapurlat // Bone. — 2017. — Vol. 94. — P. 108-113. — https://doi.org/10.1016/j.bone.2016.10.024.
12. NIH Stroke Scale. — https://stroke.nih.gov/documents/NIH_Stroke_Scale.pdf/. Accessed June 30, 2018.
13. Official Positions 2015 ISCD (Adult & Pediatric). — https://iscd.app.box.com/v/OP-ISCD-2015-Adult/. Accessed June 30, 2018.
14. Borschmann K. Exercise Protects Bone after Stroke, or Does It? A Narrative Review of the Evidence / K. Borschmann // Stroke Research. and Treatment. — 2012. — ID 103697, 12 p. http://dx.doi.org/10.1155/2012/103697.
15. Kim H.D. Change of Bone Mineral Density and Relationship to Clinical Parameters in Male Stroke Patients / H.D. Kim, S.H. Kim, D.K. Kim, H.J. Jeong, Y.J. Sim, G.C. Kim // Annals of Rehabilitation Medicine. — 2016. — Vol. 40(6). — P. 981-988. — http://doi.org/10.5535/arm.2016.40.6.981.
16. Поворознюк В.В., Григорьева Н.В. Менопауза и костно-мышечная система. — К.: Експрес, 2004. — 512 с.
17. Lazoura O. Bone mineral density alterations in upper and lower extremities 12 months after stroke measured by peripheral quantitative computed tomography and DXA / O. Lazoura, N. Groumas, E. Antoniadou, P.J. Papadaki, A. Papadimitriou, P. Thriskos et al. // J. Clin. Densitom. — 2008. — Vol. 11. — P. 511-517.
18. Hunnicutt J.L. Skeletal muscle changes following stroke: a systematic review and comparison to healthy individuals / J.L. Hunnicutt, C.M. Gregory // Topics in Stroke Rehabilitation. — 2017. — Vol. 24(6). — P. 463-471. — doi.org/10.1080/10749357.2017.1292720.
19. Lin C.H. A population-based five-year study on the risk of stroke in patients with osteoporosis in Taiwan / C.H. Lin, W.C. Chang, C.N. Kuo, H.C. Yu, C.C. Yang, Y.W. Lin, K.S. Hung, W.P. Chang // Bone. — 2015. — Vol. 72. — Р. 9-13. — https://doi.org/10.1016/j.bone.2014.11.007.

/56-1.jpg)
/57-1.jpg)
/57-2.jpg)
/58-1.jpg)