Мигрень является распространенным нейрососудистым расстройством, характеризующимся атаками головной боли, обычно односторонней, часто описываемой как тяжелая или пульсирующая, возникающей вместе с тошнотой или повышенной чувствительностью к сенсорным входам (свету, звуку, движениям головы) [1]. Во взрослой популяции распространенность мигрени варьирует от 3,3 до 21,9 % среди женщин и от 0,7 до 16,1 % среди мужчин. Пик приходится на возраст 25–55 лет. Мигрень приводит к большой социоэкономической нагрузке, что проявляется ростом прямых затрат в связи с использованием системы здравоохранения — посещением поликлиник, госпитализацией в палаты неотложной терапии, покупкой лекарственных средств, а также ростом непрямых затрат из-за отсутствия заболевших на рабочем месте либо низкой эффективности их труда. Мигрень оказывает нагрузку на семью: около 50 % респондентов сообщают, что растет их конфликтность с мужем/женой или детьми. Мигрень снижает качество жизни людей во время, сразу после и даже между эпизодами болезни [2].
В дополнение к этому мигрень тесно связана с развитием ряда других заболеваний и повреждений. Например, в систематическом обзоре и метаанализе [3, 4] наблюдательных исследований было продемонстрировано, что мигрень повышает риск развития ишемического инсульта: для мигрени с аурой относительный риск составил 2,88 (95% доверительный интервал (ДИ) 1,89–4,39), для мигрени без ауры — 1,56 (1,03–2,36). В проспективном когортном исследовании женщин [5] мигрень была связана с увеличением риска основных сердечно-сосудистых заболеваний (отношение рисков 1,50; 95% ДИ 1,33–1,69), инфаркта миокарда (1,39; 1,18–1,64), инсульта (1,62; 1,37–1,92), стенокардии / мероприятий по коронарной реваскуляризации (1,73; 1,29–2,32) по сравнению с женщинами без мигрени. Более того, мигрень приводила к достоверному росту сердечно-сосудистой смертности (1,37; 1,02–1,83).
Мигрень приводит также к субклиническим повреждениям головного мозга, визуализируемым с помощью магнитно-резонансной томографии (МРТ). Так, в поперечном исследовании [6] в мозжечковой области вертебробазилярного бассейна у пациентов с мигренью наблюдалась более высокая распространенность инфарктов по сравнению с контролем (5,4 и 0,7 % соответственно; р = 0,02; скорректированное отношение шансов 7,1; 95% ДИ 0,9–55). При этом наибольший риск был отмечен у пациентов с мигренью с аурой и частотой приступов 1 или более в месяц (15,8; 1,8–140).
С учетом всех вышеизложенных эпидемиологических и клинических данных об отрицательном влиянии мигрени становится очевидным, что данная патология требует обязательного лечения, а также внедрения комплекса мер по ее профилактике.
Существует ряд простых скрининговых тестов, позволяющих заподозрить мигрень врачам и самим пациентам. Наибольшую популярность среди них приобрел 3-пунктовый тест «ID Migraine», предложенный в 2003 г. [7]. Он был разработан специально для скрининга больных в рамках первичного звена здраво–охранения и состоит из трех вопросов: один касается наличия тошноты, другой — фотофобии, третий — нарушения функции (неспособности работать, учиться или выполнять иной вид деятельности в течение не менее чем 1 дня). Если пациент, характеризуя свою головную боль, отвечает положительно на два из трех вопросов, то вероятность наличия мигрени составляет 93 % (чувствительность 81 %, специфичность 75 %). Поскольку «ID Migraine» предназначен для использования в первичном звене здравоохранения, необходимо отобрать тех пациентов, которым рекомендовано прохождение данного теста. К ним относят: 1) пациентов, которые сообщают о 2 или более приступах головной боли в течение последних 3 месяцев, 2) больных, которые имеют намерение поговорить с врачом об их головных болях либо переживают головную боль, ограничивающую их способность работать, учиться или радоваться жизни. В систематическом обзоре и метаанализе, выполненном в 2011 г., снова была подтверждена пригодность этого краткого и легкого теста для клинической практики [8].
/98-1.jpg)
Классификация мигрени и ее диагностические критерии постоянно совершенствуются, чтобы оптимально отражать клиническую картину болезни и быть удобными для врачей. Длительное время в качестве опорного документа служила бета-версия (т.е. предварительная версия) 3-й редакции Международной классификации головных болей 2013 г. Однако в 2018 г. в журнале «Cephalalgia» была опубликована окончательная версия этой классификации [9], на которую ориентируется большинство ведущих клиник по всему миру. Классификация имеет много позиций, но наиболее важными из них являются мигрень без ауры, мигрень с аурой и хроническая мигрень. Описание этих позиций приведено во врезке к настоящему обзору.
Подходы к лечению мигрени также продолжают меняться. На первый план все больше выходят триптаны как группа, в большей степени удовлетворяющая лечебные ожидания врачей и их пациентов. Например, в одном из исследований [13] было продемонстрировано, что при назначении триптанов 84 % больных были удовлетворены и сообщали о том, что лечение было эффективным, в то время как аналогичный показатель при назначении нестероидных противовоспалительных средств (НПВС, включая аспирин) составил 37 %, анальгетиков (включая парацетамол) — 26 %, эрготамина — 47 %.
В более старых европейских рекомендациях 2007 г. была предложена двухступенчатая схема терапии, в соответствии с которой на первом этапе всем пациентам с данной болезнью назначали НПВС/анальгетики + при необходимости антиэметики. И лишь при неэффективности первого шага переходили ко второму — назначали триптаны [14]. Однако в 2013 г. по результатам одного из симпозиумов, состоявшихся в рамках XXI Всемирного конгресса по неврологии, был предложен уточненный алгоритм ведения больных с мигренозной болью (рис. 1) [15]. В соответствии с ним, как и прежде, для эпизодической легкой/умеренной мигрени в качестве терапии первой линии должны быть назначены НПВС/анальгетики. При их неэффективности используют триптаны. Однако если врач имеет дело с эпизодической умеренной/тяжелой мигренью, то в качестве терапии первой линии должны быть назначены триптаны. В случае высокой частоты атак (3 или более в месяц) должно быть назначено профилактическое лечение (используется широкий арсенал средств — пропранолол, амитриптилин, натрия вальпроат, топирамат и т.д.).
/99-1.jpg)
При хронической мигрени с избыточным употреблением лекарственных средств первым шагом должна быть отмена этих средств. Триптаны являются терапией первой линии при хронической мигрени с избыточным употреблением лекарственных средств или без избыточного употребления лекарственных средств; при этом триптаны назначают не более 10 дней в месяц. Как и при эпизодической мигрени с высокой частотой возникновения, для обеих форм хронической мигрени должна быть предусмотрена возможность профилактического лечения.
Учитывая высокую значимость триптанов для лечения мигренозной боли, мы посвятили настоящий обзор одному из наиболее хорошо изученных представителей данной фармакологической группы — ризатриптану. Его эффективность относительно плацебо не вызывает сомнений [16]. Поэтому оценка его эффективности в обзоре была выполнена относительно более старого, ставшего уже стандартным референсом препарата — суматриптана. Аналогичный подход был использован при оценке безопасности/переносимости и фармакоэкономических показателей ризатриптана.
В цитируемых исследованиях и метаанализах часто сравнивали множество триптанов между собой. При подготовке обзора из них были взяты только те сведения, которые касались ризатриптана и суматриптана.
Фармакологические свойства ризатриптана
Ризатриптан является агонистом серотониновых 5-HT1B/1D-рецепторов и относится к группе триптанов. Развиваемое им антимигренозное действие связывают с тремя основными механизмами: сужением менингеальных сосудов, подавлением нейрогенного воспаления, уменьшением проведения боли [17–19].
Стимуляция 5-HT1B-рецепторов приводит к сужению интракраниальных экстрацеребральных (т.е. менингеальных) сосудов, расширенных при мигрени. Стимуляция 5-HT1D-рецепторов блокирует высвобождение вазоактивных пептидов (например, пептида, связанного с геном кальцитонина (CGRP)) из периваскулярных тригеминальных ноцицептивных нервных терминалей. Это ведет к уменьшению экстравазации (выхода из сосудов) белков плазмы крови — эффект, важный для подавления нейрогенного воспаления. Наконец, стимуляция 5-HT1D-рецепторов ингибирует синаптическую трансмиссию (например, за счет угнетения высвобождения глутамата) от первичных ко вторичным сенсорным нейронам в тригеминоцервикальном комплексе, что ведет к уменьшению проведения боли.
После перорального приема [19] ризатриптан быстро всасывается, и максимальная концентрация в плазме крови (Tmax) достигается менее чем через 1 ч. Биодоступность составляет 40 %. Для сравнения, Tmax у суматриптана достигается через 2 ч, биодоступность составляет 14 %. Подобные фармакокинетические параметры предполагают, что ризатриптан должен действовать раньше (учитывая Tmax) и более сильно (учитывая биодоступность), чем суматриптан, что и было подтверждено в клинических исследованиях.
Прямое сравнение ризатриптана 10 мг с суматриптаном 100 мг в рандомизированном контролируемом исследовании P. Tfelt-Hansen и соавт. [20, 21]
В приводимом рандомизированном, двойном слепом, с тремя плацебо, параллельно-групповом исследовании сравнивали эффективность и безопасность ризатриптана 5 и 10 мг, суматриптана 100 мг и плацебо у 1268 амбулаторных пациентов при лечении одной мигренозной атаки. Ниже в краткой форме приведены основные результаты данной работы для тех доз препаратов, которые считаются оптимальными в лечебной практике (ризатриптан 10 мг и суматриптан 100 мг).
Чувствительность к лечению: процент пациентов, у которых тяжелая/умеренная головная боль сменилась на легкую/отсутствие боли.
Спустя 1 ч после начала лечения у достоверно большего количества пациентов, принимавших ризатриптан 10 мг, наблюдалось ослабление боли по сравнению с суматриптаном 100 мг (37 и 28 % соответственно; p ≤ 0,05). Спустя 4 ч чувствительность к лечению в обеих группах была одинаковой. Резервное обезболивающее средство использовалось с одинаковой частотой.
Чувствительность к лечению: процент пациентов с полным ослаблением головной боли.
Различия становились статистически достоверными в пользу ризатриптана 10 мг спустя 1,5 ч после начала приема препаратов. Спустя 2 ч после начала лечения достоверность различий сохранялась: у большего количества пациентов, принимавших ризатриптан 10 мг, наблюдалось полное отсутствие боли по сравнению с суматриптаном 100 мг (40 и 33 % соответственно; p = 0,032).
Вероятность ослабления головной боли с тяжелой/умеренной до легкой/отсутствия боли.
После коррекции на дисбаланс по возрасту (пациенты в группе суматриптана были старше) выяснилось, что прием ризатриптана 10 мг был связан с достоверно большей вероятностью ослабления боли в течение 2 ч после начала лечения по сравнению с суматриптаном 100 мг (отношение рисков (ОР) 1,21; р = 0,032).
Выраженность функциональных нарушений по 4-категориальной шкале («нормальная функция», «легко нарушена», «тяжело нарушена», «требуется нахождение в постели»).
Различия становились статистически достоверными в пользу ризатриптана 10 мг спустя 1 и 1,5 ч после начала приема препаратов. Спустя 2 ч после начала лечения степень функциональных нарушений была также снижена у достоверно большего количества пациентов в группе ризатриптана 10 мг по сравнению с суматриптаном 100 мг (42 и 33 %; р = 0,015).
Наличие тошноты
Спустя 2 ч после начала лечения у достоверно большего количества пациентов, принимавших ризатриптан 10 мг, не было отмечено тошноты по сравнению с суматриптаном 100 мг (75 и 67 % соответственно; р ≤ 0,01).
Безопасность и переносимость
В ходе исследования у достоверно меньшего количества пациентов, принимавших ризатриптан 10 мг, были отмечены побочные эффекты по сравнению с суматриптаном 100 мг (33 и 41 %; р = 0,014).
Выводы
По результатам исследования авторы сделали вывод о том, что ризатриптан 10 мг имеет более быстрое начало действия и ослабляет головную боль и сочетанные симптомы более эффективно, чем суматриптан 100 мг. Профиль безопасности и переносимости обоих лекарственных средств был приемлемым.
Результаты метаанализа M.D. Ferrari и соавт. [20, 22]
Авторы первого метаанализа попросили фармацевтические компании и ключевых исследователей, не зависимых от фармацевтических компаний, предоставить им исходные данные рандомизированных, двойных слепых, контролируемых клинических исследований применения пероральных триптанов при мигрени. Затем они выполнили суммарную оценку по всем этим исследованиям в отношении важных параметров эффективности и переносимости (53 исследования, из них 12 неопубликованных; 24 089 пациентов) и отдельно суммировали данные по прямым сравнительным исследованиям (22 исследования; остальная статистика была недоступна).
В конечном счете авторы соединили результаты двух вышеописанных анализов и представили их в виде таблицы (табл. 1). Было установлено, что ризатриптан 10 мг лучше ослабляет боль в течение первых 2 ч лечения, способствует меньшему числу рецидивов в течение 24 ч после приема препарата, лучше устраняет боль, если рецидив все-таки возникнет, по сравнению с суматриптаном 100 мг. При этом переносимость обоих препаратов была одинаковой.
Результаты метаанализа J.D. Belsey [20, 23]
В следующий метаанализ также были включены рандомизированные, двойные слепые, плацебо-контролируемые исследования применения пероральных триптанов при мигрени. Он состоял из двух систематических обзоров, выполненных в параллели: один был посвящен эффективности (28 исследований с 45 осями активной терапии), другой — переносимости (35 исследований с 52 осями активной терапии).
Мы представили результаты данного метаанализа в виде таблицы (табл. 2) по аналогии с тем, как это сделали авторы предыдущего метаанализа. Видно, что ризатриптан 10 мг у большего количества пациентов приводит к полному ослаблению боли спустя 2 ч лечения по сравнению с суматриптаном 100 мг, при этом переносимость обоих препаратов была одинаковой.
Автор цитируемого метаанализа выполнил также комбинированный анализ эффективности и переносимости, результаты которого представил графически (рис. 2), поместив суматриптан 100 мг в начало координат. При таком подходе отчетливее видно превосходство ризатриптана 10 мг над препаратом сравнения.
Способность восстанавливать нормальную функцию
Авторы следующей работы [24] подчеркнули, что очень часто оценка эффективности лечения мигрени сфокусирована на нивелировании симптомов данной болезни, а не на том, насколько восстановлена функция. В связи с этим они выполнили ретроспективный подгрупповой анализ данных из 5 рандомизированных, двойных слепых, плацебо-контролируемых исследований, в которых пероральный ризатриптан прямо сравнивался с другими пероральными триптанами в отношении острой терапии умеренных и тяжелых мигренозных атак. Выраженность функциональных нарушений оценивали по 4-категориальной шкале («нормальная функция», «легко нарушена», «тяжело нарушена», «требуется нахождение в постели»).
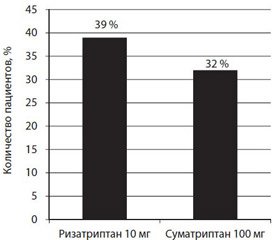
Было обнаружено, что большинство пациентов (94–100 %) в каждом исследовании и каждой лечебной группе имели некоторый уровень функциональных нарушений в исходных условиях. Спустя 2 ч после начала лечения достоверно большее количество пациентов в группе ризатриптана 10 мг возвращалось к нормальной функции по сравнению с суматриптаном 100 мг (39 и 32 % соответственно; отношение шансов (ОШ) 1,4; р = 0,021) (рис. 3). Эти результаты были получены на основе анализа 772 мигренозных атак.
Анализ «затраты — эффективность»
В транснациональном сравнении [25], выполненном на основе метаанализа J.D. Belsey [23], был проведен анализ показателя «затраты — эффективность» пероральных триптанов для шести стран — США, Великобритании, Канады, Германии, Италии и Нидерландов.
В итоге было выяснено, что прием ризатриптана 10 мг был связан с самыми низкими затратами на приобретение препарата во всех шести проанализированных странах в расчете на 1 пациента, у которого боль полностью исчезала спустя 2 ч после начала лечения.
В дополнение к этому в одном из фармакоэкономических обзоров приводятся сведения о том, что «затраты — эффективность» ризатриптана дают лучшее соотношение по сравнению с эрготамином/кофеином и НПВС/анальгетиками [26].
Заключение
Данные эпидемиологических исследований свидетельствуют о высокой распространенности мигрени среди населения, с вытекающим отсюда нарушением жизнедеятельности людей и большими экономическими затратами. Ситуация усугубляется способностью мигрени провоцировать развитие сердечно-сосудистых заболеваний и субклинических повреждений головного мозга. В связи с этим поиск эффективных средств для лечения данного вида головной боли продолжает иметь важное значение.
По состоянию на сегодняшний день были выполнены исследования, в которых продемонстрированы преимущества триптанов в терапии мигрени по сравнению с более старыми группами — алкалоидами спорыньи (эрготамин) и НПВС/анальгетиками. Это повлекло за собой соответствующую модификацию лечебных алгоритмов: при умеренной/тяжелой мигрени в качестве терапии первой линии сразу рекомендованы триптаны, минуя шаг апробации более старых средств.
Вместе с тем триптаны также оказались неодинаковыми, давая разное нетто эффективности, переносимости и фармакоэкономической целесообразности. В рамках настоящего обзора были продемонстрированы отчетливые преимущества ризатриптана перед стандартным референсным средством суматриптаном в отношении эффективности и экономической выгоды, в то время как переносимость обоих препаратов была одинаковой и клинически приемлемой. Следовательно, ризатриптан имеет хорошую доказательную базу эффективности и переносимости и остается препаратом выбора при лечении мигрени.
У большинства больных оптимальный лечебный эффект ризатриптана будет наблюдаться при дозе 10 мг. При необходимости прием следующей дозы осуществляется не ранее чем через 2 ч после начала лечения. В течение суток, по данным международных рекомендаций, может быть принято не более 30 мг ризатриптана, по данным отечественных инструкций к препарату — не более 20 мг.
Подготовил к.м.н. А.В. Савустьяненко
UA-RIZO-PIM-042018-005
Получено 05.02.2018
Список литературы
1. Miller S., Matharu M.S. Migraine is underdiagnosed and undertreated // Practitioner. — 2014. — V. 258, № 1774. — P. 19-24.
2. Lipton R.B., Bigal M.E. Migraine: epidemiology, impact, and risk factors for progression // Headache. — 2005. — V. 45 (Suppl. 1). — P. S3-S13.
3. Risk of ischaemic stroke in people with migraine: systematic review and meta-analysis of observational studies / Etminan M., Takkouche B., Isorna F.C., Samii A. // BMJ. — 2005. — V. 330, № 7482. — P. 63.
4. Correction for full version of this article; Risk of ischaemic stroke in people with migraine: systematic review and meta-analysis of observational studies // BMJ. — 2005. — V. 330, № 7491. — P. 596.
5. Migraine and risk of cardiovascular disease in women: prospective cohort study / Kurth T., Winter A.C., Eliassen A.H., Dushkes R. et al. // BMJ. — 2016. — V. 353. — P. i2610.
6. Migraine as a risk factor for subclinical brain lesions / Kruit M.C., van Buchem M.A., Hofman P.A. et al. // JAMA. — 2004. — V. 291, № 4. — P. 427-434.
7. A self-administered screener for migraine in primary care: The ID Migraine validation study / Lipton R.B., Dodick D., Sadovsky R. et al. // Neurology. — 2003. — V. 61, № 3. — P. 375-382.
8. Diagnostic accuracy of the ID Migraine: a systematic review and meta-analysis / Cousins G., Hijazze S., Van de Laar F.A., Fahey T. // Headache. — 2011. — V. 51, № 7. — P. 1140-148.
9. The International Classification of Headache Disorders, 3rd
edition / Headache Classification Committee of the International Headache Society (IHS) // Cephalalgia. — 2018. — V. 38. — P. 1-211.
10. Критерии диагностики основных видов первичных головных болей согласно новым изменениям в Международной классификации головных болей (МКГБ), версия 3 бета, 2013 / Лебедева Е.Р., Осипова В.В., Табеева Г.Р., Олесен Е. // Уральский медицинский журнал. — 2014. — № 3. — С. 5-8.
11. Морозова О.Г. Мигрень: новые международные критерии постановки диагноза и принципы терапии, основанные на доказательной медицине и собственном клиническом опыте // Міжнародний неврологічний журнал. — 2016. — № 3. — С. 131-138.
12. Практические вопросы ведения пациентов с хронической мигренью. Рекомендации российских экспертов / Латышева Н.В., Филатова Е.Г., Табеева Г.Р. и др. // Нервно-мышечные болезни. — 2015. — Т. 5, № 3. — С. 2-7.
13. An instrument to assess patient perceptions of satisfaction with acute migraine treatment (EXPERT Study) / Lantéri-Minet M., Massiou H., Romatet S. et al. // Headache. — 2011. — V. 51, № 4. — P. 590-601.
14. European principles of management of common headache disorders in primary care / European Headache Federation; Lifting The Burden: The Global Campaign to Reduce the Burden of Headache Worldwide; World Health Organization // J. Headache Pain. — 2007. — V. 8 (Suppl. 1). — P. S3-S47.
15. Evers S., Lisotto C. An Algorithm of Migraine Treatment // European Neurological Review. — 2013. — V. 8, № 2. — P. 149-152.
16. Total migraine freedom, a potential primary endpoint to assess acute treatment in migraine: comparison to the current FDA requirement using the complete rizatriptan study database / Rodgers A.J., Hustad C.M., Cady R.K. et al. // Headache. — 2011. — V. 51, № 3. — P. 356-368.
17. Canadian Headache Society Guideline: acute drug therapy for migraine headache / Canadian Headache Society Acute Migraine Treatment Guideline Development Group // Can. J. Neurol. Sci. — 2013. — V. 40, № 5 (Suppl. 3). — P. S1-S80.
18. Brandes J.L., Buchanan T.M., Welch K.M.A. Chapter 26 — Acute treatment of migraine // Handbook of Clinical Neurology. — 2010. — V. 97. — P. 323-336.
19. Bigal M.E., Krymchantowski A.V., Ho T. Migraine in the triptan era: progresses achieved, lessons learned and future developments // Arq. Neuropsiquiatr. — 2009. — V. 67, № 2B. — P. 559-569.
20. Göbel H. Efficacy and tolerability of rizatriptan 10 mg compared with sumatriptan 100 mg: an evidence-based analysis // Expert Rev. Neurother. — 2010. — V. 10, № 4. — P. 499-506.
21. Oral rizatriptan versus oral sumatriptan: a direct comparative study in the acute treatment of migraine. Rizatriptan 030 Study Group / Tfelt-Hansen P., Teall J., Rodriguez F. et al. // Headache. — 1998. — V. 38, № 10. — P. 748-755.
22. Oral triptans (serotonin 5-HT(1B/1D) agonists) in acute migraine treatment: a meta-analysis of 53 trials / Ferrari M.D., Roon K.I., Lipton R.B., Goadsby P.J. // Lancet. — 2001. — V. 358, № 9294. — P. 1668-1675.
23. Belsey J.D. Reconciling effectiveness and tolerability in oral triptan therapy: a quantitative approach to decision making in migraine management // J. Clin. Res. — 2003. — V. 4. — P. 105-125.
24 Restoring migraine sufferers’ ability to function normally: a comparison of rizatriptan and other triptans in randomized trials / Bussone G., D’Amico D., McCarroll K.A. et al. // Eur. Neurol. — 2002. — V. 48, № 3. — P. 172-177.
25. Belsey J.D. Cost effectiveness of oral triptan therapy: a trans-national comparison based on a meta-analysis of randomised controlled trials // Curr. Med. Res. Opin. — 2004. — V. 20, № 5. — P. 659-669.
26. McCormack P.L., Foster R.H. Rizatriptan: a pharmacoeconomic review of its use in the acute treatment of migraine // Pharmacoeconomics. — 2005. — V. 23, № 12. — P. 1283-1298.

/98-1.jpg)
/99-1.jpg)
/101-2.jpg)
/101-1.jpg)
/102-1.jpg)