Резюме
Співвідношення урикемії, магніємії, якості життя та функціонального резерву нирок при хронічній хворобі нирок (ХХН) остаточно не визначено. Нами проаналізовані ці показники в 145 пацієнтів із ХХН 1–5-ї стадії залежно від ступеня. Встановлено, що динаміка гіперурикемії й магніємії та урикемії й артеріального тиску має обернений кореляційний зв’язок і формує якість життя пацієнтів при ХХН 5-ї стадії. І навпаки, урикемія позитивно корелює з рівнем артеріального тиску й функціональним резервом нирки при ХХН 1–3-ї стадії. Пацієнти з гіперурикемією та ХХН 1–5-ї стадії мають вищу якість життя та більший нирковий резерв,ніж пацієнти з нормоурикемією, але в той же час у них збільшується ризик розвитку серцево-судинних та метаболічних порушень. Подальше накопичення даних та їх аналіз будуть підставою для формулювання практичних рекомендацій, зокрема, щодо доцільності застосування алопуринолу, фебуксостату та Магнероту залежно від ступеня урикемії, магніємії та ХХН.
Соотношение урикемии, магниемии, качества жизни и функционального резерва почек при хронической болезни почек (ХБП) окончательно не определено. Нами проанализированы эти показатели у 145 пациентов с ХБП 1–5-й стадии в зависимости от степени. Установлено, что динамика изменений гиперурикемии, магниемии, урикемии и артериального давления имеет обратную корреляционную связь и формирует качество жизни пациентов при ХБП 5-й стадии. И наоборот, урикемия положительно коррелирует с уровнем артериального давления и функциональным резервом почки при ХБП 1–3-й стадии. Пациенты с гиперурикемией и ХБП 1–5-й стадии имеют более высокое качество жизни и больший почечный резерв, чем пациенты с нормоурикемией, но в то же время у них увеличивается риск развития сердечно-сосудистых и метаболических нарушений. Дальнейшие накопление данных и их анализ будут основанием для формулирования практических рекомендаций, в частности, относительно целесообразности применения аллопуринола, фебукcоcтата, Магнерота в зависимости от степени урикемии, магниемии и стадии ХБП.
The ratio of uricemia, magnesia, quality of life and functional reserve of the kidneys in CKD has not been completely determined yet. These rates were analysed in 145 patients, depending on the CKD 1–5 stages. The dynamics in hyperuricemia, magnesia, uricemia and BP was established to have an inverse correlation and form the quality of life in patients with CKD 5th stage. Conversely, uricemia positively correlates with blood pressure and functional renal reserve in CKD 1–3 stages. Patients with hyperuricemia and CKD 1–5 stages have a high quality of life and greater renal reserve than patients with normouricemia, but at the same time they have increased risk for developing cardiovascular and metabolic disorders. Further accumulation of data and their analysis are needed for practical recommendations, in particular the rational of the use of allopurinol, febuxostat, Мagnerot, depending on the degree of uricemia, magnesia, and CKD stage.
Одним із основних документів з ведення хворих із подагрою на сьогодні є рекомендації EULAR, 2016 [1]. Нагадаємо вибірково основні положення щодо нефрологічної практики:
1. Кожна людина, яка має подагру, повинна систематично перевірятись на наявність супутніх захворювань та факторів ризику серцево-судинних захворювань, включаючи ниркову недостатність
2. Призначення гіпоурикемічної терапії (ГУТ) слід розглядати й обговорювати з кожним пацієнтом з визначеним діагнозом подагри з першого її епізоду. ГУТ призначається всім пацієнтам з рецидивами подагри, тофусами, уратною артропатією і/або нирковими каменями [2]. Ініціювання ГУТ рекомендується в найближчі строки від уперше встановленого діагнозу в пацієнтів до 40 років або в осіб із дуже високим рівнем урикемії (> 8,0 мг/дл, 480 ммоль/л)
і/або супутніми захворюваннями (порушення функції нирок, гіпертензія, ішемічна хвороба серця, серцева недостатність).
3. Для пацієнтів, які отримують ГУТ, показники урикемії слід контролювати та підтримувати на рівні < 6 мг/дл (360 ммоль/л). Нижчий цільовий рівень (< 5 мг/дл, 300 ммоль/л) для полегшення швидкого розчинення кристалів рекомендується для пацієнтів із тяжкою подагрою [3] до повного розчинення кристалів. Рівень урикемії < 3 мг/дл (180 ммоль/л) не рекомендується в довгостроковій перспективі.
Із клінічної практики відомо:
— рецидиви подагри можуть супроводжуватись нормальними значеннями урикемії;
— і навпаки, дуже високий рівень урикемії не обов’язково призводить до розвитку подагри [4];
— при порушенні функції нирок урикемія нерідко зростає, проте не відомо, до якого рівня.
Добре відомо, що зниження функції нирок супроводжується зростанням концентрації сечової кислоти в крові без наявних ознак подагри. Більше того, у пацієнтів, які отримують блокатори ренін-ангіотензин-альдостеронової системи, також відзначається збільшення базових рівнів урикемії. Нами проведено пошуковий аналіз залежності урикемії (а також магніємії та артеріального тиску — систолічного (САТ) та діастолічного (ДАТ)) від суб’єктивної оцінки якості життя в пацієнтів із хронічною хворобою нирок (ХХН). З огляду на те, що вищенаведені настанови підкреслюють важливість гіпоурикемічної терапії при зниженні функції нирок, нами про–аналізовано дві вибірки пацієнтів: тих, які отримують нирково-замісну терапію, та тих, які мають ХХН.
У табл. 1 наведені дані пацієнтів, які отримують лікування діалізом: із ХХН 5П (24 пацієнти) і ХХН 5Д стадії (88 осіб).
Наведені дані свідчать, що рівні урикемії та магніємії знаходились у межах нормальних значень, проте краща оцінка пацієнтом свого стану супроводжувалась більш високими показниками сечової кислоти та меншими значеннями артеріального тиску. 5 % пацієнтів отримували алопуринол або фебуксостат з метою зниження урикемії за наявності подагри. Статистично вірогідних відмінностей не отримано, проте загальні тенденції простежуються.
Звертає на себе увагу реципрокна зміна концентрації сечової кислоти й магнію в крові (коефіцієнт кореляції Спірмена –0,5; коефіцієнт кореляції Пірсона –0,623, сила зв’язку за шкалою Чеддока — помітна, t-критерій Стьюдента –0,796). Рівень урикемії мав обернений кореляційний зв’язок з величиною артеріального тиску (коефіцієнт кореляції Пірсона –0,679). У групі пацієнтів із ХХН 5-ї стадії, функція нирок у яких майже відсутня, відзначається така ж закономірність, як і в здорових людей. На наявність зв’язку між споживанням магнію та рівнями сечової кислоти в сироватці крові у своєму дослідженні вказав Y. Wang. У дослідженні взяли участь 5168 пацієнтів. Виявилося, що споживання магнію аліментарним шляхом обернено асоціюється з гіперурикемією. Ця закономірність була статистично підтверджена для чоловічої підгрупи, проте не для жіночої [5] Тому класичне призначення Магнероту, що знижує урикемію й підвищує рівень магнію [6], видається доцільним і для пацієнтів із ХХН 5-ї стадії.
Проте коректне призначення препарату подвійної дії потребує індивідуального підходу при ХХН 5-ї стадії. Наш особистий досвід свідчить, що прийом 1 таблетки Магнероту двічі на добу приводив до нормалізації рівня магніємії, але не був достатнім для суттєвого зниження гіперурикемії. Ці дані розширюють показання для призначення Магнероту, особливо в пацієнтів з помірною гіперурикемією і вираженим зниженням рівня магнію крові. З огляду на те, що Магнерот має дві діючі речовини, його застосування підвищує прихильність до лікування в пацієнтів, які отримують велику кількість інших медикаментів.
На рис. 1, 2 наведені окремо дані пацієнтів, які отримують перитонеальний діаліз (ПД) і гемодіаліз.
Як свідчать наведені дані, в осіб, які отримують перитонеальний діаліз, спостерігаються такі ж тенденції, проте рівні урикемії дещо нижчі. Реципрокні зміни (обернений кореляційний зв’язок) зберігаються в обох групах. Хворі на ПД, у яких зберігається залишкова функція нирок [7], мають більше показань для корекції Магнеротом.
Отже, аналізуючи показники осіб, які отримують нирково-замісну терапію, можна припустити, що краща якість життя супроводжується більш високими показниками урикемії, нижчими значеннями магніємії, ближчими до нормальних значеннями артеріального тиску. Проте виникає питання, чому більш високі рівні урикемії супроводжують кращу якість життя, а за наявності залишкової функції нирок у пацієнтів із ПД відзначаються менші значення урикемії. Можливо, справа у функціональному резерві нирок?
Розглянемо другу групу пацієнтів з гіперурикемією при ХХН 1–3-ї стадії.
За даними амбулаторних карт за 2014–2017 роки було визначено середні рівні сечової кислоти. Гіпер–урикемією вважалися середні рівні сечової кислоти, що перевищували 360 ммоль/л. Із 33 пацієнтів з хронічною хворобою нирок 1–3-ї стадії гіперурикемія була діагностована в 15 пацієнтів, нормальні значення сечової кислоти були у 18 пацієнтів (табл. 2). При порівнянні цих двох груп пацієнтів з використанням t-критерію Стьюдента було виявлено більш високі рівні креатиніну сироватки крові та діастолічного артеріального тиску в групі з гіперурикемією, а також у цих пацієнтів був вірогідно вищим функціональний нирковий резерв, визначений за методикою А.І. Гоженка [8], адаптованою до амбулаторних умов, з використанням водно-сольового навантаження 0,5% розчином натрію хлориду з розрахунку 0,5 % від маси тіла.
Після проведення оцінки якості життя з використанням неспецифічного опитувальника SF-36 (The Sort Form 36) і оцінки результатів за допомогою 8 шкал, у яких більш висока оцінка вказувала на більш високий рівень якості життя [9], виявлено, що пацієнти з високим рівнем сечової кислоти мали вищі показники якості життя, що відображено в табл. 3.
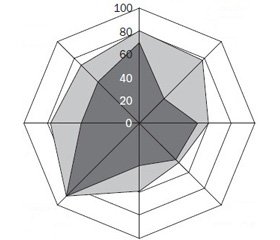
Статистично вищими були показники психічного здоров’я й життєвої активності в групі пацієнтів з гіперурикемією (рис. 3).
За результатами обстежень виявлено, що функціональний нирковий резерв у пацієнтів корелює з рівнем сечової кислоти сироватки крові, визначеним через 1 годину після водно-сольового навантаження, тобто чим вищий у пацієнта рівень сечової кислоти після навантажувальної проби, тим вищим був функціональний нирковий резерв. Показник середнього значення сечової кислоти мав сильніший кореляційний зв’язок із показником функціонального ниркового резерву (p = 0,62; p-level = 0,003), ніж значення сечової кислоти після водно-сольового навантаження (p = 0,52; p-level = 0,014).
Можна припустити існування такого механізму: оскільки сечова кислота є продуктом метаболізму продуктів білкового складу, то, можливо, саме її високі рівні чинять стимулюючий вплив на роботу нирок і збільшують швидкість клубочкової фільтрації з метою посилення виведення сечової кислоти і, відповідно, нормалізації її рівня. Показник середнього рівня сечової кислоти відображає динамічні зміни її концентрації в організмі пацієнта. Так, при однократному обстеженні можна отримати нормальні значення сечової кислоти, що не буде відповідати реальній картині. Тому при отриманні високих значень функціонального ниркового резерву, можливо, варто звернути більш прицільну увагу на пацієнта й простежити в динаміці за показниками його сечової кислоти, при необхідності — скорегувати їх. Наші дослідження свідчать, що жорсткий контроль рівня урикемії дозволяє загальмувати зниження швидкості клубочкової фільтрації [10].
Більш високі показники функціонального ниркового резерву тісно пов’язані з вищими показниками якості життя пацієнтів, такими як життєва активність, психічне здоров’я [11]. Це дуже важливо в умовах збільшення тривалості життя на фоні лікування, оскільки може забезпечити пацієнтам більшу інтегрованість у життя сім’ї, суспільства, довше збереження професійної активності.
Отже, аналізуючи та порівнюючи суб’єктивні дані — результати оцінки якості життя та об’єктивні результати досліджень, встановили наявність зв’язку між якістю життя пацієнтів та рівнями сечової кислоти. Пацієнти з гіперурикемією та ХХН 1–5-ї стадій мають вищу якість життя та більший нирковий резерв, ніж пацієнти з нормоурикемією, але в той же час у них збільшується ризик розвитку серцево-судинних та метаболічних порушень.
Потребує подальшого аналізу залежність рівня урикемії й функціонального ниркового резерву в пацієнтів з ХХН 5-ї стадії, які мають залишкову функцію нирок.
Оскільки зниження рівнів сечової кислоти є необхідною умовою покращення прогнозу пацієнтів, лікарю необхідно приділити більшу увагу психологічному стану пацієнта, що дасть змогу збільшити тривалість життя при збереженні його якості.
Отримані дані потребують проведення подальших досліджень для встановлення статистично значущих тенденцій, цільових значень урикемії в пацієнтів із ХХН 1–5-ї стадії з метою формулювання рекомендацій для нефрологічної практики.
Список литературы
1. Richette P., Doherty M., Pascual E. et al. Extended report 2016 updated EULAR evidence-based recommendations for the management of gout // Ann. Rheum. Dis. — Published Online First: on July 25, 2016. doi:10.1136/annrheumdis-2016-209707.
2. Aung T., Myung G., FitzGerald J.D. Treatment approa–ches and adherence to urate-lowering therapy for patients with gout // Patient preference and adherence. — 2017. — 11. — 795-800. doi:10.2147/PPA.S97927.
3. Sattui S.E., Gaffo A.L. Treatment of hyperuricemia in gout: current therapeutic options, latest developments and clinical implications // Therapeutic Advances in Musculoskeletal Disease. — 2016. — 8(4). — 145-159. doi:10.1177/1759720X16646703.
4. Поворознюк В.В., Дубецька Г.С. Гіперурикемія та подагра: сучасний погляд на проблему // Проблеми остеології. — 2012. — 15(3). — 19-25.
5. Wang Y. еt al. Association between dietary magnesium intake and hyperuricemia // PloSone. — 2015. — 10(11). — e0141079. doi.org/10.1371/journal.pone.0141079.
6. Кравчун П.Г., Крапивко С.А., Кравчун П.П., Кадыкова О.И. Влияние магния оротата на липидный обмен у больных хронической сердечной недостаточностью с сопутствующим сахарным диабетом 2-го типа // Международный эндокринологический журнал. — 2012. — 2(42). — 12-16.
7. Shen J.I., Saxena A.B., Vangala S., Dhaliwal S.K., Winkelmayer W.C. Renin-angiotensin system blockers and residual kidney function loss in patients in itiating peritoneal dialysis: an observational cohort study // BMC Nephrology. — 2017. — 18(1). — 196. doi: 10.1186/s12882-017-0616-4.
8. Гоженко А.І., Кравчук А.В., Сірман В.М., Никитенко О.П., Романів Л.В. Функціональний нирковий резерв: фізіологічне значення функціонального ниркового резерву та обґрунтування методики його визначення // Нирки. — 2015. — 4(14). — 7-11. doi: 10.22141/2307- 1257.0.4.14.2015.74890.
9. Khanna P.P., Perez-Ruiz F., Maranian P., Khanna D. Long-term therapy for chronic gout results in clinically important improvements in the health-related qualityoflife: short form-36 is responsive to change in chronic gout // Rheumatology (Oxford, England). — 2011. — 50(4). — 740-745. doi:10.1093/rheumatology/keq346.
10. Ivanov D.D., Ivanova M.D. SP326 Febuxostat improves GFR and BP in non-diabetic adults with CKD 2–3: 4 years follow-up // Nephrology dialysis transplantation. — 2015. — 30(3). — 486-487. https://doi.org/10.1093/ndt/gfv191.46
11. Савицька Л.М. Взаємозв’язок між функціональним нирковим резервом, рівнем сечової кислоти та якістю життя пацієнтів з ХХН І–ІІІ стадії // Нирки. — 2017. — 2(6). — 99-104. doi: http://dx.doi.org/10.22141/2307-1257.6.2.2017.102788

/156-2.jpg)
/156-1.jpg)
/157-1.jpg)
/157-2.jpg)
/158-1.jpg)