Резюме
Вступ. Колінний суглоб оточують різноманітні кістоподібні утворення (КПУ) — бурси, які у нормі клінічно не проявляються. Усі синовіальні порожнини, до яких, зокрема, належать колінний суглоб та бурси, які оточують колінний суглоб, містять синовіальну рідину. Синовіальна рідина є ультрафільтратом плазми крові і складається із білків та інтерстиціальної рідини. У літературі описані бурси, що оточують колінний суглоб, висвітлена ультразвукова класифікація кіст Бейкера залежно від стадії перебігу, яка запропонована І.М. Даниловою [10], та класифікація кістозного переродження меніска, але відсутня інформація щодо патофізіологічних та гістохімічних змін, які відбуваються у КПУ ділянки колінного суглоба, а також відсутня патофізіологічна модель КПУ ділянки колінного суглоба, яка б відображала природу даного захворювання з точки зору фізико-біохімічних процесів. Матеріали та методи. У травматологічному відділенні клініки ушкоджень Військово-медичного клінічного центру Північного регіону з початку 2016 року під спостереженням знаходилось 15 пацієнтів із клінічної картиною кістоподібного утворення ділянки колінного суглоба, що підтверджено інструментальними методами обстеженнями: ультразвуковим дослідженням (УЗД), магнітно-резонансною томографією (МРТ) та спіральною комп’ютерною артрографією (СКТА) колінного суглоба. Із них литково-напівперетинчастий бурсит спостерігався у 9 пацієнтів, кісти менісків — у 5 пацієнтів, бурсит переднього відділу колінного суглоба — в 1 пацієнта. Серед пацієнтів 11 чоловіків та 4 жінки. Середній вік пацієнтів становив 43,5 року. Об’єктом дослідження були кістоподібні утворення ділянки колінного суглоба. Усім хворим із КПУ проводили комплексне інструментальне обстеження, яке включало УЗД, СКТА, МРТ, вимірювання внутрішньосуглобового та внутрішньокістозного тисків за допомогою контактного манометра фірми Stryker та надалі — діагностично-лікувальної артроскопії. На основі отриманих даних УЗД проводився розподіл хворих на 4 групи, що базується на процентному відношенню внутрішньопросвітних нашарувань (включень) до загального просвіту КПУ, що дало можливість сформувати нову класифікацію КПУ ділянки колінного суглоба для вибору того чи іншого методу лікування. Результати та обговорення. Для формування та прогресування КПУ має значення підвищений тиск, який становить у середньому 29 мм рт.ст. у положенні згинання та до 58,4 мм рт.ст. у положенні розгинання. Виходячи із попередніх даних, на нашу думку, критичним показником тиску, при якому може настати розрив кісти Бейкера, є тиск більше 60 мм рт.ст. Зазвичай таке ускладнення виникає при тривалому існуванні кісти, коли тривала адсорбція білкових молекул на стінці кісти призводить до адсорбційного зниження міцності та зниження поверхневого натягу — ефект Ребіндера. Висновки. Враховуючи дані біохімічних процесів, УЗД та ендоскопії кіст Бейкера на різних стадіях, ми дослідили, що сама стінка кісти не потовщується, а відбувається пристінкове нашарування білкових молекул із формуванням глобул, які і формують так звану псевдостінку. У подальшому ці нашарування починають формувати перетинки між протилежними стінки, ущільнюватись, що призводить до камерності КПУ. На пізніх стадіях дані нашарування переважають над просвітом КПУ. Запропонована нами класифікація заснована на визначенні процентного відношення внутрішньопросвітних нашарувань до загального просвіту КПУ у двох зрізах та відображає основні морфологічні зміни, що дає можливість визначити оптимальний метод лікування даного кістоподібного утворення та широкого практичного використання у травматології та ортопедії.
Введение. Коленный сустав окружают разнообразные кистозные образования (КО) — бурсы, которые в норме клинически не проявляются. Все синовиальные полости, к которым, в частности, относятся коленный сустав и бурсы, окружающие коленный сустав, содержат синовиальную жидкость, которая является ультрафильтратом плазмы крови и состоит из белков и интерстициальной жидкости. В литературе описаны бурсы, окружающие коленный сустав, освещена ультразвуковая классификация кист Бейкера в зависимости от стадии течения, предложенная И.М. Даниловой [10], и классификация кистозного перерождения мениска, но отсутствует информация о патофизиологических и гистохимических изменениях, происходящих в КО области коленного сустава, а также отсутствует патофизиологическая модель КО области коленного сустава, которая отражала бы природу данного заболевания с точки зрения физико-биохимических процессов. Материалы и методы. В травматологическом отделении клиники повреждений Военно-медицинского клинического центра Северного региона с начала 2016 года под наблюдением находилось 15 пациентов с клинической картиной кистозного образования области коленного сустава, что подтверждено инструментальными методами обследованиями: ультразвуковым исследованием (УЗИ), магнитно-резонансной томографией (МРТ) и спиральной компьютерной артрографией (СКТА) коленного сустава. Из них икроножно-полуперепончатый бурсит наблюдался у 9 пациентов, кисты менисков — у 5 пациентов, бурсит переднего отдела коленного сустава — у 1 пациента. Среди пациентов 11 мужчин и 4 женщины. Средний возраст пациентов составил 43,5 года. Объектом исследования были кистозные образования области коленного сустава. Всем больным с КО проводили комплексное инструментальное обследование, которое включало УЗИ, СКТА, МРТ, измерение внутрисуставного и внутрикистозного давления с помощью контактного манометра фирмы Stryker и далее — диагностико-лечебной артроскопии. На основе полученных данных УЗИ проводилось распределение больных на 4 группы, базирующееся на процентном отношении внутрипросветных наслоений (включений) к общему просвету КО, что дало возможность сформировать новую классификацию КО области коленного сустава для выбора того или иного метода лечения. Результаты и обсуждение. На формирование и прогрессирование кистозных образований оказывает значение повышенное давление, которое составляет в среднем 29 мм рт.ст. в положении сгибания и до 58,4 мм рт.ст. в положении разгибания. Исходя из предварительных данных, по нашему мнению, критическим показателем давления, при котором может наступить разрыв кисты Бейкера, является давление более 60 мм рт.ст. Обычно такое осложнение возникает при длительном существовании кисты, когда имеет место адсорбция белковых молекул на стенке кисты, что приводит к адсорбционному снижению прочности и поверхностного натяжения — эффект Ребиндера. Выводы. Учитывая данные биохимических процессов, УЗИ и эндоскопии кист Бейкера на разных стадиях, мы обнаружили, что сама стенка кисты не утолщается, а происходит пристеночное наслоение белковых молекул с формированием глобул, которые и формируют так называемую псевдостенку. В дальнейшем эти наслоения начинают формировать перемычки между противоположными стенками, что приводит к камерности образования. На поздних стадиях данные наслоения преобладают над просветом КО. Предложенная нами классификация основана на определении процентного соотношения внутрипросветных наслоений к общему просвету кистозного образования в двух срезах и отражает основные морфологические изменения, что позволяет определить оптимальный метод лечения данного кистозного образования и широкого практического использования в травматологии и ортопедии.
Introduction. The knee joint is surrounded by a variety of cystic formations (CF) — bursa, which normally are not clinically manifested. All synovial cavities, particularly knee joints and bursa, which surround the knee joint, contain synovial fluid. Synovial fluid is an ultrafiltrate of the blood plasma and consists of proteins and interstitial fluid. The literature describes the bursa surrounding the knee joint, the ultrasound classification of Baker’s cysts depending on the stage of the course, which is offered by I.M. Danilova [10], and classification of cystic meniscal degeneration, but provides no information about the pathophysiological and histochemical changes that occur in CF of the knee joint, as well as no data on the pathophysiological model of the knee CF, which would reflect the nature of this disease in terms of physical and biochemical processes. Materials and methods. In the trauma department of the clinic of injuries of the Military Medical Center of the Northern Region from the beginning of 2016, we have observed 15 patients with a clinical picture of the knee cyst, verified by instrumental methods of examination: ultrasound investigation (UI), magnetic resonance imaging (MRI) and spiral computed tomographic arthrography (SCТA) of the knee joint. Of these, calf-semimembranosus bursitis was observed in 9 patients, meniscal cysts — in 5 patients, bursitis of the anterior knee — in 1 patient. Among patients, the men prevailed — there were 11 men and 4 women, respectively. The average age of patients was 43.5 years. The objects of the study were cystic formations of the knee joint. All patients with CF underwent a comprehensive survey that included UI, SCTA, MRI, measurement of intraarticular and intracystic pressure using contact manometer manufactured by the Stryker company and, subsequently, diagnostic and therapeutic arthroscopy. According to the US data, the patients were divided into 4 groups based on the percentage ratio of intraluminal layers (inclusions) to the total lumen of CF, making it possible to form a new classification of the knee CF to select a particular treatment. Results and discussion. The formation and progression of CF are influenced by a high blood pressure, which is an average of 29 mmHg in the flexion position and 58.4 mmHg in the extension position. Based on preliminary data, in our opinion, critical rates, at which rupture of a Baker’s cyst may occur, is pressure more than 60 mmHg. Usually, this complication occurs in chronic cyst when long-term adsorption of protein molecules on the cystic wall leads to the adsorption weakening of the strength and reduction of surface tension — Rehbinder effect. Conclusions. Taking into account the data of biochemical processes, ultrasound pictures and endoscopy data of the Baker’s cysts in various stages, we have found that the cyst wall itself doesn’t thickens, but there is parietal layers of protein molecules with the formation of globules, which form the so-called pseudowall. Subsequently, these layers are beginning to form the membranes between opposite walls, to thicken, leading to intimacy of a CF. In the later stages, these layers dominated over the lumen of a CF. This classification, which is offered by us, is based on the determination of percentage of intraluminal layers and the total lumen of a CF in two sections and reflects the main morphological changes that makes it possible to determine the optimal treatment for cystic formation and wide practical use in traumatology and orthopedics.
Статтю опубліковано на с. 37-44
Вступ
Колінний суглоб оточують різноманітні кістоподібні утворення (КПУ) — бурси, які у нормі клінічно не проявляються. У результаті патологічних змін, які у них виникають, дані утворення можна виявити за допомогою клініко-інструментальних методів обстеження. Інші кістоподібні утворення виникають у ділянці пошкодження або тривалого перевантаження структурних елементів колінного суглоба [8].
Патофізіологія кіст, що оточують колінний суглоб, залежить від їх етіології. В основі формування більшості кіст і мішкоподібних утворень лежить механічне та біохімічне подразнення [9]. Так, кіста Бейкера, або литково-напівперетинчастий бурсит, виникає при надмірному накопиченні синовіальної рідини у порожнині колінного суглоба із подальшим її перетіканням через отвір у задньомедіальному відділі капсули у литково-напівперетинчасту бурсу. Причиною надмірного скупчення рідини та розвитку синовіїту може бути будь-яка внутрішньосуглобова патологія. У переважній більшості це наслідки травм менісків, суглобового хряща, внутрішньосуглобових зв’язкових структур, а також дегенеративно-дистрофічні зміни у колінному суглобі [11, 12]. Основною причиною кісти меніска є утворення мукоїдної речовини у структурі меніска на фоні його пошкодження, що підтверджено даними магнітно-резонансної томографії (МРТ), спіральної комп’ютерної артрографії (СКТА) та артроскопії. Причому у переважній більшості це горизонтальні або комплексні розриви. Також існує гіпотеза щодо конституційної схильності, а також теорії пухлинного, лімфатичного і дегенеративного походження кіст меніска.
Усі синовіальні порожнини, до яких, зокрема, належать колінний суглоб та бурси, що оточують колінний суглоб, містять синовіальну рідину, яка виробляється внутрішньою синовіальною мембраною та схожа макроскопічно на яєчний білок [1]. Для розуміння патологічних процесів, що можуть відбуватися із бурсами колінного суглоба, необхідно розглянути основні біохімічні характеристики синовіальної рідини.
Синовіальна рідина є ультрафільтратом плазми крові і складається з білків та інтерстиціальної рідини. Основним білком в ультрафільтраті є гіалуронан, або гіалуронова кислота. Нормальна синовіальна рідина містить 3–4 мг/мл гіалуронану [2]. Це полімер, що складається з дисахаридів D-глюкуронової кислоти і D-N-ацетилглюкозаміну, які поєднанні beta 1,4 та beta 1,3 глікозидними зв’язками [3]. Інший важливий білок — любрицин (протеоглюкан 4), який синтезують хондроцити суглобового хряща [4].
Ця рідина формує тонкий шар (приблизно 50 нм) на поверхні суглобового хряща та заповнює його мікропорожнини та нерівності [5]. Під час рухів у колінному суглобі синовіальна рідина діє на поверхні суглобового хряща як лубрикант. У нормі у колінному суглобі знаходиться до 3,5 мл синовіальної рідини. Вона характеризується високою в’язкістю, є прозорою та солом’яного кольору. Вміст лейкоцитів та еритроцитів — до 2 • 109/л, полісахаридів — до 25 %. До основних функцій синовіальної рідини належать: 1) зменшення тертя; 2) амортизаційна функція [6]; 3) транспортування поживних речовин до суглобового хряща та продуктів метаболізму назад у венозне кров’яне русло; 4) молекулярне просіювання. Парціальний тиск, що чинить гіалуронан у рідині на синовіальну мембрану у суглобі, утворює вибірковий бар’єр проти певних клітин, які мігрують у порожнину колінного суглоба. Ця функція залежить від молекулярної маси гіалуронану [7].
Описані бурси, що оточують колінний суглоб, висвітлена класифікація кіст Бейкера, яка заснована на ультразвукових дослідженнях (УЗД) залежно від стадії перебігу [10], та класифікація кістозного переродження меніска, яка включає у себе 3 стадії. Але до цього часу відсутня інформація щодо патофізіологічних змін, які відбуваються у КПУ ділянки колінного суглоба, а також відсутня патофізіологічна та гідростатична модель КПУ ділянки колінного суглоба, яка б відображала природу даного захворювання з точки зору фізико-біохімічних процесів.
Мета дослідження: визначити особливості структурно-функціональних порушень та розробити гідростатичну модель кісти Бейкера.
Матеріали та методи дослідження
У травматологічному відділенні клініки ушкоджень Військово-медичного клінічного центру Північного регіону з початку 2016 року під спостереженням перебувало 15 пацієнтів із клінічної картиною кістоподібного утворення ділянки колінного суглоба, що підтверджено інструментальними методами обстеженнями: УЗД, МРТ та СКТА колінного суглоба. Із них литково-напівперетинчастий бурсит спостерігався у 9 пацієнтів, кісти менісків — у 5 пацієнтів, бурсит переднього відділу колінного суглоба — в 1 пацієнта. Серед пацієнтів було 11 чоловіків та 4 жінки. Середній вік пацієнтів — 43,5 року. Об’єктом дослідження були кістоподібні утворення ділянки колінного суглоба. Пацієнтам із литково-напівперетинчастим бурситом проводилось клінічне обстеження, на підставі якого визначались локалізація, розміри, консистенція та зміни розміру кісти при згинально-розгинальних рухах у колінному суглобі.
УЗД зміненої бурси, зокрема литково-напівперетинчастої, проводили у поздовжньому та поперечному зрізах (рис. 1, 2) на апараті ULTIMAPA L5-10/40E та VOLUSON L5,5-7,5 Mhz/40 mm/128 element фірми Radmir із допплерівським скануванням для обстеження судин підколінної ділянки та виявлення можливих змін з їх сторони, таких як тромбофлебіти, аневризми та інші. Визначали локалізацію КПУ, його форму, розмір, товщину стінки, об’єм внутрішньопросвітних включень та нашарувань, а також наявність поєднання КПУ із порожниною колінного суглоба. При підозрі на внутрішньосуглобову патологію проводились СКТА або МРТ колінного суглоба.
При кістах менісків також проводили їх УЗД для встановлення стадії патологічного процесу. У всіх випадках при параменіскових кістах проводили СКТА або МРТ колінного суглоба. У випадку бурситів переднього відділу колінного суглоба проводили лише УЗД для визначення стадії структурних змін.
На основі проведеного УЗД визначали процентне відношення внутрішньопросвітних включень (нашарувань) до загального розміру кісти за формулою:
де S — площа, що обмежена контуром кісти на скані (зрізі) (рис. 3), SH — площа, що обмежена контуром внутрішньопросвітних нашарувань на даному зрізі (рис. 4).
У результаті досліджень була запропонована нова класифікація структурних змін КПУ ділянки колінного суглоба. До першої стадії відносяться структурні зміни, при яких частка нашарувань (Н) становить від 0 до 25 %, до другої стадії — від 25 до 50 %, до третьої стадії — від 51 до 75 %, до четвертої — від 75 % і більше.
/39_2.jpg)
Наприклад, при поздовжньому скануванні площа, що обмежена контуром кісти, становить 9 см2. При цьому площа, що обмежена контуром внутрішньопросвітних нашарувань, становила 3 см2. Таким чином, частка нашарувань становить 33 %, що відповідає другій стадії структурних змін. При поперечному скануванні площа, що обмежена контуром кісти, становила 6 см2. Площа, що обмежена контуром нашарувань, становила 2,5 см2. У процентному відношенні Н = 42 %, що також відповідає другій стадії морфологічних змін кісти Бейкера. Якщо на поздовжньому і поперечному зрізах мали місце різні стадії структурних змін, то обиралася стадія, що була більш виражена (2-й варіант: стадія визначалась через середнє значення процентної частки нашарувань — Нсер.). Згідно з зазначеною класифікацією хворі розподілялись на 4 групи для вибору того чи іншого методу лікування.
Тиск (мм рт.ст.) у порожнині колінного суглоба та КПУ вимірювали в умовах операційної перед артро-скопією за допомогою контактного манометра фірми Stryker (рис. 5) у положенні згинання та розгинання у колінному суглобі. Тобто у кожного хворого визначали чотири показники тиску: тиск у порожнині колінного суглоба у положенні згинання та розгинання та показники тиску у КПУ. Отриманні результати ультразвукового обстеження та вимірювання тиску наведені у табл. 1.
Після обстеження всім хворим проводилась діагностично-лікувальна артроскопія.
Під час ендоскопії литково-напівперетинчастої бурси, що проводилась через ендоскопічний передньомедіальний трансартикулярний порт та інструментальний задньомедіальний порт після видалення клапанного механізму кісти Бейкера та частини задньої стінки колінного суглоба, спостерігали ніжні нашарування на стінках КПУ із формуванням міжстінкових перетяжок. Ступінь щільності та товщина залежали від стадії патологічного процесу. За допомогою викусувачів та шейверного леза проводили максимальне видалення внутрішньопросвітних нашарувань та включень.
При артроскопії колінного суглоба у хворих із кістою меніска в усіх випадках ми спостерігали жирове переродження тканини меніска у ділянці його пошкодження та у напрямку до параменіскової кісти. Під час артроскопії хворих із параменісковими кістами ми виявили, що кісти зовнішнього меніска розміщуються спереду від зовнішньої колатеральної зв’язки та сухожилка підколінного м’яза, параменіскові кісти внутрішнього меніска — назад від внутрішньої колатеральної зв’язки, що необхідно пам’ятати при внутрішньосуглобовому дренуванні даних кістоподібних утворень.
/41.jpg)
Із фізичної точки зору КПУ являють собою м’яку біологічну оболонку, яка заповнена синовіальною рідиною (рис. 6). Тиск синовіальної рідини призводить до виникнення напруження у стінках КПУ, яке врівноважує його. Для м’яких оболонок найбільш адекватною є безмоментна теорія оболонок, у якій вважається відсутньою жорсткість до деформації згинання, а існує лише жорсткість до деформації розтягнення. Умова рівноваги безмоментної оболонки у найбільш простій формі описується рівнянням Лапласа:
де Р — тиск синовіальної рідини, σm — меридіональне напруження оболонки КПУ, σt — тангенціальне напруження оболонки, R1 та R2 — радіуси кривини оболонки у відповідних напрямках, h — товщина стінки кісти.
Для оціночного аналізу будемо вважати, що радіуси кривини стінки кісти у меридіональному та тангенціальному напрямках приблизно однакові R1 ≈ R2 = R, а також однакові відповідні напруження
σt ≈ σm = σ. Тоді з формули (1) отримуємо співвідношення:
У випадку патологічного процесу при підвищенні тиску Р з рівняння (2) випливає, що зростає механічне напруження σ у стінках кісти. Ми вважаємо, що компенсаторна реакція організму (як біологічної системи) буде спрямована на зменшення механічного напруження. Із рівняння (2) зрозуміло, що це може бути досягнуто за рахунок збільшення товщини оболонки h. Таким чином зростання товщини стінки КПУ під час патологічного процесу є наслідком компенсаторної реакції організму на підвищення тиску синовіальної рідини з метою зменшення механічного напруження у її стінках.
Крім того, на зростання товщини стінки кісти h впливає ще один фактор. Під час патологічного процесу зростає розмір кісти R, що характерно для всіх без винятку кістоподібних утворень. Крім того, під час вимірювання внутрішньокістозного тиску у пацієнтів із кістами Бейкера в усіх випадках спостерігався стійкий підвищений тиск до рівня 28–29 мм рт.ст. у положенні згинання у колінному суглобі. Це означає, що для виконання умови механічної рівноваги (2) збільшення розмірів кісти R при постійному тиску P = const потребує додаткового збільшення товщини стінки h.
Чому утворюються внутрішньопросвітні нашарування або так зване потовщення стінки кісти Бейкера із точки зору біохімічних процесів?
Згідно з даними літератури, основними елементами синовіальної рідини є різні фракції білка та гіалуронова кислота, які формують специфічний компонент складного білка — несульфатований глікозаміноглікан — гіалуронову кислоту (полімер дисахаридних послідовностей ацетильованого аміносахару та уронової кислоти). Відомо, що до складу синовії він входить у вигляді комплексу «гіалуронат — протеїн» та вбудований у поверхню суглобового хряща.
Білки в організмі зберігаються у нативному стані за рахунок факторів стійкості, до яких належить заряд білкової молекули та гідрантна оболонка навколо неї. Зникнення цих факторів, що відбувається при синовіїті колінного суглоба внаслідок запалення та зміни біохімічних характеристик синовіальної рідини, призводить до склеювання молекул білків та випадінню їх в осад із формуванням спочатку пристінкових шарів, а у подальшому міжстінкових перетинок, що призводить до камерності кістоподібного утворення, що має місце на пізніх стадіях захворювання.
Як відомо, осадженню, денатурації та склеюванню білкових молекул сприяють два фактори: підвищення температури та підвищення тиску, що завжди має місце при запаленні у суглобі. Тому при запаленні процеси денатурації та склеювання білкових молекул посилюються, що потрібно пам’ятати та не призначати теплові процедури на ділянку колінного суглоба за наявності кістоподібних утворень.
Крім того, адсорбція призводить до адсорбційного зниження міцності твердого тіла, а у рідинах — до пониження поверхневого натягу (ефект Ребіндера), що може пояснити патогенез розриву кісти на пізніх стадіях.
Результати обстеження та їх обговорення
Після проведеного обстеження встановлено, що середня тривалість захворювання хворих на кісту Бейкера становить 26,4 місяця, на параменіскові кісти — 10,6 місяця. Середній розмір кісти Бейкера, за даними УЗД, становить 56,04 см3. Параменіскові кісти на фоні застарілого пошкодження менісків характеризувались середнім розміром 3,6 см3.
Згідно з запропонованою 4-стадійною ультразвуковою класифікацією, заснованою на прицільному вивчені максимального поздовжнього та поперечного зрізів КПУ, стало відомо, що в обстежуваних хворих переважають кісти Бейкера 2–3-ї стадії структурних змін. Паракапсулярні кісти менісків у хворих зустрічались у 3-й стадії структурних змін.
При розгинанні у колінному суглобі середні показники внутрішньосуглобового тиску становили 58,1 мм рт.ст., при згинанні тиск зменшується майже у два рази і в середньому дорівнює 28,5 мм рт.ст. Тиск у кісті Бейкера вимірювали у положенні розгинання та згинання у колінному суглобі, і середнє значення його становило 29 мм рт.ст. у положенні згинання та 58,4 мм рт.ст. у положенні розгинання.
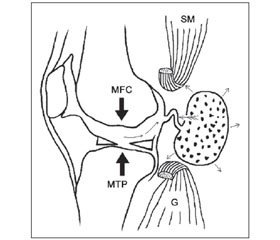
Враховуючи результати обстежень хворих із кістою Бейкера, стало відомо, що внутрішньосуглобовий тиск та тиск у КПУ практично однаковий. Дані факти пояснюються тим, що внутрішні порожнини суглоба та кісти сполучені між собою (устям) каналом (рис. 7), через який, згідно з законом Паскаля, і відбувається гідростатичне вирівнювання тисків.
Зміна тиску при згинанні та розгинанні обумовлена анатомо-фізіологічною будовою колінного суглоба: об’єм порожнини колінного суглоба мінімальний у положенні повного розгинання та максимальний у положенні згинання. Тому і внутрішньосуглобовий тиск буде максимальним у положенні повного розгинання і мінімальним у положенні повного згинання. При цьому рівновага тисків свідчить про достатньо ефективне двостороннє гідростатичне поєднання між суглобом та кістою.
Із цього випливає, що переміщення рідини у будь-які порожнисті структури, які поєднуються із порожниною колінного суглоба, відбувається у положенні максимального розгинання у колінному суглобі, що підтверджується клінічно та інструментально на основі вимірювання внутрішньосуглобового та внутрішньокістозного тиску.
Але така гідростатична рівновага тисків може існувати лише у тому випадку, коли має місце двонаправлений потік рідини через устя КПУ, що відповідає класичній картині кісти Бейкера.
З огляду на існування клапана устя кісти Бейкера у вигляді синовіальної складки або мембрани, що підтверджено численними науковими працями та власними дослідженнями переміщення рідини спочатку має двонаправлений характер. З часом відбувається облітерація устя кісти Бейкера, що призводить до однонаправленого потоку рідини із порожнини суглоба у порожнину КПУ. У цьому разі у КПУ підтримується постійний підвищений тиск на рівні 60 мм рт.ст. та більше. Це пришвидшує процеси випадання в осад білкових молекул із формуванням нашарувань та різного роду включень, а також до розвитку ускладнень перебігу захворювання, включаючи розрив КПУ.
Висновки
Враховуючи дані літератури щодо основних елементів синовіальної рідини, дані ультразвукового обстеження та ендоскопії кіст Бейкера на різних стадіях, ми дослідили, що потовщення стінки кісти відбувається за рахунок пристінкового нашарування білкових молекул із формуванням глобул, які і формують так звану псевдостінку. У подальшому ці нашарування починають формувати перетинки між протилежними стінками, ущільнюватись, що призводить до камерності КПУ. На пізніх стадіях дані нашарування можуть переважати над просвітом КПУ.
На формування та прогресування КПУ має значення підвищений тиск, який становить у середньому 29 мм рт.ст. у положенні згинання та до 58,4 мм рт.ст. у положенні розгинання. Виходячи із попередніх даних, на нашу думку, критичним показником тиску, при якому може настати розрив кісти Бейкера, є тиск більше 60 мм рт.ст. Зазвичай таке ускладнення перебігу КПУ може виникати при тривалому існуванні кісти, коли тривала адсорбція білкових молекул на стінці кісти призводить до адсорбційного зниження міцності та зниження поверхневого натягу (ефект Ребіндера). Але дана теорія потребує подальшого вивчення.
Запропонована нами класифікація відображає основні морфологічні зміни та дає уявлення про стадійність перебігу даного захворювання, це дає можливість визначити оптимальний метод лікування даного кістоподібного утворення та широкого практичного використання у травматології та ортопедії.
Список литературы
1. West Sterling G. Rheumatology secrets. The secrets series. — 3rd ed). — Philadelphia: Elsevier Mosby, 2015. — Р. 19.
2. Hui Alexander Y., McCart William J., Masuda Koichi, Firestein Gary S., Sah Robert L. A Systems Biology Approach to Synovial Joint Lubrication in Health, Injury, and Disease // Systems Biology and Medicine. Wiley Interdisciplinary Reviews. — Jan–Feb 2012. — № 4(1). — Р. 15-7.
3. GlycoForum. Science of Hyaluronan, 15 December 1997.
4. Bennike Tue, Ayturk Ugur, Haslauer Carla M., Froehlich John W., Proffen Benedikt L., Barnaby Omar, Birkelund Svend, Murray Martha M., Warman Matthew L. A Normative Study of the Synovial Fluid Proteome from Healthy Porcine Knee Joints // Journal of Proteome Research. — 2014. — № 13(10).
5. Edwards Jo. Normal Joint Structure. Notes on Rheumato-logy. — University College London. Archived from the ori-ginal on 19 Nov 2012. Retrieved 5 April 2013.
6. Christorpher GF. The role of protein content onthe steady and oscillatory shear rheology of model synovial fluids // Royal Society of Chemistry. — 201. — 10.
7. Sabaratnam S., Arunan V., Coleman P.J., Mason R.M., Levick J.R. Size selectivity ofhyaluronan molecular sieving by extracellular matrix in rabbit synovial joints // The Journal of Physiology. — 2005. — 567 (Pt 2). — Р. 569-81. — doi: 10.1113/jphysiol.2005.
8. Луговец С.Г. Подколенные кисты при ревматических болезнях: диагностика и частота (по данным артросонографии): Автореф. дис… канд. мед. наук. — М., 1998. — 95 с.
9. Макушин В.Д., Чегуров О.К., Камшилов Б.В. Опыт оперативного лечения кисты Backer // Новые технологии в медицине: Тез. докл. науч.-практ. конф. с международ. участием: в 2 ч. — Курган, 2000. — Ч. 1. — С. 186-187.
10. Данилова И.М. Ультрасонографическая диагностика кисты Бейкера при гонартрозе: Автореф. дис… канд. мед. наук. — Курган, 2000. — 115 с.
11. Оперативное лечение синовиальных кист заднего отдела коленного сустава / В.Д. Макушин, О.К. Чегуров, Б.В. Камшилов, И.М. Данилова // Лечение инвалидов с патологией крупных суставов: Тез. докл. — Н.-Новгород, 2002. — С. 105-107.
12. English S., Perret D. Posterior knee pain // Curr. Rev. Musculoskelet. Med. — 2010 Jun 12. — № 3(1–4). — Р. 3-10.
/39.jpg)
/41_2.jpg)
/41_3.jpg)
/42.jpg)

/39_2.jpg)
/40.jpg)
/41.jpg)