Журнал «Актуальная инфектология» 2 (7) 2015
Вернуться к номеру
Препараты, восстанавливающие микробиоценоз, как этиотропная терапия острых кишечных инфекций у детей
Авторы: Ершова И.Б., Мочалова А.А., Осипова Т.Ф., Рещиков В.А., Козина С.Ю. — ГУ «Луганский государственный медицинский университет»
Рубрики: Инфекционные заболевания
Разделы: Справочник специалиста
Версия для печати
В статье рассматриваются вопросы клинической тактики врача при диарее инфекционного генеза. Описана распространенность устойчивых к антимикробным препаратам патогенных микроорганизмов. Показана роль препарата Биоспорин в монотерапии у детей с легкими и среднетяжелыми формами острых кишечных инфекций.
У статті розглядаються питання клінічної тактики лікаря при діареї інфекційного генезу. Описано поширеність стійких до антимікробних препаратів патогенних мікроорганізмів. Показана роль препарату Біоспорин у монотерапії в дітей із легкими та середньотяжкими формами гострих кишкових інфекцій.
This article discusses the issues of clinical approach of the physician in infectious diarrhea. We described the prevalence of germs resistant to antimicrobial agents. The role of Biosporin in monotherapy of children with mild and moderate forms of acute intestinal infections is shown.
острая кишечная инфекция, диагностика, лечение, Биоспорин.
гостра кишкова інфекція, діагностика, лікування, Біоспорин.
acute intestinal infection, diagnosis, treatment, Biosporin.
Статья опубликована на с. 45-50
Термин «острые кишечные инфекции» (ОКИ) собирательный. Несмотря на полиэтиологическое (объединяет более 30 заболеваний бактериальной, вирусной или протозойной этиологии), патогенетическое и клиническое разнообразие, эти инфекции имеют ряд сходных признаков, что позволяет объединить их в одну группу. Среди инфекционной патологии у детей и взрослых ОКИ стойко занимают одно из ведущих мест во всем мире. Проблема усложняется также достаточно высокой смертностью от кишечных инфекций, особенно в раннем детском возрасте. По данным ВОЗ, от острых кишечных инфекций и их осложнений каждую минуту в мире погибает 10 человек. Все это обусловливает дальнейшее усовершенствование этиопатогенетической терапии ОКИ.
С позиций доказательной медицины крайне убедительным является мониторинг ведения пациентов с подозрением на кишечную инфекцию, представленный рекомендациями Американского общества инфекционных болезней [8] (табл. 1).
/45/45.jpg)
Общепринято, что при большинстве кишечных инфекций специфическая антибиотикотерапия не требуется. Особенно если речь идет о секреторной диарее, которая чаще всего вызывается вирусами или простейшими.
Терапия инвазивных диарей требует назначения антибактериальных препаратов, если они могут обеспечить не только клинический, но и бактериологический эффект. Однако использование в последние годы антибиотиков и химиопрепаратов антибактериального действия часто не дает ни клинического, ни санирующего эффекта. Кроме того, при нерациональном их назначении такая терапия может привести к нежелательным последствиям (токсическому поражению различных органов и систем, дисбактериозу кишечника, затяжному течению, развитию эндогенной инфекции и т.д.) [7, 12].
Одной из проблем является распространение устойчивых к антимикробным препаратам патогенных микроорганизмов. Показательно, что растет количество возбудителей, имеющих множественную устойчивость к антибиотикам. При этом заболевание протекает в значительно более тяжелой форме, часто с летальным исходом. Это требует более дорогостоящей и длительной терапии. Причиной такого положения является, с одной стороны, высокая частота необоснованного назначения антибактериальных препаратов (при ОРВИ, дисфункциях желудочно-кишечного тракта, повышении температуры и т.д.), с другой — повышение частоты назначения антибиотиков последних поколений, широкого спектра действия. Следствием этого является распространение бактерий, устойчивых к антибиотикам, массовая аллергизация больных и развитие дисбиотических изменений в организме, частота которых постоянно растет [1].
Все это привело к поиску новых методов и схем лечения ОКИ без использования антибиотиков. Одной из возможностей решения этого вопроса является все более широкое использование биопрепаратов — пробиотиков [3, 5]. Само название «пробиотик» является антонимом слова «антибиотик» и означает «защита жизни». С фармокологической точки зрения под термином «пробиотики» подразумевают препараты из живых микробных культур, используемые для коррекции микрофлоры хозяина, а также для лечения ряда заболеваний. Основоположником концепции пробиотиков является И.И. Мечников, который еще в 1903 году рекомендовал применение микробных культур-антагонистов для борьбы с патогенными бактериями [17, 18].
В отличие от антибиотиков пробиотики не угнетают нормальную микрофлору и в связи с этим получили высокую оценку как препараты для профилактики и лечения дисбактериозов. Биопрепараты широко применяются как для лечения, так и для долечивания острых кишечных инфекций. Немаловажным отличием от антибиотиков, снижающих противоинфекционную резистентность и вызывающих неспецифическую иммуносупрессию, является способность пробиотиков повышать противоинфекционную устойчивость организма, проявлять иммуномодулирующее действие, противоаллергический эффект, а также регулировать и стимулировать пищеварение [9, 15].
Благодаря последним достижениям современной науки врачи практического здравоохранения имеют в своем распоряжении богатый арсенал препаратов этой группы для лечения ОКИ и антибиотикоустойчивых дисбиозов [5].
Важным средством совершенствования биопрепаратов является использование аэробных спорообразующих бактерий рода Bacillus, которые относятся к семейству Bacillaceae. Этот род отличается от других бактериальных организмов высокой устойчивостью благодаря способности образовывать эндоспоры. В организме происходит преобразование спор в вегетативные клетки. При этом происходит активизация ферментов, энергетических и биосинтетических процессов [10].
Спорообразующие бактерии обладают способностью разлагать структурные белковые соединения до аммиака, что стало одной из основных физиологических характеристик этой группы бактерий. Именно таким образом бациллы проявляют антагонистическую активность ко многим патогенным и условно-патогенным микроорганизмам [13].
Большинство бактерий этой группы даже в концентрациях, намного превышающих необходимые для применения, совершенно безвредны для макроорганизма. Они способны значительно стимулировать неспецифические факторы защиты, что активизирует иммунитет в целом и делает многие виды бацилл неоценимыми в борьбе с патогенной флорой. Высокая ферментативная активность позволяет не только стимулировать пищеварение, но и оказывать антитоксическое и противоаллергенное действие [14].
К этому виду бацилл относятся широко распространенные в природе бактерии Bacillus subtilis и licheniformis. Это наиболее древние микроорганизмы, с которыми человек сталкивался на протяжении многовекового сосуществования. Именно эти два вида бактерий, взаимно усиливающих лечебный эффект друг друга, B.subtilis и В.licheniformis, входят в состав пробиотического препарата Биоспорин. Это обусловлено тем, что они дополняют друг друга по спектру антагонистической активности и, что очень важно, не подавляют при этом резидентные микроорганизмы.
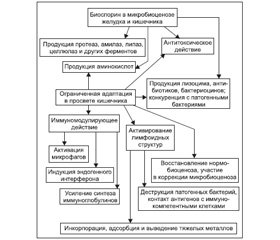
B.subtilis и В.licheniformis оказывают избирательный подавляющий эффект на патогенную микрофлору:
— за счет прямого бактерицидного действия на патогенные и условно-патогенные микроорганизмы;
— продукции ферментов (ряда заменимых и незаменимых аминокислот, витаминов, ферментов: протеиназы, амилазы, липазы, целлюлазы и др.);
— активации защитных реакций (индукции эндогенного интерферона, стимуляции фагоцитарной активности лейкоцитов крови, а также синтеза иммуноглобулинов),
— «популяционного давления» — конкурентного вытеснения патогенных и условно-патогенных бактерий из желудочно-кишечного тракта.
На основе этих бактерий был создан препарат Биоспорин. Разработчиком Биоспорина являются ученые Киевского НИИ микробиологии и вирусологии НАН Украины во главе с академиком В.В. Смирновым [12].
После продолжительных опытов на различных видах животных, а впоследствии — клинических исследований на добровольцах и больных в клиниках мира были созданы рекомендации по использованию Биоспорина как для профилактики, так и для лечения желудочно-кишечных заболеваний, причиной которых в основном являются патогенные и условно-патогенные микроорганизмы. К числу таких заболеваний относятся сальмонеллезы, дизентерия, пищетоксикоинфекции, дисбактериозы, энтероколиты и т.п. [4, 11].
Со временем накопленный опыт использования Биоспорина позволил открывать все новые и новые свойства препарата. Так, удалось установить, что Биоспорин подавляет жизнедеятельность целого ряда микроорганизмов, которые обладают множественной антибиотикорезистентностью (кампилобактер, иерсениа, энтеропатогенная коли, псевдотуберкулезис, кандида, стафилококк). Другие же пробиотики (бактисубтил, энтерогермин, цереобиоген) не оказывали на них антагонистического действия [2, 3].
И хотя Биоспорин, согласно класификации АТС, относится к группе пробиотиков, он имеет принципиальные отличия от них и дополнительные свойства:
— вырабатывает антибиотикоподобные вещества [16];
— обладает высокой антагонистической активностью по отношению к патогенным микроорганизмам, в том числе устойчивым к антибиотикам [18];
— самостоятельно выводится из организма (самоэлиминируется), не колонизирует кишечник [19].
Как следствие, его можно назвать самоэлиминирующимся антагонистом патогенной микрофлоры.
Хотелось бы остановиться еще на одном вопросе. Существует мнение, что пробиотики нельзя принимать одновременно с антибиотиками, так как антибиотики подавляют жизнедеятельность не только патогенных, но и полезных пробиотических микроорганизмов. Чтобы разобраться в этой проблеме, необходимо остановиться на двух ключевых моментах: во-первых, необходимо учитывать чувствительность пробиотиков к антибактериальным препаратам, во-вторых, опираться на клинические данные об эффективности пробиотиков на фоне антибактериальной терапии.
В настоящее время многочисленные микробиологические исследования показывают высокую устойчивость B.subtilis и В.licheniformis к целому ряду антибактериальных препаратов, что делает возможным их назначение с первого дня приема антибиотиков в случаях, когда это необходимо. С учетом широкой распространенности антибиотикоустойчивых патогенов и высокой антибактериальной активности бацилл, входящих в состав Биоспорина, становится понятной целесообразность одновременного (с антибиотиками) назначения данного пробиотика, который сразу действует на антибиотикорезистентные штаммы микроорганизмов, что приводит к облегчению состояния больного и сокращению срока терапии. Тем более если учитывать тот факт, что на практике в большинстве случаев антибактериальные препараты назначаются эмпирически, т.к. микробиологические исследования слишком длительны, а прием антибиотика не терпит отлагательства, и мы не знаем, с каким возбудителем имеем дело. Биоспорин является дополнительной страховкой антибактериальной защиты.
К числу наиболее устойчивых к антибактериальным препаратам бактерий относится золотистый стафилококк. Исследования показали, что Биоспорин эффективен против золотистого стафилококка, препятствует его размножению и росту, вытесняет и выводит из организма. Поэтому совершенно понятным становится необходимость использовать уникальную способность бацилл подавлять развитие стафилококков, в том числе антибиотикоустойчивых.
Литературные данные и практический опыт свидетельствуют о высокой устойчивости к антибиотикам клебсиелл, которые вызывают инфекции дыхательных путей, пиелонефрит, перитонит, ринит, инфекции мочевых путей. Именно поэтому так часто встречаются рецидивирующие бронхиты, хронические пиелонефриты, хронические инфекции урогенитального тракта после лечения антибиотиками. B.subtilis и В.licheniformis являются прямыми конкурентами клебсиелл, угнетают их рост и выводят из организма.
В настоящее время существует целый ряд данных рандомизированных контролируемых исследований и метаанализов, которые подтверждают эффективность профилактического применения пробиотиков на фоне антибактериальной терапии [17].
Именно поэтому анализ клинических исследований показал высокую эффективность Биоспорина при лечении дисбактериозов различной степени тяжести, в том числе с такими сопутствующими заболеваниями, как язвенная болезнь двенадцатиперстной кишки, хронический анацидный гастрит, холецистит и др. [1].
Применение Биоспорина при дисбактериозе у новорожденных детей позволило еще раз убедиться в его безвредности и полностью отказаться от антибиотиков [6].
Успешно применяется Биоспорин и при лечении такого тяжелого заболевания, как неспецифический язвенный колит [4, 19].
Имеются основания для использования Биоспорина в качестве иммуномодулирующего и антиаллергенного средства [16]. B.subtilis и В.licheniformis обладают свойством изменять фенотип Т-хелперов (Th) — с предоминированных Тh2, участвующих в реакциях гуморального иммунитета, на Th1, участвующие в клеточном иммунитете. Именно это делает представителей данной микрофлоры особенно значимыми для реализации защиты организма [12].
/48/48.jpg)
Кратковременный прием Биоспорина в период вакцинации, например вакциной АКДС, повышает титр специфических антител в 2–3 раза [8].
Перспективным представляется использование Биоспорина в борьбе с иерсиниозами, заболеваниями, вызванными микроорганизмами кампилобактер, включая хеликобактер пилори [2, 12]. Последнее обстоятельство является весьма важным, поскольку дает возможность при специфической терапии избегать применения антибиотиков при лечении язвенной болезни желудка и некоторых форм гастритов, при которых в 95–99 % случаев выделяется этот микроорганизм.
Биоспорин (Bacillus subtilis + Bacillus licheniformis) — это препарат, представляющий собой сухую пористую биомассу, которую перед употреблением необходимо развести водой; ампулы содержат по 4–5 млрд микробных тел (для сравнения: в одной капсуле бактисубтила содержится до 1 млрд микробных тел). Препарат начинает действовать уже в ротовой полости, а затем, повторяя природный путь бацилл, охватывает все отделы пищеварительного тракта. Пробиотики же, упакованные в капсулы, начинают действовать лишь в двенадцатиперстной кишке, что значительно ограничивает их терапевтический эффект. В ампуле Биоспорина находятся не только споры бацилл, но и вещества, которые вырабатываются в процессе их роста и размножения (антибиотики, аминокислоты, лизоцим, протеазы, амилазы, липазы и др.). Его терапевтический эффект достигается без фиксации бацилл на слизистой оболочке пищеварительного тракта даже при выраженном диарейном синдроме.
Учитывая, что вегетативные формы препарата Биоспорин (B.subtilis, B.liceniformis) выделяют более 200 антибиотикоподобных веществ, обладающих высокоспецифичной активностью в отношении грамположительных и грамотрицательных кокков и грибов рода Сandida, что делает препарат высокоэффективным средством при ОКИ и диареях неопределенного генеза, целью нашего исследования стало изучение эффективности Биоспорина у детей с острыми кишечными инфекциями в монотерапии.
Материалы и методы
Под нашим наблюдением находились 68 детей с острыми кишечными инфекциями в возрасте от 3 мес. до 14 лет, в комплексной терапии которых в качестве единственного средства этиотропной терапии был использован пробиотик Биоспорин (20 больных) 5–7-дневным курсом. Группами сравнения служили больные ОКИ, получавшие традиционную терапию антибиотиками (20 больных) и химиопрепаратами (28 больных).
Группы больных были сопоставимы по возрасту, тяжести заболевания, топике поражения желудочно-кишечного тракта (энтерит, энтероколит и т.д.) и типу диарейного синдрома (инвазивная, секреторная диарея и др.). Большинство (77,9 %) больных, находившихся под нашим наблюдением, были детьми раннего (41,2 %) и дошкольного (36,7 %) возраста со среднетяжелыми формами кишечной инфекции (38,2 %). Тяжелые формы ОКИ имели место у 3 (4,4 %) больных. Этиологический диагноз ОКИ на основании клинико-эпидемиологических и лабораторных данных (бактериологических и серологических) был установлен у 30,9 % больных (эшерихиоз — у 11, шигеллез Зонне и Флекснера — у 6, сальмонеллез — у 4 больных).
Все больные, независимо от метода и схемы лечения, получали общепринятую базисную терапию (диета, пероральная регидратация, ферменты, симптоматические средства и др.). Из лечения больных, получавших пробиотики, были исключены другие средства этиотропной терапии.
Биоспорин как единственное средство этиотропной терапии был использован нами в комплексной терапии легких (11 детей) и среднетяжелых (8 детей) форм кишечных инфекций (табл. 2).
Эффективность терапии оценивалась по длительности клинических проявлений ОКИ и количеству детей с повторным баквыделением возбудителей.
Статистическая обработка результатов проводилась с использованием программы Statistica 6.0. Значения представлены в виде средней арифметической ± стандартная ошибка среднего (М ± m).
Результаты и обсуждение
Сравнительный анализ клинической эффективности Биоспорина при ОКИ у детей показал, что он является более эффективным при легких и среднетяжелых формах заболевания, чем терапия химиопрепаратами. Средняя продолжительность симптомов интоксикации и эксикоза при лечении Биоспорином составила 3,2 ± 0,5 дня, диарейного синдрома — 4,3 ± 0,4 дня (табл. 3).
На 2–3-й день от начала лечения Биоспорином нормализация частоты и характера стула наступила у 1/3 детей, на 4–5-й — у 70 % больных, в то время как при лечении фуразолидоном — у 0 и 32,0 % больных соответственно. В результате терапии у всех детей наступало клиническое выздоровление. При контрольном бактериологическом обследовании только у 1 ребенка, получающего Биоспорин, наблюдалось выделение возбудителя (Shigella dysenteriae), в то время как в группе получающих химиопрепараты — у 5 детей (у 3 — E.coli, у 1 — Shigella sonnei, у 1 — Salmonella enterica) (табл. 4).
Среди детей, получающих антибактериальную терапию, повторное выделение возбудителей наблюдалось у 2 больных (в обоих случаях — E.coli). Для элиминации возбудителей и профилактики носительства этим детям назначался 10-дневный курс Биоспорина (уже амбулаторно наступающая санация кишечника).
Биоспорин переносился детьми хорошо. При этом ни у одного ребенка мы не наблюдали побочных действий препарата или осложнений.
Полученные результаты позволили сделать следующие выводы:
1. Пробиотик Биоспорин является эффективным этиотропным препаратом в монотерапии у детей с легкими и среднетяжелыми формами острых кишечных инфекций, что подтверждается положительной клинической динамикой и высокой санирующей способностью.
2. Биоспорин может быть альтернативой использования антибиотика у детей с острыми кишечными инфекциями в случаях, когда антибактериальная терапия противопоказана.
3. Применение препарата Биоспорин позволяет уменьшить медикаментозную нагрузку на детей во время терапии ОКИ.
4. Препарат Биоспорин хорошо переносится детьми, без побочных эффектов и осложнений.
1. Андрейчин М.А. Шигельоз / М.А. Андрейчин, В.М. Козько, В.С. Копча. — Тернопіль: Укрмедкнига, 2012. — 362 с.
2. Борщ С.К. Диференційоване використання біоспорину для антагоністичного впливу на грампозитивні бактерії при лікуванні захворювань кишечника / С.К. Борщ // Совр. педиатрия. — 2013. — № 3. — С. 127–131.
3. Борщ С.К. Диференційоване використання пробіотиків для антагоністичного впливу на грампозитивні бактерії у лікуванні кишкових інфекцій і синдрому дизбактеріозу кишечника / С.К. Борщ // Ліки України. — 2008. — № 6. — С. 69–74.
4. Борщ С.К. Застосування Біоспорину та інших пробіотиків для профілактики та лікування кандидозів і синдрому подразненого кишечника / С.К. Борщ, Т.Є. Маковська // Здоровье женщины. — 2013. — № 7. — С. 112–117.
5. Копча В.С. Пробіотики: роздуми з позиції їх якості, ефективності, антибіотикорезистентності й безпеки / В.С. Копча // Вісн. наук. досліджень. — 2011. — № 1 (62). — С. 4–8.
6. Корекція біоспорином порушень мікробіоценозу кишечника у новонароджених дітей / Сорокулова І.Б., Сафронова Л.А., Виноградов В.П. [та ін.] // Перинатол. та педіатрія. — 2003. — № 2. — С. 23–26.
7. Крамарев С.А. Защитные функции микрофлоры кишечника / С.А. Крамарев, О.В. Выговская, Д.С. Янковский, Г.С. Дымент // Здоровье ребенка. — 2008. — № 2. — С. 11.
8. Лобзин Ю.В. Практические рекомендации по ведению пациентов с инфекционной диареей (по материалам рекомендаций Американского общества инфекционных болезней — R.L. Guerrant, T.V. et al. Practice guidelines for the management of infectious diarrhea. Clin. Infect. Dis. 2001; 32: 331–50) / Ю.В. Лобзин, С.Б. Якушин, С.М. Захаренко // Клиническая микробиология и антимикробная химиотерапия. — 2001. — Т. 3, № 2. — С. 163–182.
9. Можина Т.Л. Роль и место пробиотических препаратов в современной медицине (по материалам руководства Probiotics and prebiotics, 2008) / Т.Л. Можина // Суч. гастроентерол. — 2009. — № 1. — С. 5–13.
10. Похиленко В.Д. Пробиотики на основе спорообразующих бактерий и их безопасность / В.Д. Похиленко, В.В. Перелыгин // Химич. и биологич. безопасность. — 2010. — № 2–3. — С. 27–33.
11. Применение Биоспорина при лечении кишечных инфекций / Лигеза К.Н., Чаплинский В.Я., Сорокулова И.Б. [и др.] // Совр. педиатрия. — 2013. — № 5. — С. 1–3.
12. Смирнов В.В. Антибиотики и/или пробиотики: размышления и факты / В.В. Смирнов // Лікування та діагностика. — 2001. — № 3. — С. 8–16.
13. Современные представления о механизмах лечебно-профилактического действия пробиотиков из бактерий рода Bacillus / Смирнов В.В., Резник С.Р., Вьюницкая В.А. [и др.] // Микробиол. журн. — 2003. — Т. 55, № 4. — С. 92–112.
14. Чаплинский В.Я. Биоспорин — эффективный лечебный препарат на основе бацилл / В.Я. Чаплинский // Доктор. — 2004. — № 4. — С. 75–76.
15. Шендеров Б.А. Современное состояние и перспективы развития концепции «Пробиотики, пребиотики и синбиотики» [Электронный ресурс] / Б.А. Шендеров. — Режим доступа: http://www.disbak.ru/php/content.php.id725. — Название с экрана.
16. Katz E. The peptide antibiotics of Bacillus: chemistry, biogenesis and possible functions / T. Katz, A.E. Demain // Bacteriol. Rev. — 1997. — Vol. 41. — P. 449–474.
17. Lebenthal E. Пробиотики: концепция лечебного применения, ожидающая своего признания / E. Lebenthal, Y. Lebenthal // Журн. микробиол., эпидемиол. и иммунобиол. — 2013. — № 4. — С. 88–90.
18. Probiotics: from myth to reality.Demonstration functionality in animal models disease and in humen clinical trials / C. Dunne, L. Murphy, S. Flynn [et al.] // Журн. микробиол., эпидемиол. и иммунобиол. — 1999. — Vol. 76, № 1–4. — P. 279–292.
19. Stein T. Bacillus subtillis antibiotics: structures, syntheses and specific functions / T. Stein // Mol. Microbiol. — 2005. — Vol. 56. — P. 845–857.

/48/48_2.jpg)
/49/49.jpg)