Журнал «Медицина неотложных состояний» 8 (63) 2014
Вернуться к номеру
Диагностика и коррекция мультиорганных нарушений у критических пациентов с геморрагическим инсультом
Авторы: Сериков К.В., Голдовский Б.М., Поталов С.А. — ГУ «Запорожская медицинская академия последипломного образования МЗ Украины»; Светлицкий А.А. — Запорожский государственный медицинский университет; Левкин О.А., Сидь Е.В. — ГУ «Запорожская медицинская академия последипломного образования МЗ Украины»
Рубрики: Медицина неотложных состояний
Разделы: Клинические исследования
Версия для печати
В статье рассмотрены современные представления о концепции мультиорганных повреждений, критериях оценки и методах коррекции. Проведено комплексное обследование и мероприятия интенсивной терапии 25 критическим больным с геморрагическим инсультом (первичным внутримозговым кровоизлиянием). Разработан протокол диагностики и интенсивной терапии мультиорганных повреждений, исходя из выраженности нарушений церебральной, дыхательной и сердечно-сосудистой систем.
У статті розглянуті сучасні уявлення про концепцію мультиорганних ушкоджень, критерії оцінки та методи корекції. Проведено комплексне обстеження та заходи інтенсивної терапії 25 критичним хворим із геморагічним інсультом (первинним внутрішньомозковим крововиливом). Розроблено протокол діагностики та інтенсивної терапії мультиорганних пошкоджень, виходячи з вираженості порушень церебральної, дихальної та серцево-судинної систем.
The article deals with the current understanding of the concept of multiorgan injuries, evaluation criteria and methods of correction. A comprehensive examination and intensive care measures were carried out in 25 critically ill patients with hemorrhagic stroke (primary intracerebral hemorrhage). A protocol for the diagnosis and intensive care for multiorgan injuries were worked out, based on the severity disorders of cerebral, respiratory and cardiovascular systems.
диагностика, мультиорганные нарушения, геморрагический инсульт, интенсивная терапия.
діагностика, мультиорганні порушення, геморагічний інсульт, інтенсивна терапія.
diagnosis, multiorgan disorders, hemorrhagic stroke, intensive care.
Статья опубликована на с. 74-78
Введение
В 1995 году J. Marshall, D. Cook, N. Cristou предложили шкалу для оценки полиорганной дисфункции — Multiple Organ Dysfunction Score, которая включала определение степени дисфункции в системах организма. Первоначально названная мультиорганной системной недостаточностью, теперь в англоязычной литературе она предпочтительно называется синдромом мультиорганной дисфункции (СМОД). Считается, что этот термин лучше описывает изменения органов, происходящие в динамике, а не просто говорит о наличии или отсутствии органной недостаточности [1].
Однако и по сегодняшний день нет единого мнения о том, когда пораженный орган или система имеют нарушенную, но еще удовлетворяющую запросам организма функцию, а когда его можно признать несостоятельным, что связано с надвигающейся гибелью организма [2].
Системная дисфункция рассматривается только применительно к острым патологическим состояниям. Для умирающего вследствие хронического патологического процесса или старости организма более приемлем термин «терминальная висцеропатия», обозначающий необратимую утрату функций в конце жизненного цикла, что принципиально отличается диагностической и лечебной тактикой [3].
Материалы и методы
В условиях отделения анестезиологии с палатами интенсивной терапии (ОАсПИТ) коммунального учреждения «Запорожская городская многопрофильная клиническая больница № 9» проведено комплексное обследование и мероприятия интенсивной терапии 25 критическим больным с геморрагическим инсультом.
Средний возраст больных составил 62 ± 2 года, из них мужчин 14 (56,0 %) — средний возраст 64 ± 3 года; женщин 11 (44 %) — средний возраст 63 ± 4 года.
При этом выздоровевших больных было 18 — средний возраст 64 ± 2 года, из них мужчин 9 (50 %) — средний возраст 65 ± 4 года; женщин 9 (50 %) — средний возраст 64 ± 3 года.
Умерших больных было 7 — средний возраст 60 ± 5 лет, из них мужчин 5 (71,4 %) — средний возраст 62 ± 3 года; женщин 2 (28,6 %) — средний возраст 55 ± 19 лет.
Критерии включения:
1. Больные с первичным внутримозговым кровоизлиянием — код МКБ-10: I61.
Критерии исключения:
1. Больные с субарахноидальным кровоизлиянием — код МКБ-10: I60.
2. Больные с повторным внутримозговым кровоизлиянием — код МКБ-10: I61.
3. Больные с другими нетравматическими кровоизлияниями — код МКБ-10: I62.
4. Больные с ишемическим инсультом — код МКБ-10: I63.
Всем больным проводился неврологический мониторинг тяжести геморрагического инсульта по шкале National Institutes of Health Stroke Scale (NIHSS) [4, 5] (табл. 1).
Наличие мультиорганных повреждений определяли по выраженности нарушений церебральной, дыхательной и сердечно-сосудистой систем (табл. 2).
Динамику нарушений функции центральной нервной системы оценивали по шкале комы Глазго (ШКГ).
В англоязычной литературе нарушение функции дыхательной системы принято определять по отношению парциального давления кислорода в артериальной крови в альвеолах (PaO2) к фракции вдыхаемого кислорода (FiO2) — PaO2/FiO2: Multiple Organ Dysfunction Score (MODS), Sequential Organ Failure Assessment (SOFA), Logistic organ dysfunction (LOG).
При этом необходимо учитывать, что РaО2 не отражает степень насыщения крови кислородом. Значительно более информативным для оценки оксигенации артериальной крови является показатель насыщения кислородом артериальной крови (SaO2) [6].
У больных с геморрагическим инсультом определить тяжесть гемодинамических нарушений исходя из цифр артериального давления вследствие компенсаторной гипертензии представляется затруднительным. Поэтому выраженность нарушений функции сердечно-сосудистой системы оценивали по гемодинамическому профилю.
Результаты и обсуждение
Характеристика тяжести геморрагического инсульта по шкале NIHSS при поступлении больных в ОАсПИТ представлена в табл. 3.
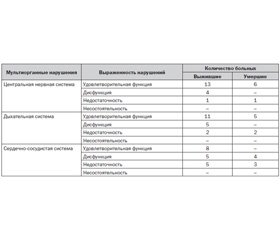
В табл. 4 представлена выраженность мультиорганных нарушений у критических больных с геморрагическим инсультом при поступлении в отделение анестезиологии с палатами интенсивной терапии.
Коррекция мультиорганных нарушений у критических пациентов с геморрагическим инсультом (первичной внутримозговой гематомой) проводилась с учетом унифицированного протокола медицинской помощи больным с геморрагическим инсультом [4].
Коррекция нарушений функции центральной нервной системы
Кровоток в сосудах головного мозга в норме определяется церебральным перфузионным давлением (ЦПД). При его снижении происходит компенсаторная вазодилатация артерий и артериол, что обеспечивает поддержание мозгового кровообращения на оптимальном уровне. Церебральное перфузионное давление в норме составляет 70–100 мм рт.ст., при его снижении возникают метаболические признаки ишемии головного мозга [7, 8].
ЦПД рассчитывается как разница между средним артериальным давлением (САД, мм рт.ст.) и внутричерепным давлением (ВЧД, мм рт.ст.):
ЦПД = САД – ВЧД, мм рт.ст., при этом:
1. При оценке сознания по ШКГ в 14–13 баллов ВЧД составляет 15 мм рт.ст.
2. При уровне сознания по ШКГ в 12–11 баллов ВЧД соответствует 20 мм рт.ст.
3. При оценке сознания по ШКГ в 10–9 баллов ВЧД составляет 25 мм рт.ст.
4. При уровне сознания по ШКГ ≤ 8 баллов ВЧД соответствует 30 мм рт.ст.
Исходя из этого, производится целевая коррекция значений САД с целью поддержания адекватного мозгового кровотока:
САД = ЦПД + ВЧД, мм рт.ст., где:
1. САД = 70 (нижняя граница нормы ЦПД) + 15 = 85 мм рт.ст. — у пациентов с нарушением сознания по типу заторможенности.
2. САД = 70 + 20 = 90 мм рт.ст. — у больных в контактном сопоре.
3. САД = 70 + 25 = 95 мм рт.ст. — у больных в неконтактном сопоре.
4. САД = 70 + 30 мм рт.ст. = 100 мм рт.ст. — у больных в коматозном состоянии.
Коррекция нарушений функции дыхательной системы
Профилактическая оксигенация осуществляется при SaO2 ≤ 94 % увлажненным кислородом со скоростью потока 2–6 литров в минуту (л/мин–1) [4, 5].
При этом уровень фракции вдыхаемого кислорода при спонтанном дыхании зависит от нарушения сознания больных по ШКГ (табл. 5).
1. При уровне сознания по ШКГ 14–13 баллов FiO2 составляет 0,3 %.
2. При оценке сознания по ШКГ 12–11 баллов FiO2 составляет 0,4 %.
3. При уровне сознания по ШКГ 10–9 баллов FiO2 составляет 0,5 %.
4. При сознании по ШКГ 8 баллов, частоте дыхательных движений > 7 или < 30 в минуту, напряжении кислорода в артериальной крови (раО2) > 70 мм рт.ст., напряжении углекислого газа в артериальной крови (раСО2) < 45 мм рт.ст. FiO2 составляет 0,6 %.
В случае нарастания признаков дыхательной недостаточности или дальнейшего нарушения сознания по ШКГ решается вопрос о проведении оротрахеальной интубации и перевода больного на искусственную вентиляцию легких (ИВЛ). При этом достаточно одного из нижеперечисленных факторов [10]:
— уровень сознания по ШКГ < 8 баллов;
— брадипноэ < 7 или тахипноэ > 30 в 1 минуту;
— гипоксемия (раО2 < 70 мм рт.ст.);
— гиперкапния (раСО2 > 45 мм рт.ст.).
Фракция вдыхаемого кислорода при ИВЛ определяется по формуле [9]:
FiO2 = (поток О2 + 0,21 • (МОД – поток О2)) / МОД, %, где:
поток О2 — поток кислорода по ротаметру, л/мин–1; МОД — минутный объем дыхания = масса тела / 10 + 1, л/мин–1.
Коррекция гемодинамических нарушений
Коррекция гипертензии [4]:
— систолическое артериальное давление (АД сист.) > 220 или САД > 150 мм рт.ст. без подозрения на увеличение ВЧД — длительная в/в инфузия гипотензивного препарата с мониторингом АД каждые 5 минут;
— АД сист. > 180 или САД > 130 мм рт.ст. в сочетании с подозрением на повышение ВЧД — мониторинг ВЧД, а также снижение АД до уровня ЦПД ≥ 70 мм рт.ст.
— АД сист. > 180 или САД > 130 мм рт.ст. без подозрения на повышение ВЧД — снижение АД сист. до 160 или САД до 110 мм рт.ст. каждые 15 мин.
Коррекция гипотензии:
— норадреналин в начальной дозе 5 мкг/мин–1, увеличивая дозу до достижения желаемого эффекта:
— 5–10 мкг/мин–1 — преобладающий бета-адреностимулирующий (кардиотонический) эффект;
— > 10 мкг/мин–1 — преобладающий бета-адреностимулирующий (вазотонический) эффект, применяется при ультимативной гипотензии (АД сист. < 70 мм рт.ст.), после ее устранения показано введение дофамина или добутамина [11];
— дофамин 1 мкг/кг–1/мин–1, увеличивая дозу до достижения желаемого эффекта:
— 1–3 мкг/кг–1/мин–1 — дофаминстимулирующий эффект (улучшение перфузии мезентериальных сосудов, почек и миокарда);
— 4–10 мкг/кг–1/мин–1 — преобладающий бета-адреностимулирующий эффект;
— 11–20 мкг/кг–1/мин–1 — сочетанный aльфа- и бета-адреностимулирующий эффект;
— > 20 мкг/кг–1/мин–1 — преобладающий бета-адреностимулирующий эффект;
— добутамин 5 мкг/кг–1/мин–1, увеличивая дозу до достижения желаемого эффекта:
— 5–15 мкг/кг–1/мин–1 — нарастающий бета-адреностимулирующий эффект;
— > 15 мкг/кг–1/мин–1 — преобладающий бета-адреностимулирующий эффект;
— адреналин 1 мкг/мин–1, увеличивая дозу до достижения желаемого эффекта:
— 1–4 мкг/мин–1 — бета-адреностимулирующий эффект;
— 5–20 мкг/мин–1 — нарастающий бета-адреностимулирующий эффект;
— > 20 мкг/мин–1 — преобладающий бета-адреностимулирующий эффект.
Выводы
1. У критических больных с геморрагическим инсультом использование шкалы NIHSS позволяет определить тяжесть заболевания, исходя из выраженности неврологической симптоматики.
2. Мониторинг мультиорганных нарушений отражает витальные изменения в организме критических больных с геморрагическим инсультом, что позволяет своевременно скорригировать интенсивную терапию, направленную на стабилизацию жизненно важных функций организма.
1. Александрович Ю.С., Гордеев В.И. Оценочные и прогностические шкалы в медицине критических состояний. — СПб.: ЭЛБИ-СПб., 2010. — 248 с.
2. Шифрин А.Г., Шифрин Г.А. Научные основы интегративной медицины. — Запорожье: Дикое Поле, 1999. — 207 с.
3. Шифрин А.Г., Шифрин Г.А. Медицина биологической целостности организма. — М.: Медицина, 2009. — 224 с.
4. Уніфікований клінічний протокол медичної допомоги та медичної реабілітації — Геморагічний інсульт // Новости медицины и фармации. — 2013. — № 469. — С. 15-50.
5. Guidelines for the Early Management of Patients with Acute Ischemic Stroke: A Guideline for Healthcare Professionals from the American Heart Association / American Stroke Association // Stroke (published online). — January 31, 2013.
6. Марино Л. Пауль. Интенсивная терапия. — М.: ГЭОТАР-Медицина, 1999. — 639 с.
7. Мальцева Л.А., Усенко Л.В. Нейрореаниматология: нейромониторинг, принципы интенсивной терапии, нейрореабилитация. — Днепропетровск: АРТ-ПРЕСС, 2008. — Т. 2. — 278 с.
8. Віничук С.М., Прокопів М.М. Гострий ішемічний інсульт. — К.: Наукова думка, 2006. — 279 с.
9. Корячкин В.А., Страшнов В.И., Чуфаров В.Н. Клинические функциональные и лабораторные тесты в анестезиологии и интенсивной терапии. — Санкт-Петербургское медицинское издательство, 2004. — 304 с.
10. Наказ Міністерства охорони здоров’я України від 01.03.2004 року № 108 «Про удосконалення організації невідкладної нейрохірургічної допомоги».
11. Усенко Л.В., Шифрин Г.А. Интенсивная терапия кровопотери. — 3-е издание, концептуальное и инновационное. — Днепропетровск: Новая идеология, 2007. — 290 с.

/75/75.jpg)
/76/76.jpg)
/77/77.jpg)