Журнал «Травма» Том 15, №4, 2014
Вернуться к номеру
Влияние биокомпозитного материала Остеоматрикс на процессы регенерации костной ткани в условиях эксперимента (иммуногистохимическое исследование)
Авторы: Науменко Л.Ю., Панасюк А.Ф., Кострица К.Ю., Горегляд А.М., Бондаренко А.А., Хороших В.В. - Днепропетровская государственная медицинская академия
Рубрики: Травматология и ортопедия
Разделы: Клинические исследования
Версия для печати
Представлены результаты экспериментального исследования на макро- и микропрепаратах биокомпозитного костного материала Остеоматрикс при замещении дефектов бедренной кости у крыс с применением иммуногистохимического метода и метода световой микроскопии. Динамика исследований — 3 месяца. Изучены иммуногистохимические и гистоморфологические признаки перестройки костных имплантатов, разработана экспериментальная модель трансплантации костных имплантатов на лабораторных животных. Показана информативность иммуногистохимического исследования для объективной оценки скорости ремоделирования костной ткани и ее реакции на имплантат. Этот метод позволяет достоверно идентифицировать остеоиндуктивные протеины, а также количественно оценить их уровень экспрессии.
Наведені результати експериментального дослідження на макро- і мікропрепаратах біокомпозитного кісткового матеріалу Остеоматрикс при заміщенні дефектів стегнової кістки у щурів із застосуванням імуногістохімічного методу та методу світлової мікроскопії. Динаміка досліджень — 3 місяці. Вивчені імуногістохімічні та гістоморфологічні ознаки перебудови кісткових імплантатів, розроблена експериментальна модель трансплантації кісткових імплантатів на лабораторних тваринах. Показана інформативність імуногістохімічного дослідження для об’єктивної оцінки швидкості ремоделювання кісткової тканини та її реакції на імплантат. Цей метод дозволяє вірогідно ідентифікувати остеоіндуктивні протеїни, а також кількісно оцінити їх рівень експресії.
The results of experimental study on the macro- and micropreparations of biocomposite bone graft Osteomatrix when replacing the femoral defects in rats using immunohistochemical method and light microscopy are provided. Dynamics of the researches — 3 months. We have studied immunohistochemical and histomorphological features of restructuring bone implants, developed an experimental model for transplantation of bone implants in laboratory animals. Information value of immunohistochemical study for an objective evaluation of bone remodeling rate and its response to the implant has been demonstrated. This method helps to identify reliably osteoinductive proteins, as well as to quantify level of their expression.
иммуногистохимический метод, остеоиндуктивные протеины, костный имплантат, перестройка имплантата.
імуногістохімічний метод, остеоіндуктивні протеїни, кістковий імплантат, перебудова імплантата.
immunohistochemical method, osteoinductive proteins, bone implant, implant remodeling.
Статья опубликована на с. 66-72
Введение
Необходимость экспериментального исследования заключается в том, что в опыте на животных возможно использование методов, недоступных для клинического применения. К этим методам прежде всего относятся иммуногистохимические и гистоморфологические исследования репарации костной ткани в динамике.
Проблема пластического закрытия дефектов костей различной локализации до настоящего времени остается актуальной. Одной из главных задач является выбор материала для трансплантации. Поиски оптимальных материалов продолжаются и поныне.
Одним из вариантов решения задачи восстановления целостности кости может стать практика использования деминерализованных костных имплантатов.
Трансплантация органо-тканевых участков в пораженной области организма является одной из важных проблем современной медицины. При костной хирургии восстановление должно происходить как за счет специфической структуры и свойств трансплантата или имплантата, так и за счет активации собственных клеточных элементов и усиления регенерации костной ткани в целом [1].
Сегодня в мире существует большое количество разнообразных остеопластических материалов (костных заменителей) для остеосинтеза и остеопластики, применяемых в стоматологии, травматологии, нейрохирургии, ортопедии и челюстно-лицевой хирургии. К наиболее известным в заместительной хирургии относятся коллагены, гидроксиапатиты, биокерамика, декальцинированный костный матрикс и др. Для восстановления дефектов костной ткани (остеосинтез и костная пластика) остеопластические биоматериалы получают, как правило, из костей и/или хряща различных животных и человека. Эти имплантаты в первую очередь должны обладать остеоинтегративными, остео–кондуктивными и остеоиндуктивными свойствами (A.L. Heller, 1994).
По литературным данным, под остеоиндукцией понимают процесс начальной активации клеток-предшественников для формирования костной ткани в процессе регенерации.
Остеокондукция — рост кости на поверхностях имплантата.
Остеоинтеграция — процесс, обеспечивающий клинически бессимптомную жесткую фиксацию биоимплантатов при функциональной нагрузке [1].
Биоимплантаты нашли применение в травматологии и ортопедии при лечении больных с посттравматическими несращениями длинных костей, ложными суставами, доброкачественными опухолями и опухолевидными заболеваниями костей. Костная алло- и ксенопластика является методом выбора при замещении дефектов костей после резекций. Алло- и ксеногенные ткани позволяют добиться положительных результатов в пластике сухожилий и связочного аппарата. Созданы и совершенствуются технологии получения имплантатов, разрабатываются клеточные технологии, изучаются возможности костных морфогенетических белков в перспективе их использования в травматологии и ортопедии [4].
Ремоделирование костной ткани и ее реакция на имплантат являются сложными процессами, в которых остеобласты и их предшественники играют весомую роль. Поскольку ответ на имплантат в значительной степени зависит от сигнальных клеток, участвующих в регенерации, данное исследование было направлено на изучение биологического влияния исследуемого материала на секрецию остеотропных лигандов и их рецепторов в костной ткани.
В настоящее время известно множество биологически активных веществ белковой природы, которые могут усиливать или, наоборот, подавлять остеогенез и, следовательно, непосредственно участвовать в формировании костной ткани и ее ремоделировании. Иммуногистохимический метод позволяет не только достоверно идентифицировать такие протеины, но и давать количественную оценку их уровня экспрессии. С учетом функциональной значимости и коммерческой доступности антител для исследования было отобрано несколько таких маркеров: остеокальцин, остеопонтин, ВМР-2 (bone morphogenetic protein-2) и VEGFR (рецептор сосудисто-эндотелиального роста) [1–4].
Цель исследования — изучить эффективность, биосовместимость и динамику перестройки костно-пластического материала Остеоматрикс при замещении дефекта бедренной кости у крыс.
Задачи исследования:
1) разработать экспериментальную модель трансплантации костных имплантатов на лабораторных животных;
2) изучить результаты экспериментального исследования на макро- и микропрепаратах костного материала при замещении дефектов бедренной кости у крыс, применив иммуногистохимический метод и метод световой микроскопии.
Материалы и методы
Экспериментальной моделью изучения свойств биокомпозитного материала Остеоматрикс является имплантация его в костный дефект бедренной кости крысы инъекционным путем и гистоморфологическое исследование полученного материала в различные сроки после операции.
Группе беспородных крыс (20 шт.) массой 200–300 г проводили пластику костного дефекта, образованного на уровне большого вертела бедренной кости. Для наркоза использовался 1% раствор тиопентала натрия, который вводили внутрибрюшинно из расчета 1 мл на 1 кг массы тела животного. Животным в межвертельной области бедренной кости создавали костный дефект. Идентичность формы и размера дефектов достигалась путем использования сверла диаметром 2,7 мм. Животным опытной группы дефекты заполняли инъекционным материалом Остеоматрикс, представляющим собой стабильную, не расслаивающуюся суспензию, беспрепятственно проходящую через канюлю. Размер частиц суспензии варьировал от 0,1 до 0,7 мм. В контрольной группе животных дефект ничем не восполняли. Животных выводили из эксперимента на 20-е и 60-е сутки поле операции. На каждый срок использовали по 6 лабораторных животных. Проксимальный фрагмент бедренной кости с имплантатом и без него резецировали, оценивали макроскопически и фиксировали в 10% растворе нейтрального формалина. При исследовании руководствовались Европейской конвенцией относительно защиты позвоночных животных, которые используются с экспериментальными и другими научными целями (Страсбург, 18.03.1986 г.).
Методика эксперимента
Подготовка костной ткани
Для исследования была получена бедренная кость крысы серой (Rattus norvegicus) с окружающими мягкими тканями (мускулатура, фасции), фиксированная в 96% этаноле. Предварительно материал был оценен макроскопически. Дальнейшие манипуляции были произведены в соответствии с разработанной стратегией гистологического исследования костных биоимплантатов, производимых Междисциплинарным исследовательским центром (SFB599) на базе Медицинского университета и Университета ветеринарной медицины г. Ганновера (Германия) [1]. Исследуемая бедренная кость предварительно была препарирована и разделена при помощи циркулярной пилы на пять фрагментов: проксимальный конец бедренной кости, дистальный и три фрагмента, которые включали участок с имплантатом.
Обработка мягких тканей
Мягкие ткани, прилегавшие к участку с имплантатом, были аккуратно отсепарированы от кости, фиксированы в 10% нейтральном формалине, залиты в парафин и порезаны на ротационном микротоме Leica RM2500 (фрагмент МВ). Полученные срезы окрашены гематоксилин-эозином и оценены гистологически.
Декальцинирование и обработка образцов
После промывки в проточной воде (30 мин) фрагменты были помещены на 14 суток в 10% раствор этилендиаминтетраацетата (EDTA, рН 7,0, комнатная температура) для декальцинации. Смена рабочего раствора проводилась ежедневно. Контроль конечной точки декальцинирования производился при помощи рентген-снимков — на 14-е сутки декальцинации очаги минерализации не наблюдались. После промывки в проточной воде (30 мин) кусочки были повторно фиксированы в 10% растворе нейтрального формалина в течение 48 часов, а затем обезвожены и залиты в парафин согласно стандартной методике. Из полученных блоков были изготовлены срезы толщиной 3 мкм.
Гистологические окраски
Все полученные срезы были окрашены гематоксилин-эозином и по методу Массона — Голднера (четырехцветная окраска соединительной ткани). Данная методика окраски позволяет дифференцировать костный матрикс различной степени зрелости. Так, минерализованная кость окрашивается в зеленый цвет, остеоид — в красный. Это позволяет оценить процесс формирования костной ткани и ее ремоделирования.
Иммуногистохимический метод
Для оценки биосовместимости имплантата, его остеоиндуктивных свойств и костного ремоделирования был применен иммуногистохимический метод. Его цель — определение экспрессии маркеров, отражающих процессы ремоделирования в зоне имплантации. В данном исследовании были использованы первичные моноклональные антитела к остеокальцину (клон OCG4, Novus Biologicals), остеопонтину (клон 1B20, Novus Biologicals), ВМР-2 — bone morphogenetic protein-2 (1A11, Sigma Aldrich) и VEGFR — vascular-endothelial growth factor receptor (Flk-1, Thermo Scientific).
Подготовленные срезы были депарафинированы в ксилоле. Блокировка эндогенной пероксидазы проводилась в 80% этаноле с 1 % перекиси водорода в течение 30 мин при комнатной температуре. Демаскировка антигенов производилась при помощи детергента Triton X100 с добавлением EDTA в течение 45 мин при комнатной температуре. После блокировки неспецифической иммунореактивности нормальной козьей сывороткой в течение 20 мин срезы были инкубированы с первичными антителами в течение 12 часов при температуре 4 °С. Были применены следующие разведения: остеокальцин — 1 : 800, остеопонтин — 1 : 400, ВМР-2 — 1 : 1000, VEGFR — 1 : 500. В качестве вторичных антител были использованы антимышиная (к остеокальцину и остеопонтину) и антикроличья (к ВМР-2 и VEGFR) биотинилированные сыворотки. Для визуализации реакции использовался АВС-метод (Vectastain Elite Kit, Vector) с последующей реакцией хромогенного субстрата (DAB Kit, Vector). Продукт реакции визуализировался в виде коричневого окрашивания в участках экспрессии исследуемых маркеров. Позитивный контроль для остеокальцина и остеопонтина проводился на декальцинированной костной ткани кроликов, ВМР-2 — мышей, VEGFR — на биоптате гемангиосаркомы собаки. Для негативного контроля вместо первичных антител были использованы неиммунная мышиная (остеокальцин, остеопонтин) и кроличья (ВМР-2 и VEGFR) сыворотки. Оценивалась как матриксная, так и клеточная экспрессия исследуемых маркеров.
Микроскопия
Микроскопирование препаратов производилось на микроскопе Zeiss AxioLab 4.0 увеличениями x 100, x 200 и x 400. Для анализа и фотографирования изображений была использована программа AxioVision 7.2 для Windows.
Результаты и их обсуждение
Клинически течение послеоперационного периода у животных было без особенностей. Послеоперационные раны зажили первичным натяжением. Гнойно-септических осложнений не отмечалось. Две крысы погибли в первый час после операции, предположительно вследствие передозировки препарата для наркоза.
Макроописание
У крыс опытной группы на 20-е сутки определялось кратерообразное мелкобугристое утолщение костной ткани округлой формы (5 мм) с небольшим (1 мм) углублением посередине, выступающее на 3 мм над поверхностью остальной кости. Консистенция и вид на разрезе соответствовали таковым в нормальной губчатой кости. На остальном протяжении кость имела нормальное анатомическое строение. Прилегающие к утолщению мягкие ткани (мускулатура, надкостница) были плотно спаяны с ним, на разрезе мышечная ткань имела буроватый оттенок. На 60-е сутки наблюдения утолщение кости составляло в среднем 5 мм в диаметре, дефект макроскопически не визуализировался.
В контрольной группе на 20-е сутки дефект был заполнен грубоволокнистой соединительной тканью. Через 2 месяца 2/3 дефекта было заполнено незрелой регенерирующей костной тканью.
Иммуногистохимия
Остеокальцин: была определена негативная реакция антител к данному маркеру, по-видимому, из-за отсутствия их реактивности к протеину крысы.
Остеопонтин: наиболее целесообразно оценивать экспрессию остеопонтина в исследованиях регенерации костной ткани: в остеоиде — для анализа степени резорбции кости (остеопонтин усиливает адгезию остеокластов), в остеобластах — для анализа их активности [7].
На 20-е сутки экспрессия остеопонтина наблюдалась в веществе губчатой кости, остеоиде и остеобластах. Экспрессия в межклеточном матриксе визуализировалась как фокальное окрашивание вдоль волокон в зрелой кости и диффузно — в остеоиде. Кроме того, маркер определялся в клетках костного мозга и фибробластах. Наблюдалась повышенная экспрессия данного маркера в местах активного остеогенеза — в месте имплантации (рис. 2с), а также в участках периостальной реакции в более дистальных отделах диафиза (рис. 1е).
На 60-е сутки слабая экспрессия данного маркера определялась в местах лакунарного остеоида, достоверно не отличаясь от таковой в остальных участках образцов кости оперированной группы, а также контроля. Уменьшение экспрессии остеопонтина на 60-е сутки после имплантации свидетельствует о снижении активности остеобластов, резорбции новообразованной кости и, следовательно, о завершении процесса ремоделирования.
BMP-2 (bone morphogenetic protein-2): оценка экспрессии ВМР-2 позволяет оценить остеоиндуктивные свойства того или иного имплантационного материала, поскольку данный протеин обеспечивает трансформацию мезенхимальных стволовых клеток в преостеобласты, их созревание до остеобластов [4].
В опытной группе на 20-е сутки данный маркер характеризовался экспрессией преимущественно в миелоидной ткани, а также в участках остеогенеза — остеоид, остеобласты, хондроид и хондробласты метафизарной пластинки (рис. 1f, 2в). На 60-е сутки отмечалось значительное снижение экспрессии в месте имплантации, преимущественно в активных остеобластах и в остеоиде. Неактивные остеобласты (клетки выстилающие кость) демонстрировали негативную окраску.
В контрольной группе определялась слабая экспрессия BMP-2 в остеобластах и остеоиде как в раннем, так и в позднем постимплантационном периоде.
Различия уровня экспрессии между опытной и контрольной группой, очевидно, свидетельствует о стимуляции имплантированным костным субстратом клеток-предшественников остеогенеза, то есть о наличии у исследуемого материала остеоиндуктивных свойств.
VEGFR (vascular-endothelial growth factor receptor): на 20-е сутки маркер характеризовался преимущественно клеточной экспрессией. Кроме эндотелиоцитов, фактор роста экспрессировался в остеобластах и хондробластах, а также в незначительном количестве в фиброзной ткани и костном матриксе (рис. 1d, 2а). На 60-e сутки как в опытной группе, так и в контрольной значительных различий в экспрессии VEGFR обнаружено не было.
Окраска на этот маркер позволяет оценивать степень васкуляризации, а также анализировать остеоиндуктивные, остеокондуктивные и остеоинтегративные свойства имплантатов [3]. Полученные результаты показывают, что альтерация экспрессии VEGFR не зависела от наличия имплантата и, следовательно, исследуемый материал, скорее всего, не влияет на ангиогенез в зоне имплантации.
Гистологическое описание
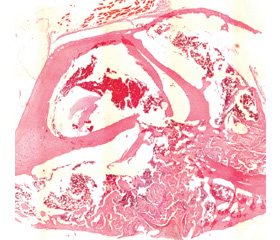
В опытной группе на 20-е сутки в мягких тканях в зоне имплантации определялись очаги кровоизлияний, депозиты гемосидерина, незначительная (до 10 клеток в поле зрения) инфильтрация полиморфноядерными лейкоцитами и фиброз. В местах повреждения кости отмечалось разрастание губчатой костной ткани. Повышенное костеобразование наблюдалось как периостально, так и в костномозговом канале с частичным вытеснением костного мозга в данном участке. Следует отметить значительную периостальную реакцию дистальнее места имплантации, вплоть до дистального эпифиза бедра. Сформированные костные балки располагались беспорядочно (рис. 1, 3).
Межбалочные пространства были заполнены миелоидной тканью. С внутренней поверхности межбалочных пространств располагались в ряд остеобласты призматической формы (активные) и остеокласты. Под этими клетками определялся слой остеоида. Остеоид присутствовал не во всех костных балках. Фрагменты биоимплантата практически не отличались от окружающей костной ткани — васкуляризация, костный матрикс и клеточное строение соответствовало строению компактной кости. Выраженных очагов некроза или воспалительной реакции выявлено не было.
В контрольной группе нами были выявлены некоторые отличия. Так, в месте дефекта часто формировался значительно больший объем грубоволокнистой соединительной ткани и, как следствие этого, снижался объем новообразованной кости.
На 60-е сутки отмечались минимальные изменения в зоне имплантации, характеризовавшиеся небольшим утолщением компактной костной ткани со стороны как периоста, так и эндоста. В то же время в прилегающих мягких тканях наблюдались выраженные процессы фиброза и сохранялись депозиты гемосидерина.
Выводы
1. Ни у одного из оперированных животных реакции отторжения или какой-либо иной местной патологической реакции воспаления обнаружено не было, что говорит о хорошей биосовместимости исследуемого материала.
2. Композитный материал Остеоматрикс, по данным нашего исследования, не оказывает токсического действия на организм животного и положительно влияет на репаративные процессы в костной ткани.
3. По данным иммуногистохимического исследования в динамике от 20 до 60 суток выявлена выраженная тенденция к разрастанию губчатой костной ткани в зоне имплантации Остеоматрикса. Кроме того, имела место хорошая консолидация имплантата с реципиентным ложем с последующей его перестройкой и формированием в месте дефекта новообразованной костной ткани.
4. Иммуногистохимический метод исследования позволяет достоверно идентифицировать остеоиндуктивные протеины, а также давать количественную оценку их уровня экспрессии. Данный метод позволяет более объективно оценивать скорость ремоделирования костной ткани и ее реакцию на имплантат. По нашим данным, после имплантации материла Остеоматрикс он повышает в клетках соединительной ткани синтез BMP-2 и остеопонтина, непосредственно участвующих в формировании костной ткани.
1. Albrektsson T. Osteoinduction, osteoconduktion and osseointegration / T. Albrektsson, C. Jonansson // Eur. Spine J. — 2001. — Vol. 10. — Р. S96-S101.
2. An Y.H. Handbook of histology methods for bone and cartilage / Y.H. An, K.L. Martin. — NY: Humana Press, 2003. — 587 p.
3. Bluteau G. VEGF and VEGF receptors are differentially expressed in chondrocytes / Bluteau G., Julien M., Magne D. // Bone. — 2007. — Vol. 40, № 3. — Р. 568-576.
4. Chen D. // Bone morphogenetic proteins / Chen D., Zhao M., Mundy G.R. // Growth Factors. — 2004. — Vol. 22, № 4. — Р. 233-241.
5. Comparison of the resorbable magnesium alloys LAE442 und MgCa0.8 concerning their mechanical properties, their progress of degradation and the bone-implant-contact after 12 months implantation duration in a rabbit model / Thomann M., Krause C., Bormann D. [еt al.] // Mat.-wiss. und Werkstofftech. — 2009. — Vol. 40. — Р. 82-87.
6. Immunohistochemical, tomographic and histological study on onlay bone graft remodelling. Part II: calvarial bone / Pedrosa Jr. W.F., Okamoto R., Faria P.E.P. [еt al.] // Clin. Oral. Impl. Res. — 2009. — Vol. 20. — Р. 1254-1264.
7. Osteopontin — a possible anchor of osteoclasts to bone / Reinholt F.P., Hultenby K., Oldberg A., Heinegård D. // Proc. Natl. Acad. Sci. U.S.A. — 1990. — Vol. 87, № 12. — Р. 4473-4475.

/70/70.jpg)
/69/69.jpg)
/71/71.jpg)