Журнал «Здоровье ребенка» 4 (55) 2014
Вернуться к номеру
Результати багатоцентрового проспективного дослідження ефективності амінокислотної суміші у дітей грудного віку з тяжким атопічним дерматитом та алергією до білків коров’ячого молока
Авторы: Няньковський С.Л. - Львівський національний медичний університет ім. Данила Галицького; Шадрін О.Г. - ДУ «Інститут педіатрії, акушерства та гінекології АМН України», м. Київ; Клименко В.А. - Харківський національний медичний університет; Добрянський Д.О., Яцула М.С., Івахненко О.С. - Львівський національний медичний університет ім. Данила Галицького; Недельська С.М. - Запорізький державний медичний університет; Кобець Т.В. - Кримський державний медичний університет ім. С.І. Георгієвського, м. Сімферополь; Ащеулов О.М. - Харківський національний медичний університет; Гайдучик Г.А. - ДУ «Інститут педіатрії, акушерства та гінекології АМН України», м. Київ; Пахольчук О.П. - Запорізький державний медичний університет; Гостіщева О.В. - Кримський державний медичний університет ім. С.І. Георгієвського, м. Сімферополь
Рубрики: Педиатрия/Неонатология
Разделы: Клинические исследования
Версия для печати
У статті наведені основні результати багатоцентрового проспективного дослідження ефективності застосування в дієтотерапії амінокислотної суміші у дітей грудного віку з тяжким атопічним дерматитом (АД) та алергією до білків коров’ячого молока (БКМ), що проводилось у 5 центрах України. Під спостереженням знаходились 30 дітей із тяжким атопічним дерматитом (EASI > 18) віком від 29 днів до 11 міс. Закінчили дослідження 22 пацієнти. Лікувальне харчування проводилось амінокислотною сумішшю, що містить 100 % вільних амінокислот, протягом 4 тижнів. Оцінку клінічної ефективності дієтотерапії АД та алергії на БКМ амінокислотною сумішшю здійснювали на 7-му, 14-ту та 28-му добу після досягнення повного об’єму харчування. На 28-й день виконували провокаційну пробу сумішшю зі значним гідролізом сироваткового білка, оцінюючи реакції негайного та сповільненого типу.
Для дітей із тяжким перебігом АД (оцінка за шкалою EASI > 18 балів) було характерне ураження кількох органів і систем: у 68 % випадків шкірні симптоми поєднуються з ураженням шлунково-кишкового тракту у вигляді зміни частоти випорожнень (запори, діарея), появи патологічних домішок у випорожненнях (слиз, кров), блювоти тощо. На тлі застосування амінокислотної суміші відзначено вірогідне зменшення тяжкості не лише ізольованих шкірних (98 %), а і поєднаних шкірно-шлунково-кишкових проявів харчової алергії (82 %).
Амінокислотна суміш добре переноситься дітьми з тяжким АД і може за потреби використовуватися як лікувальна суміш для повного годування малюків із тяжкою формою алергії до БКМ. Тривалість дієтотерапії повинна становити не менше 4 тижнів. Батьками та лікарями ефективність дієтотерапії амінокислотної сумішшю в немовлят з АД оцінена як висока.
В статье приведены основные результаты многоцентрового проспективного исследования эффективности в диетотерапии аминокислотной смеси у детей грудного возраста с тяжелым атопическим дерматитом (АД) и аллергией к белкам коровьего молока (БКМ), которое проводилось в 5 центрах Украины. Под наблюдением находились 30 детей с тяжелым атопическим дерматитом (EASI > 18) в возрасте от 29 дней до 11 мес. Закончили исследование 22 пациента. Лечебное питание проводилось аминокислотной смесью, которая содержит 100 % свободных аминокислот, в течение 4 недель. Оценку клинической эффективности диетотерапии АД и аллергии на БКМ аминокислотной смесью осуществляли на 7, 14 и 28-е сутки после достижения полного объема питания. На 28-й день выполняли провокационную пробу смесью со значительным гидролизом сывороточного белка, оценивая реакции немедленного и замедленного типа.
Для детей с тяжелым течением АД (оценка по шкале EASI > 18 баллов) было характерным поражение нескольких органов и систем: в 68 % случаев кожные симптомы сочетались с поражением желудочно-кишечного тракта в виде изменения частоты стула (запоры, диарея), появления патологических примесей в испражнениях (слизь, кровь), рвоты и т.д. На фоне применения аминокислотной смеси отмечено достоверное уменьшение тяжести не только изолированных кожных (98 %), а и сочетанных кожно-желудочно-кишечных проявлений пищевой аллергии (82 %).
Аминокислотная смесь хорошо переносится детьми с тяжелым АД и может при необходимости использоваться как лечебная смесь для полного кормления детей с тяжелой формой аллергии к БКМ. Продолжительность диетотерапии должна составлять не менее 4 недель. Родителями и врачами эффективность диетотерапии аминокислотной смесью у новорожденных с АД оценена как высокая.
The article presents the main results of prospective multicenter study of effectiveness of using amino acid formula in diet therapy for the infants with severe atopic dermatitis (AD) and allergy to cow''s milk protein (CMP). The study was conducted in 5 centers of Ukraine and included 30 infants with severe atopic dermatitis (EASI score > 18) aged from 29 days to 11 months. 22 patients completed the study. Diet therapy considered administration of amino acid formula containing 100 % free amino acids, for 4 weeks. Evaluation of clinical effectiveness of AD and allergy to CMP diet therapy with amino acid formula was carried out on the 7th, 14th and 28th day after reaching the full daily volume of the formula. Provocative test was performed on the 28th day with extensively hydrolyzed whey protein formula followed with evaluation of immediate and late reactions.
Infants with severe AD (EASI score > 18) were characterized by impairment of several organs and systems: in 68 % of cases skin symptoms were associated with the gastrointestinal signs like change in stool frequency (constipation, diarrhea), appearance of pathological admixtures in feces (mucus, blood), vomiting, and others. With administration of amino acid formula significant decrease in severity of skin (98 %) and gastro-intestinal manifestations of food allergy (82 %) were seen.
Amino acid formula was well tolerated by children with severe AD and, if needed, it might be used as a therapeutic formula for an exclusive feeding of infants with severe allergies to CMP. Duration of the diet therapy should not be less than 4 weeks. High effectiveness of this formula in infants with AD was proved by parents and doctors.
діти, харчова алергія, амінокислотна суміш, атопічний дерматит, дієтотерапія.
дети, пищевая аллергия, аминокислотная смесь, атопический дерматит, диетотерапия.
infants, food allergy, amino acid formula, atopic dermatitis, diet therapy.
Статья опубликована на с. 43-50
В останні роки у дітей відмічається збільшення частоти харчової алергії та пов’язаних із нею алергічних захворювань. Це особливо помітно в розвинутих країнах, у сім’ях із високим соціально-економічним статусом [1]. Практично з грудного віку можуть спостерігатися клінічні прояви алергічних реакцій, що переважно пов’язані з особливостями харчування [2].
Харчова алергія в дітей раннього віку переважно представлена гіперергічною (імунологічною) реакцією на один або декілька білків коров’ячого молока (БКМ) [3]. Її поширеність у дітей першого року точно невідома, орієнтовно вона становить від 2 до 6 % [4–6]. Майже в половини дітей клінічні прояви алергії до БКМ (АБКМ) зменшуються або зникають у кінці першого року, майже у 80 % — протягом перших 3 років життя [7, 8].
За даними Emilia-Romagna робочої групи з алергології та робочої групи з дитячої гастроентерології (EWGPAG), АБКМ зустрічається у 2–6 % дітей, найбільш поширена в дітей першого року життя [6]. Австралійські вчені повідомляють, що 2 % дітей раннього віку мають прояви алергії до БКМ [4]. Згідно з останніми дослідженнями японських учених, поширеність АБКМ становить 0,21 % у новонароджених і 0,35 % у недоношених дітей, які народилися з вагою менше 1000 г [9]. Більшість авторів оцінюють поширеність алергії до БКМ у дітей раннього віку у 5–8 %, у дорослих — 1–2 % [10–12]. За даними американських авторів, серед 28 % дітей раннього віку з імовірними клінічними проявами харчової алергії провокаційна проба підтвердила діагноз АБКМ у 8 % [13].
Епідеміологічні дані щодо поширеності алергії до БМК, яка підтверджена провокаційною пробою, переважно базуються на таких 5 дослідженнях:
1. У Данії, 1749 дітей першого року життя — 2,2 % [14].
2. У Фінляндії, 6209 дітей до 15-місячного віку — 1,9 % [15].
3. У Норвегії, 193 недоношених дитини і 416 доношених дітей у віці до 6 міс. — 4,9 % [16].
4. У Великобританії, 969 дітей першого року життя — 2,16 % [17].
5. У Нідерландах, 1158 дітей першого року життя — 2,24 % [18].
Епідеміологічні дані щодо поширеності АБКМ в Україні вимагають уточнень і проведення відповідних досліджень.
За узагальненими даними, АБКМ клінічно проявляється шкірними симптомами у 5–90 %, гастроінтестинальними симптомами — у 32–60 %, респіраторними симптомами — у 19–30 %, анафілаксією — у 0,8–9 % дітей [19]. Симптоматика варіюється від легкого до середнього та тяжкого ступеня.
Аналіз етіологічного спектра харчової алергії дітей раннього віку свідчить, що БКМ належать до одного з трьох головних алергенів, але в усіх країнах, де проводилось дослідження, БКМ посідають за частотою друге рангове місце після алергенів яйця (DRAGMA, 2010). На третьому місці алергени арахісу (США, Швейцарія), пшениці (Германія, Японія), риби (Іспанія) або кунжуту (Ізраїль).
Але незважаючи на такі «невизначні» місця БКМ у рейтингу поширеності та структури алергії, проблема алергії до БКМ надзвичайна актуальна, і актуальність її обумовлена тим фактом, що в певному віковому періоді розвитку людини (а саме в періоді грудного віку) молоко є тим унікальним продуктом харчування, який неможливо просто елімінувати, як ми елімінуємо причинно-значимий алерген при харчовій алергії іншого генезу або на початку лікування будь-якого іншого алергічного захворювання.
Грудний період характеризується найвищими темпами фізичного та психомоторного розвитку. Такі інтенсивні пластичні процеси потребують відповідного забезпечення енергією, харчовими інгредієнтами, біологічно активними речовинами, потреба в яких найбільша (в перерахунку на 1 кг ваги) порівняно з усіма іншими періодами розвитку дитини.
Цей інтенсивний розвиток відбувається на тлі функціональної незрілості основних ферментативних систем шлунково-кишкового тракту та в умовах еволюційно сформованого виключно лактотрофного харчування. Елімінація молока з харчового раціону дитини грудного віку не проблема, але виникає інше питання: чим годувати дитину? Тільки молоко або молочні продукти містять усі необхідні речовини, і тільки молоко є фізіологічним продуктом для дитини перших місяців життя.
З іншого боку, якщо не елімінувати причинно-значимий алерген, сенсибілізація буде зростати з імовірним формуванням тяжких форм алергічних захворювань. БКМ — це перший харчовий алерген для дітей на штучному вигодовуванні (та дуже частий — при природному вигодовуванні), з яким зустрічається дитина. З алергії до БКМ починається «атопічний марш» з поступовим розширенням спектра сенсибілізації та зміною органа-мішені: атопічний дерматит (АД), бронхіальна астма (БА), алергічний риніт (АР). Від грамотного ведення хворого з першими проявами сенсибілізації залежить не тільки його фізичний розвиток протягом першого року життя, анатомо-фізіологічні властивості всіх органів та систем, але і сценарій атопічного маршу протягом усього життя з можливістю його модифікації та поліпшення прогнозу.
Десятки років науковці працювали над вирішенням проблеми алергії до БКМ у дитини раннього віку. Свідченням цього є не тільки створення нових продуктів — замінників молока на основі гідролізу білка, але й наявність міжнародних консенсусів стосовно проблеми алергії до БКМ. Жодному алергену не було присвячено консенсусу. З іншого боку, створення консенсусів із вирішення проблеми, а не з нозологічних форм (традиційний підхід) свідчить про виняткове, глобальне значення проблеми. Основні консенсуси, що створені на засадах доказової медицини і відображають досягнення у вирішенні існуючої проблеми, — австралійський Management of cow’s milk protein allergy in infants and young children: An expert panel perspective (2009), американський Guidelines for the Diagnosis and Management of Food Allergy in the United States: Report of the NIAID-Sponsored Expert Panel (2010), італійський EWGPAG. Cow’s milk protein allergy in children: a practical guide (2010), Всесвітньої алергологічної організації (World Allergy Organization (WAO)) Diagnosis and Rationale for Action against Cow’s Milk Allergy (DRACMA) Guidelines (2010). Важливо, що в Україні ця проблема також вивчалась, обговорювалась та основні висновки щодо ведення хворих з алергією до БКМ відображені в національних клінічних «Рекомендаціях щодо ведення дітей із харчовою алергією до білка коров’ячого молока», що були затверджені на І відкритому міжнародному конгресі педіатрів-гастроентерологів і нутриціологів України (Львів, 2012) [20].
Рекомендації світових та національних консенсусів єдині: за наявності алергії до БКМ елімінація причинних алергенів обов’язкова, але оптимальною заміною у дітей перших 2 років життя можуть бути тільки суміші на основі екстенсивного гідролізу БКМ та амінокислотні. У більшості випадків суміші, що містять молочні протеїни зі значним гідролізом, є ефективними в лікуванні захворювань з алергією до БКМ у патогенезі. Але в частини хворих ці суміші неефективні — це найбільш тяжко хворі пацієнти з безперервно рецидивним перебігом хвороби, у яких розвиваються імунопатологічні реакції навіть на тлі застосування сумішей зі значним гідролізом протеїну. Для ведення цих пацієнтів у світі вже понад чверть століття рекомендують амінокислотні суміші. Довгий час вони були недоступні українським дітям. Із серпня 2012 р. ситуація змінилась: в Україні була зареєстрована перша амінокислотна суміш (АКС) для вигодовування дітей раннього віку — Nutrilon Аміно.
Стосовно АКС, незважаючи на тривалий термін їх існування на ринку, залишаються невирішеними багато питань як наукового, так і практичного напрямку. У науковому аспекті подальшого вивчення потребує ефективність суміші при тяжких формах АД, бо існують лише одиничні когортні дослідження з цієї проблеми. У практичному аспекті важливо надати лікарям — дитячим алергологам України власний досвід застосування суміші.
Мета дослідження — підвищити ефективність терапії дітей грудного віку, хворих на АД з харчовою алергією до БКМ шляхом раціоналізації елімінаційної дієти.
Завдання дослідження
1. Встановити переносимість та нутритивні якості АКС у дітей грудного віку.
2. Вивчити ефективність АКС в лікуванні тяжких форм АД у дітей грудного віку з алергією до БКМ.
3. Вивчити ефективність АКС в лікуванні гастроінтестинальних проявів харчової алергії до БКМ у дітей грудного віку.
4. Визначити місце АКС у сучасних вітчизняних протоколах лікування дітей з АД та ведення дітей з алергією до БКМ.
Матеріал та методи дослідження
У багатоцентрове проспективне дослідження були включені 30 дітей із тяжким АД на штучному вигодовуванні віком від 29 днів до 11 міс. У 5 дітей (22 %) відзначалась відсутність ефекту від попередньої дієтотерапії з використанням продуктів зі значним гідролізом БКМ. Необхідною умовою залучення пацієнтів у дослідження була тяжкість АД за індексом EASI > 18 балів. Іншими критеріями включення були наявність клініко-анамнестичних даних про алергію дитини на БКМ, а також письмова інформована згода обох батьків на участь дитини в дослідженні. Відповідно критерії виключення: наявність ускладнень АД (бактеріальні, грибкові інфекції шкіри, лімфаденіт тощо), вад розвитку, інших хронічних захворювань (у тому числі первинного імунодефіциту, порушень метаболізму) або будь-якого гострого захворювання; використання під час дослідження будь-яких інших продуктів харчування, крім АКС; потреба призначення системних глюкокортикостероїдів; а також нездатність або небажання батьків виконувати протокол дослідження. Дослідження закінчили 22 дитини. 8 дітей вибуло з дослідження через недотримання умов протоколу.
Дослідження проводилось в 5 центрах України (Київ, Львів, Харків, Запоріжжя, Сімферополь).
Упродовж дослідження всіх дітей годували спеціальною амінокислотною сумішшю Nutrilon Аміно, що складається на 100 % з вільних амінокислот і є сухим продуктом швидкого приготування та призначена для повноцінного дієтичного харчування дітей від народження. Суміш вироблено й упаковано на заводі Nutricia Liverpool/100 Wavertree Boulevard, Wavertree Technology Park, Liverpool L7 9PT (Велика Британія). Імпортер ТОВ з ІІ «Нутриція Україна».
Уводили суміш до харчового раціону кожної дитини поступово, досягаючи 100 % добового об’єму протягом 3 днів. Після цього амінокислотну суміш призначали на 4 тижні в кількості, що відповідала віковим потребам дитини. Оцінку клінічної ефективності лікувального харчування сумішшю АКС здійснювали на 7-му, 14-ту та 28-му добу після досягнення повного об’єму харчування згідно з попередньо визначеними оцінювальними критеріями. На 28-й день виконували провокаційну пробу сумішшю Nutrilon Пепті, що містить значний (екстенсивний) гідроліз сироваткового білка, оцінюючи реакції негайного типу (протягом 2 годин на прийомі у лікаря) та сповільненого типу (через 72 години — на 31-й день).
Протягом дослідження здійснювали шість лікарських оглядів, які передбачали оцінку основних масоростових показників, тяжкості атопічного дерматиту (за індексами EASI і SCORAD), ефективності дієтотерапії за 10-бальною шкалою (зі слів батьків і на думку лікаря), а також результатів провокаційної проби тощо. Ступінь вияву шкірних симптомів АД оцінювали в ділянці максимального ураження.
Батьки оцінювали ефективність дієтотерапії (зникнення шлунково-кишкових симптомів, динаміка тяжкості шкірних симптомів) за 10-бальною шкалою (0 — відсутність ефекту, 10 — відмінний ефект) 1 раз на тиждень. Лікар вносив результат батьківської оцінки у щоденник спостереження за дитиною, що заповнювався під час візиту. Лікарі також паралельно оцінювали ефективність лікування дитини за аналогічною 10-бальною шкалою під час кожного візиту.
Зовнішню терапію тяжкого дерматиту здійснювали за допомогою топічних кортикостероїдних препаратів I–III класу активності відповідно до клінічних показань і вікових обмежень, а також із використанням зволожуючих засобів. Санували вогнища вторинної інфекції. За наявності тяжких загострень і локалізації ураження на шкірі тулуба і кінцівок лікування починали з топічних кортикостероїдних препаратів III класу, для обробки чутливих ділянок шкіри (шия, складки) — I класу. У випадку локалізації ураження на шкірі тулуба і кінцівок використовували топічні кортикостероїди I–II класу. Залучені в дослідження діти з тяжким АД не отримували тривалої системної терапії кортикостероїдами. Антигістамінні засоби застосовували за показаннями.
Для характеристики ознаки за умови нормального розподілу даних використовували середнє значення і його стандартне відхилення (M ± SD); у випадку ненормального розподілу — медіану і значення 25-го і 75-го центилів [25; 75]. Для порівняння бальної оцінки ефективності дієтотерапії в динаміці використовували непараметричний критерій Вілкоксона (двосторонній тест). Статистично значущими вважали відмінності, якщо альфа-помилка була меншою за 5 % (р < 0,05). Для статистичного аналізу використовували статистичну програму Statistica 8 (StatSoft Inc., 2008; США).
Основні результати дослідження
Відповідно до критеріїв залучення у дослідження всі 22 дитини (13 хлопчиків, 9 дівчаток) народилися доношеними, з нормальними масоростовими показниками (середня маса тіла при народженні 3458,640 ± 464,064 г; довжина тіла — 52,14 ± 2,38 см). Оцінка стану всіх дітей за шкалою Апгар була більше ніж 7 балів. Більшість із них (19–86 %) були прикладені до грудей матері в першу годину життя.
Більшість матерів дітей, залучених у дослідження, мали вищу (13–59 %) або незакінчену вищу (3–14 %) освіту. Частки батьків відповідних категорій становили 55 і 5 %. Семеро батьків (32 %) мали середню професійну освіту. Більшість матерів (15–68 %) на момент дослідження перебували в декретній відпустці, 2 (9 %) навчались і 2 (9 %) працювали. Більшість батьків (19–86 %) працювали.
Четверо дітей (18 %) народились від ускладнених вагітностей, перебіг пологів був обтяженим у 3 випадках (14 %), 5 дітей (23 %) народились за допомогою кесарева розтину. У 8 (36 %) матерів і 7 (32 %) батьків був обтяжений алергологічний анамнез, в однієї дитини обоє батьків мали обтяжений алергологічний анамнез. З них 4 (18 %) матері під час вагітності дотримувались елімінаційної дієти. На грудному вигодовуванні діти перебували в середньому протягом 6 [3, 12] днів (табл. 1).
Перші ознаки АД у вигляді змін на шкірі з’явились у середньому віці 4,5 тижня. Дебют АД найчастіше пов’язувався з початком штучного вигодовування (11 випадків — 50 %) або споживанням матір’ю-годувальницею алергенних продуктів (9 випадків — 45 %). У 9 дітей (41 %) наявність алергічного захворювання була підтверджена результатами дослідження специфічного й загального IgЕ (табл. 1).
У більшості випадків захворювання характеризувалося безперервно рецидивним перебігом, недостатньою ефективністю дієтотерапії й інших заходів. До включення у дослідження 5 (22) % дітей як дієтотерапію отримували суміш зі значним гідролізом білка, 10 (45 %) — гіпоалергенну суміш із частковим гідролізом білка, а 7 (33 %) — стандартну суміш. У комплексному лікуванні четверо дітей (18 %) отримували зовнішню гормональну терапію препаратами ІІ класу, а 7 пацієнтів (32 %) — препаратами ІІІ класу активності. Протизапальну терапію препаратами інших груп здійснювали в 7 дітей (32 %). Базисне лікування зволожуючими середниками проводили всім дітям. Більшість дітей отримували також антигістамінні і пробіотичні препарати (16 випадків — 73 %), 17 пацієнтів (77 %) лікувались сорбентами, 10 (45 %) — ферментами, 6 дітей (27 %) отримували гепатопротектори.
Вік дітей на момент включення в дослідження й відповідно призначення амінокислотної суміші становив 5,5 ± 2,3 міс. Середній показник тяжкості АД, оцінений за шкалою EASI, у цей момент дорівнював 34,49 ± 13,59 бала.
Призначення АКС загалом добре переносилось пацієнтами, однак спричинило блювоту в однієї дитини (5 %), супроводжувалось появою симптомів діареї у 5 (23 %), тенденцією до запору — у 8 (36 %), домішками слизу у випорожненнях — у 4 дітей (18 %).
Водночас на тлі дієтотерапії майже у всіх дітей відзначалась позитивна динаміка збільшення маси й довжини тіла (рис. 1). Лише у 3 пацієнтів із дуже тяжкими формами АД упродовж місяця лікування маса тіла збільшилась лише на 50–150 г, а у двох інших довжина тіла зросла на 0,4 см і 0,5 см. Загальні ж середні показники збільшення маси і довжини тіла у групі дітей, які перебували під спостереженням, становили відповідно 500 [300; 700] г і 1,0 [1,0; 3,0] см.
На момент закінчення дослідження жодна дитина не мала дефіциту маси тіла або затримки росту для віку з урахуванням відповідних Z-індексів. Водночас на відміну від Z-індексів для маси тіла, які не змінились або збільшились у всіх, за винятком 1 дитини (рис. 2), Z-індекси для довжини тіла у 9 дітей (41 %) зменшились (рис. 3), хоча їх величини і не вийшли за нормальні межі. Не було встановлено вірогідної кореляції між тяжкістю АД у будь-який момент спостереження за підсумками оцінювання за шкалами EASI/SCORAD і динамікою маси і довжини тіла упродовж дослідження.
Динаміка індексів EASІ і SCORAD на тлі лікувального харчування АКС наведена на рис. 4.
Уже через тиждень після призначення АКС у повному добовому об’ємі спостерігалось вірогідне зниження індексів EASІ (від 32,16 ± 12,6 бала до 14,98 ± 9,92 бала; p = 0,000001) і SCORAD (від 71,23 ± 11,43 бала до 47,086 ± 16,760 бала; р < 0,000001). На момент закінчення 28-денного курсу лікування відповідні показники зменшились до 1,46 ± 1,31 бала і 14,18 ± 6,17 бала (рис. 5, 6).
Окрім ознак ураження шкіри, на початку дослідження у 6 (27 %) дітей були симптоми діареї без підвищення температури тіла, у 5 (23 %) — блювота, у 7 (32 %) — запори й у 8 (36 %) — кишкові кольки. У середньому діти мали за добу випорожнення 2 рази (2 [1; 3]). Принаймні одне із зазначених порушень мали 9 дітей (41 %), а 2 або 3 порушення — по 3 дитини (14 %). Семеро пацієнтів (32 %) не мали шлунково-кишкових розладів.
Після 28 днів призначення АКС у повному добовому об’ємі лише в однієї дитини (5 %) зберігались періодичні блювання (не частіше 2 разів за останній тиждень) і ще у трьох дітей (14 %) продовжували виявлятись ознаки запору. 18 пацієнтів (82 %) не мали шлунково-кишкових розладів.
За підсумками кореляційного аналізу початкова тяжкість АД, визначена в момент досягнення повного добового об’єму харчування АКС за шкалами EASI та SCORAD, вірогідно не асоціювалась із виявом і тяжкістю шлунково-кишкових симптомів. Однак тяжкість АД, визначена за шкалою EASI після 7 днів дієтотерапії, була вірогідно пов’язаною з наявністю й тяжкістю діареї (R = 0,36; p < 0,05) і блювоти (R = 0,48; p < 0,05), а також із батьківськими (R = –0,77; p < 0,05) й лікарськими (R = –0,61; p < 0,05) оцінками ефективності лікування в цей момент. Тяжкість АД, визначена за шкалою SCORAD під час цього ж візиту, вірогідно корелювала з наявністю й тяжкістю запорів (R = 0,43; p < 0,05), блювоти (R = 0,48; p < 0,05), а також із батьківською оцінкою ефективності лікування (R = –0,46; p < 0,05). У дітей із більш тяжким АД після 7 днів дієтотерапії з вірогідно більшою ймовірністю на 28-й день дослідження зберігалась блювота (R = 0,36; p < 0,05), рідше траплялись запори (R = –0,41; p < 0,05) і більш позитивно оцінювалась медичними працівниками ефективність лікування (R = 0,45; p < 0,05).
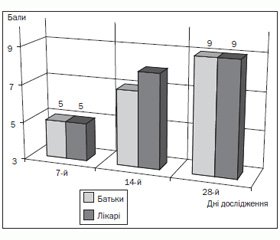
Загальну ефективність дієтотерапії оцінювали батьки і лікарі, використовуючи просту 10-бальну шкалу. На тлі дієтотерапії обидві групи респондентів майже однаково відзначали у дітей явну позитивну динаміку шкірних і шлунково-кишкових симптомів (рис. 7).
/48/48_2.jpg)
Після закінчення курсу дієтотерапії у трьох дітей (14 %) відзначались негайна або сповільнена реакції на провокаційну пробу із сумішшю зі значним гідролізом сироваткового білка протягом 72 год після прийому останньої, що вимагало призначення суміші АКС.
Отримані нами дані узгоджуються з результатами, які були отримані в інших клінічних дослідженнях. Так, у роботі Л.Ф. Казначеєва із співавт. (2013) відзначена висока ефективність суміші на основі амінокислот в терапії АД, викликаного алергією до БКМ. На підставі спостереження за 24 дітьми з тяжкою малюковою формою АД поліпшення у вигляді зниження величини індексу SCORAD і зникнення гастроінтестинальної симптоматики досягнуто у всіх пацієнтів (100 %) протягом 4–14 днів [21].
У роботі А.Н. Пампури та співавт. (2013) була проведена оцінка ефективності амінокислотної суміші в комплексній терапії тяжкого атопічного дерматиту. У багатоцентрове проспективне дослідження було включено 99 хворих дітей віком від 3 до 11 міс. (SCORAD > 40 балів). За даними дослідження, призначення амінокислотної суміші протягом 4 тижнів ефективно зменшує як ізольовані шкірні (у 98 % дітей), так і поєднані шкірно-гастроінтестинальні прояви харчової алергії (у 87 % дітей) [22].
У європейських країнах протягом останніх 25 років накопичений певний досвід застосування амінокислотних сумішей у дієтотерапії дітей раннього віку з алергічними захворюваннями, у тому числі з гастроінтестинальними проявами харчової алергії, непереносимістю молочних сумішей з глибоким гідролізом білка. Позитивний ефект стверджується в роботах J. Vanderhoof et al. (1997), D. Hill et al. (1999, 2000), D. Estep, A. Kulczycki (2000), B. Niggemann et al. (2001) та інших [23–27].
Отримані нами результати та результати інших клінічних досліджень дозволяють рекомендувати включення амінокислотних сумішей у дієтотерапію тяжких форм харчової алергії, у тому числі атопічного дерматиту та гастроінтестинальних розладів у дітей першого року життя в Україні.
Висновок
Проведене дослідження стало першим в Україні дослідженням ефективності амінокислотної суміші у дітей із тяжким АД та алергією до БКМ. Отримані результати дозволяють оптимізувати підходи до комплексного лікування цього небезпечного захворювання в дітей першого року життя на тлі зростаючої неефективності традиційно доступної дієтотерапії сумішами зі значним гідролізом білка.
Для дітей із тяжким перебігом АД (оцінка за шкалою EASI > 18 балів) характерне ураження кількох органів і систем: в 68 % випадків шкірні симптоми поєднуються з ураженням шлунково-кишкового тракту у вигляді зміни частоти випорожнень (запори, діарея), появи патологічних домішок у випорожненнях (слиз, кров), блювоти тощо.
На тлі застосування амінокислотної суміші Nutrilon Аміно, що містить 100 % вільних амінокислот, виявляється вірогідне зменшення тяжкості не лише ізольованих шкірних (98 %), а і поєднаних шкірно-шлунково-кишкових проявів харчової алергії (82 %).
Амінокислотна суміш Nutrilon Аміно добре переноситься дітьми з тяжким АД і може за потреби використовуватися як суміш для повного годування малюків із тяжкою формою алергії до БКМ.
Таким чином, амінокислотні суміші мають застосовуватися при лікуванні тяжких форм АД у дітей з алергією до БКМ. Тривалість дієтотерапії повинна становити не менше 4 тижнів. Батьками та лікарями ефективність дієтотерапії амінокислотної сумішшю в немовлят з АД оцінена як висока.
1. Недельська С.М. Раціональне харчування в профілактиці та лікуванні алергії на їжу у дітей / С.М. Недельська, О.П. Пахольчук, Т.Г. Бессікало // Современная педиатрия. — 2012. — № 6. — С. 113–114.
2. Няньковский С.Л., Кліменко В.А., Івахненко О.С. Харчова алергія на білок коров’ячого молока у дітей раннього віку з позиції лікаря-педіатра // Здоровье ребенка. — 2012. — № 6 (41). — С. 159–166.
3. Hill D.J., Firer M.A., Shelton M.J., Hosking C.S. Manifestations of milk allergy in infancy: clinical and immunologic findings // J. Pediatr. — 1986. — Vol. 109. — Р. 270–276.
4. Allen K. Management of cow’s milk protein allergy in infants and young children: an expert panel perspective / Allen K., Davidson G., Day A., Hill D., Kemp A., Peake J., Prescott S., Shugg A., Sinn J., Heine R. // J. Paediatr. Child. Health. — 2009. — Vol. 45. — P. 481–486.
5. Boyce J. Guidelines for the diagnosis and management of food allergy in the United States: report of the NIAID-sponsored expert panel / Boyce J., Assa’ad A., Burks A., Jones S., Sampson H., Wood R., Plaut M., Cooper S., Fenton M., Arshad S., Bahna S., Beck L., Byrd-Bredbenner C., Camargo C., Eichenfield L., Furuta G., Hanifin J., Jones C., Kraft M., Levy B., Lieberman P., Luccioli S., McCall K., Schneider L., Simon R., Simons F., Teach S., Yawn B., Schwaninger J. // J. Allergy Clin. Immunol. — 2010. — Vol. 126. — S1–58.
6. Caffarelli C. EWGPAG. Cow’s milk protein allergy in children: a practical guide / Caffarelli C., Baldi F., Bendandi B., Calzone L., Marani M., Pasquinelli P. // Ital. J. Pediatr. — 2010. — Vol. 15. — P. 36–45.
7. Wood R.A. The natural history of food allergy // Pediatrics. — 2003. — Vol. 111. — P. 1631–1637.
8. Host A. Clinical course of cow’s milk protein allergy/intolerance and atopic diseases in childhood / Host A., Halken S., Jacobsen H.P., Christensen A.E., Herskind A.M., Plesner K. // Pediatr. Allergy Immunol. — 2002. — Vol. 13. — P. 23–28.
9. Miyazawa T., Itahashi K., Imai T. Management of neonatal cow’s milk allergy in high-risk neonates // Pediatr. Int. — 2009. — Vol. 51. — P. 544–547.
10. Brugman E. / Brugman E., Meulmeester J.F., Speevan der W.A., Beuker R.J., Radder J.J., Verloove-Vanhorick S.P. Prevalence of self-reported food hypersensitivity among school children in The Netherlands // Eur. J. Clin. Nutr. — 1998. — Vol. 52. — P. 577–581.
11. Eggesbo M., Botten G., Halvorsen R., Magnus P. The prevalence of allergy to egg: a population-based study in young children // Allergy. — 2001. — Vol. 56. — P. 403–411.
12. Halmerbauer G. Study on the Prevention of Allergy in Children in Europe (SPACE): Allergic sensitization in children at 1 year of age in a controlled trial of allergen avoidance from birth / Hal-merbauer G., Gartner C., Schierl M., Arshad H., Dean T. // Pediatr. Allergy Immunol. — 2002. — Vol. 13. — P. 47–54.
13. Bock S.A. Prospective appraisal of complaints of adverse reactions to foods in children during the first three years of life // Pediatrics. — 1987. — Vol. 79. — P. 683–688.
14. Höst A. Clinical course of cow’s milk protein allergy/intolerance and atopic diseases in childhood / Höst A., Halken S., Jacobsen H.P., Christensen A.E., Herskind A.M., Plesner K. // Pediatr. Allergy Immunol. — 2002. — Vol. 13(Suppl. 15). — P. 23–28.
15. Saarinen K. Supplementary feeding in maternity hospitals and the risk of cow’s milk allergy: a prospective study of 6209 infants / Saarinen K., Juntunen-Backman K, Järvenpää A., Kuitunen P., Lope L., Renlund M., Siivola M., Savilahti E. // J. Allergy Clin. Immunol. — 1999. — Vol. 104. — P. 457–461.
16. Kvenshagen B, Halvorsen R, Jacobsen M. Adverse reactions to milk i infants // Acta Paediatr. — 2008. — 97. — 196–200.
17. Venter C., Pereira B., Grundy J., Clayton C.B., Roberts G., Higgins B., Dean T. Incidence of parentally reported and clinically diagnosed food hypersensitivity in the first year of life // J. Allergy Clin. Immunol. — 2006. — Vol. 117. — P. 1118–1124.
18. Schrander J., Van Den Bogart J. Cow’s milk protein intolerance i infants under 1 year of age: a prospective epidemiological study // Eur. J. Pediatr. — 1993. — Vol. 152. — P. 640–644.
19. Fiocchi A. World Allergy Organization (WAO) Special Committee on Food Allergy. World Allergy Organization (WAO) Diagnosis and Rationale for Action against Cow’s Milk Allergy (DRACMA) Guidelines / Fiocchi A., Brozek J., Schünemann H., Bahna S.L., von Berg A., Beyer K., Bozzola M., Bradsher J., Compalati E., Ebisawa M., Guzmán M.A., Li H., Heine R.G., Keith P., Lack G., Landi M., Martelli A., Rancé F., Sampson H., Stein A., Terracciano L., Vieths S. // Pediatr. Allergy. Immunol. — 2010. — Vol. 21, Suppl. 21. — P. 1–125.
20. Шадрін О.Г. Рекомендації щодо ведення дітей із харчовою алергією до білка коров’ячого молока / Шадрін О.Г., Няньковський С.Л., Уманець Т.Р., Клименко В.А., Добрянський Д.О., Івахненко О.С., Яцула М.С., Гайдучик Г.А. // Дитячий лікар. — 2012. — № 7. — С. 27–42.
21. Казначеева Л.Ф., Ишкова Н.С., Казначеев К.С., Дубровина Л.Н., Геращенко Н.В. Опыт применения смесей на основе аминокислот у детей с пищевой аллергией // Педиатрия. — 2013. — Том 92, № 4. — С. 92–96.
22. Пампура А.Н. Эффективность аминокислотной смеси при тяжелом атопическом дерматите у детей первого года жизни: результаты открытого многоцентрового проспективного исследования / Пампура А.Н., Лаврова Т.Е., Тренева М.С., Таран Н.Н., Филатова Т.А. // Российский вестник перинатологии и педиатрии. — 2013. — № 1. — С. 93–100.
23. Vanderhoof J.A., Murray N.D., Kaufman S.S. et al. Intolerance to protein hydrolysate infant formulas: an under recognized cause of gastrointestinal symptoms in infants // J. Pediatr. — 1997. — Vol. 131. — P. 741–744.
24. Hill D., Heine R., Cameron D. et al. The natural history of intolerance to soy and extensively hydrolyzed formula in infants with multiple food protein intolerance // J. Pediatr. — 1999. — Vol. 135. — P. 118–121.
25. Estep D., Kulczycki A. Treatment of infant colic with amino acid-based infant formula: a preliminary study // Acta Paediatr. — 2000. — Vol. 89. — P. 22–27.
26. Hill D., Heine R., Cameron D. et al. Role of food protein intolerance in infants with persistent distress attributed to reflux esophagitis // J. Pediatr. — 2000. — Vol. 136. — P. 641–647.
27. Niggemann B., Binder C., Dupont C. et al. Prospective, controlled, multi-center study on the effect of an amino-acid-based formula in infants with cow’s milk allergy/intolerance and atopic dermatitis // Pediatr. Allergy Immunol. — 2001. — Vol. 12. — P. 78–82.

/46/46.jpg)
/47/47.jpg)
/47/47_2.jpg)
/48/48.jpg)