Журнал «Травма» Том 14, №1, 2013
Вернуться к номеру
Локальная терапия в комплексном лечении пациентов старших возрастных групп с болью в нижней части спины
Авторы: Макогончук А.В., Винницкий национальный медицинский университет им. Н.И. Пирогова
Рубрики: Травматология и ортопедия, Неврология, Геронтология
Разделы: Справочник специалиста
Версия для печати
Одним из главных клинических проявлений остеохондроза позвоночника, которое ухудшает функциональные возможности пациента и качество его жизни, является болевой синдром. Применение кетопрофена в виде геля (Фастум гель) в составе комплексного лечения боли в нижней части спины у пациентов старших возрастных групп приводит к уменьшению выраженности болевого синдрома, улучшению функциональных возможностей позвоночника и связанному с этим повышению уровня жизнедеятельности пациентов. Длительное применение локальной терапии в виде противовоспалительных гелей, в частности 2,5% кетопрофена, позволяет эффективно лечить болевой синдром без использования физиотерапевтических методов лечения, которые часто противопоказаны у значительного числа пациентов пожилого возраста, и без риска возникновения осложнений, связанных с системным применением нестероидных противовоспалительных препаратов.
Одним із головних клінічних проявів остеохондрозу хребта, що погіршує функціональні можливості пацієнта і якість його життя, є больовий синдром. Застосування кетопрофену у вигляді гелю (Фастум гель) у складі комплексного лікування болю в нижній частині спини в пацієнтів старших вікових груп призводить до зменшення вираженості больового синдрому, поліпшення функціональних можливостей хребта та пов’язаного з цим підвищення рівня життєдіяльності пацієнтів. Тривале застосування локальної терапії у вигляді протизапальних гелів, зокрема 2,5% кетопрофену, дозволяє ефективно лікувати больовий синдром без використання фізіотерапевтичних методів лікування, які часто протипоказані в значної кількості пацієнтів літнього віку, і без ризику виникнення ускладнень, пов’язаних із системним застосуванням нестероїдних протизапальних препаратів.
One of the major clinical manifestations of osteochondrosis, which impairs the functionality of the patient and the quality of his life, is a pain syndrome. The use of ketoprofen in gel (Fastum gel) in the complex treatment of low back pain in elderly patients leads to a reduction of pain, improvement of the functionality of the spine and the related increase in the level of life of patients. Prolonged use of a local therapy in the form of anti-inflammatory gels, in particular 2.5% ketoprofen, can effectively treat pain syndrome, without the use of physiotherapy treatments, which are often contraindicated in a significant number of elderly patients, and without the risk of complications associated with systemic use of nonsteroidal anti-inflammatory drugs.
остеохондроз, кетопрофен, локальная терапия.
остеохондроз, кетопрофен, локальна терапія.
osteochondrosis, ketoprofen, local therapy.
Остеохондроз позвоночника — одно из самых распространенных заболеваний костномышечной системы. Одним из главных клинических проявлений остеохондроза позвоночника, которое ухудшает функциональные возможности пациента и качество его жизни, является болевой синдром [24]. Под болью в нижней части спины (БНС) подразумевается боль в спине, локализующаяся ниже края реберной дуги и выше ягодичной складки. Она может иррадиировать в ногу. Это, без сомнения, одно из наиболее распространенных патологических состояний, которое является причиной обращения к врачу [4, 5, 13, 21]. Синдром БНС является серьезной медицинской и социальной проблемой. По данным разных исследователей, в США и странах Западной Европы распространенность БНС составляет от 40 до 80 % [5]. Боль длительностью менее 6 недель считается острой, от 6 до 12 недель — подострой, более 12 недель — хронической [10]. Согласно современной классификации American College of Physician and American Pain Society, выделяют три типа боли в нижней части спины: неспецифическую боль, составляющую 85 % всех случаев; боль, ассоциированную с такими патологическими состояниями позвоночника, как спинальный стеноз, компрессионные переломы позвонков и др.; боль, ассоциированную с опухолевыми процессами [7, 21]. Частота и характер неврологических проявлений остеохондроза позвоночника, как правило, не коррелируют с выраженностью дегенеративнодистрофических изменений, а связаны со сложностью взаимоотношений между межпозвоночным диском и нервным корешком (вегетососудистые, реактивновоспалительные и другие факторы) и зависят, конечно, от степени вовлечения в процесс различных нервных и сосудистых структур, расположенных в позвоночном канале [22, 23]. Анализ 31 исследования взаимосвязи изменений, выявляемых при рентгенографии поясничного отдела позвоночника, и острой боли в поясничнокрестцовой области показал, что сужение межпозвоночных промежутков, остеофиты и склероз замыкательных пластинок являются факторами риска скелетномышечной боли в спине (относительный риск 1,2–3,3). Спондилолистез, spina bifida, люмбализация, болезнь Шейермана — Мау не связаны с увеличением частоты боли в поясничнокрестцовой области (степень доказательности А) [19]. Не получено связи между выраженностью дегенеративных изменений позвоночника и трансформацией острой боли в спине в хроническую [12]. Обзор методов диагностической визуализации (рентгенография, МРТ, КТ поясничного отдела позвоночника, сцинтиграфия) показал, что у пациентов моложе 50 лет без признаков серьезной патологии проведение нейровизуализации не оказывает влияния на исход эпизода острой боли в спине. У пациентов старше 50 лет и в случаях подозрения на серьезную вертеброгенную или соматическую патологию нормальные результаты рентгенографии поясничнокрестцового отдела позвоночника и простых лабораторных исследований надежно исключат предполагаемое заболевание [18]. Более углубленные методы визуализации показаны пациентам, которым необходимо нейрохирургическое вмешательство, и тем, у кого после проведенных рутинных методов обследования (рентгенография, лабораторные исследования) сохраняется стойкое подозрение на наличие серьезного заболевания (степень доказательности А) [9]. Европейские клинические рекомендации указывают на нецелесообразность рутинного применения визуализационных методов обследования (рентгенографии, КТ, МРТ) при острой боли поясничнокрестцовой локализации [10].
При анализе первичной обращаемости к врачам общей практики по поводу острой боли в поясничнокрестцовой области вертеброгенные (прямо или косвенно связанные с изменением позвоночника и околопозвоночных структур) причины выявляются у 97 % пациентов. При этом компрессионная радикулопатия поясничнокрестцовых корешков выявляется в 4 %, а неврологические осложнения поясничного стеноза — в 3 % случаев. Нередко обнаруживаются компрессионные переломы тел позвонков, связанные с остеопорозом (4 % обращений), и спондилолистез (2 % случаев) [2, 3]. В подавляющем большинстве случаев острая боль в спине имеет скелетномышечное происхождение, а точный источник болевой импульсации при рутинном клиническом обследовании в ряде случаев выявить не удается. Показано, что микротравматизация и растяжение мышцы при выполнении неподготовленного движения является причиной боли у подавляющего большинства пациентов (> 70 % случаев). Дискогенная боль и боль, связанная с дисфункцией дугоотростчатых (фасеточных) суставов, отмечается у 10 % пациентов с острой болью в спине. В этих случаях для уточнения диагноза требуется проведение дискографии (КТдискографии) и диагностических блокад суставов раствором местного анестетика соответственно. Боль, связанную с указанными выше причинами, в англоязычной литературе принято обозначать термином mechanical low back pain. В тех случаях, когда речь идет о вертеброгенных болевых синдромах без признаков поражения поясничнокрестцовых корешков и специфических изменений позвоночника (спондилолистез, остеопороз), нередко применяется термин «неспецифическая боль в поясничной области», отражающий, с одной стороны, доброкачественность состояния, с другой — трудность точной локализации источника боли без дополнительных инвазивных методов дообследования, применение которых в случаях острой боли в спине не является оправданным. Основными серьезными вертеброгенными причинами боли в спине, которые отмечаются у 1 % пациентов, являются опухоли позвоночника (0,7 % случаев), воспалительные и инфекционные его поражения (0,3 и 0,01 % случаев соответственно). Невертеброгенные, связанные с соматической патологией боли в спине встречаются у 2 % пациентов и обусловлены заболеваниями органов таза (простатит, эндометриоз и т.д.), забрюшинного пространства (аневризма аорты, нефролитиаз, пиелонефрит) и брюшной полости (панкреатит, холецистит, язвенная болезнь двенадцатиперстной кишки) [4, 5].
Диагностический поиск в случае острой боли в спине, согласно современным клиническим рекомендациям, целесообразно проводить: 1) между серьезной патологией вертеброгенного и невертеброгенного происхождения (компрессия конского хвоста, травматическое, опухолевое, воспалительное и инфекционное поражение позвоночника, остеопороз и заболевания внутренних органов); 2) компрессионной радикулопатией поясничнокрестцовых корешков; 3) доброкачественной скелетномышечной (неспецифической) болью в спине [13, 14].
Широкая распространенность остеохондроза позвоночника, полиморфность его клинических проявлений у людей разных возрастных групп обусловливают поиск и изучение новых препаратов для успешного решения этой проблемы [1].
Ведущую роль в существующем арсенале лекарственных средств для лечения БНС играют нестероидные противовоспалительные препараты (НПВП). Это обусловлено их значительным противовоспалительным и анальгезирующим эффектом [2, 3]. Механизм действия НПВП обусловлен угнетением превращения арахидоновой кислоты в простагландины. Сегодня определено, что ведущую роль в этом процессе играет фермент цоклооксигеназа (ЦОГ). Выделены две изоформы ЦОГ — ЦОГ1 и ЦОГ2. ЦОГ1 постоянно присутствует во многих тканях, обеспечивает синтез простагландинов, которые выполняют цитопротекторную функцию, а ЦОГ2
синтезируется только при повреждении тканей, обеспечивая синтез провоспалительных простагландинов, обусловливает развитие воспалительного процесса [16, 20]. Активность ЦОГ1 в слизистой оболочке желудка обеспечивает секрецию бикарбонатов эпителиальными клетками, синтез и секрецию слизи, что защищает стенки желудка и двенадцатиперстной кишки от повреждающего воздействия соляной кислоты [3, 11]. Снижение цитопротекции приводит к различным осложнениям со стороны желудочнокишечного тракта (диспепсия, образование эрозий и язв, кровотечения и перфорации). В настоящее время золотым стандартом среди НПВП признан диклофенак натрия [15, 17], но, к сожалению, он имеет побочные действия вследствие ингибирования циклооксигеназы, что приводит к развитию гастропатий. Особенно актуальна эта проблема у лиц пожилого возраста, у которых, с одной стороны, в несколько раз увеличивается относительный риск язвенного поражения верхних отделов желудочнокишечного тракта вследствие НПВПгастропатии, а с другой — часто отсутствуют клинические проявления, что связано с высоким риском желудочнокишечных кровотечений [8].
Распространенность у пациентов старших возрастных групп заболеваний сердечнососудистой системы, опорнодвигательного аппарата и др. значительно увеличивает частоту полипрагмазии [1]. Следовательно, очень важно взвесить соотношение ожидаемой пользы и возможной опасности в каждом конкретном случае, особенно если боль в нижней части спины не сопровождается другими симптомами, свидетельствующими о заболевании позвоночника или вовлечении в патологический процесс элементов нервной системы. Все вышеуказанное создало предпосылку для поиска новых путей лечения боли в нижней части спины. Одной из возможностей решения этой проблемы является применение местных средств без системного действия [6]. Биодоступность местных НПВП варьирует от 5 до 15 % от той, которая достигается при системном применении. В экспериментальных исследованиях анальгетический эффект местно применяемых НПВП отмечен при боли, связанной с повреждением мышц и кожных покровов [14]. Три обзора, посвященных локальному лечению боли, включавшие анализ 86 исследований и свыше 10 000 пациентов с заболеваниями мягких тканей, ревматологической, скелетномышечной патологией, показали анальгетический эффект НПВП [9]. При местном применении препаратов максимальная концентрация отмечается в дерме, концентрация в прилежащих мышцах сопоставима с таковой после системного применения НПВП. Желудочнокишечные побочные эффекты отмечаются реже, чем при пероральном приеме препаратов; при этом риск их развития выше у тех, у кого они отмечались при системном применении НПВП [14]. При выборе противовоспалительного препарата местного воздействия следует учитывать несколько факторов. Вопервых, в состав должны входить вещества, хорошо зарекомендовавшие себя в лечебной практике: диклофенак натрия, кетопрофен (Фастум гель), ибупрофен, индометацин, бутадион. Вовторых, необходимо учитывать концентрацию действующего вещества в том или ином креме или геле. Большинство известных мазей, кремов и гелей имеют 1% концентрацию действующего вещества, концентрация в препарате Фастум гель — 2,5 %. Втретьих, как и при применении любого терапевтического средства, необходимо назначать оптимальную терапевтическую дозу, обеспечивающую анальгетический и противовоспалительный эффект. Малая концентрация действующего вещества, неполное прохождение препарата непосредственно к очагу воспаления диктуют необходимость многократного нанесения мази или геля на пораженный участок в течение суток. Данные многих клинических испытаний [13, 17, 19] показали, что минимальным является 4кратное нанесение локального средства в день, а при активном воспалении частота нанесения препарата может увеличиваться до 5–6 раз в день. Количество наносимого препарата зависит от величины сустава: на область крупных суставов (коленный, плечевой) однократно следует наносить полоску мази или геля длиной от 5 до 10 см, на область средних по величине суставов (голеностопный, лучезапястный, локтевой) — от 3 до 5 см и на область мелких суставов кистей и стоп — 1–2 см. Необходимо учитывать состояние кожи в области применения средства для локальной терапии. Так, у лиц пожилого возраста проницаемость кожи снижается [4], что указывает на необходимость увеличения как количества наносимого на кожу препарата, так и кратности нанесения. Следует отметить, что наиболее удачной формой для противовоспалительной локальной терапии является гель. Наличие спиртовых растворителей, используемых при приготовлении геля, обеспечивает быстрое впитывание лекарственного средства в кожу. Применение геля является более гигиеничным, чем применение мазей или кремов, экономным, так как максимальное количество наносимого препарата проходит кожный барьер. Кроме того, в состав некоторых гелей входят вещества, обеспечивающие проведение действующего вещества через дерму и подлежащие ткани. Таким препаратом является формуляр 2,5% кетопрофена (Фастум гель).
Целью нашего исследования было изучение эффективности препарата Фастум гель в комплексном лечении боли в нижней части спины у пациентов старших возрастных групп.
Материал и методы исследования
В клинике кафедры травматологии и ортопедии ВНМУ обследовано 20 больных с болью в нижней части спины (средний возраст 60,5 ± 2,4 года), из них 10 больных составили основную группу и 10 больных — контрольную (табл. 1).
Больные основной группы в комплексе с традиционной медикаментозной терапией применяли местно Фастум гель (полоска длиной ≈ 5 см), содержащий 2,5 % кетопрофена, 5 раз в день в течение 21 суток. У больных контрольной группы локальная терапия в лечении не использовалась. И в основной, и в контрольной группе применялись НПВП (диклофенак натрия per os по 100 мг 2 раза в день), сосудистые препараты (актовегин 10 мл в/в капельно № 5 через день, Lлизина эсцинат 5 мл в/в капельно № 5 через день), миорелаксанты (мидокалм 1 мл в/м 1 раз в день 10 дней, потом per os по 150 мг 2 раза в день 11 дней). Из немедикаментозных методов лечения использовали ЛФК (групповые занятия под руководством инструктора). Массаж, мануальная терапия и физиотерапевтическое лечение не проводили изза наличия противопоказаний у пациентов (аритмии, наличие опухолевидных образований).
Состояние больных оценивали трижды: перед лечением, на 11е сутки и 21е сутки после начала лечения. Все пациенты были обследованы согласно плану, приемлемому для ортопедического больного. Наряду с общеклиническими и рентгенологическими исследованиями проводили определения интенсивности болевого синдрома по четирехсоставной визуальной аналоговой шкале боли (ВАШ) и по опроснику МакГилла, использовали опросник Роланда — Морриса «Боль в нижней части спины и нарушения жизнедеятельности, связанные с ним» и опросник Освестри. Кроме того, все пациенты заполняли Европейский опросник качества жизни (EvroQol5D). Функциональное состояние позвоночника оценивали с помощью тестов Томайера, Шобера, амплитуды наклонов вправо и влево.
Результаты и обсуждение
Оценка состояния больных в начале исследования показала однородность групп больных по возрасту, интенсивности болевого синдрома, уровню жизнедеятельности и связанным с этим проявлениям тревожности. В начале лечения составляющие болевого синдрома по опроснику МакГилла у больных основной и контрольной группы были соответственно: дескрипторы — 9,4 ± 1,5 балла и 11,9 ± 1,7 балла, ранги — 17,9 ± 3,1 балла и 22,3 ± 2,9 балла. Уровень тревожности по шкале Цунга составил 29,5 ± 2,3 балла и 22,9 ± 3,7 балла соответственно. Данные по опроснику Освестри в основной и контрольной группах соответствовали следующим значениям: 34,6 ± 1,2 балла и 27,1 ± 3,5 балла, по опроснику Роланда — Морриса: 9,20 ± 1,41 балла и 8,7 ± 1,1 балла.
В процессе лечения на 11е сутки у пациентов основной группы установлено достоверное снижение интенсивности болевого синдрома по показателям опросника МакГилла (рис. 1). У пациентов контрольной группы на 11е сутки отмечалась лишь тенденция к снижению интенсивности болевого синдрома (р = 0,06), а достоверное снижение интенсивности боли наблюдалось лишь через 3 недели от начала лечения (р = 0,01).
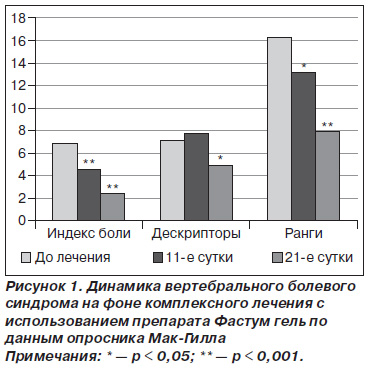
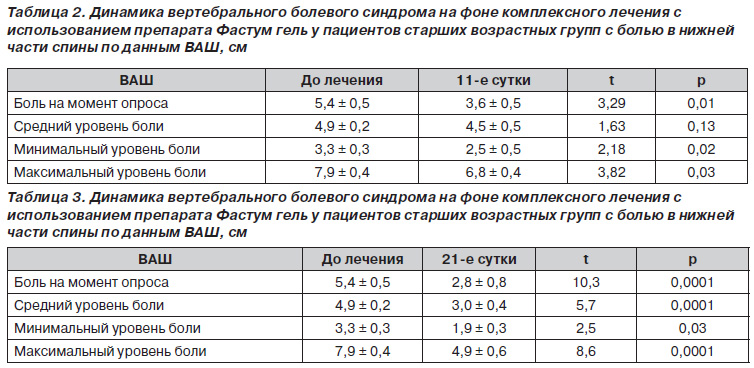
После завершения полного курса комплексного лечения боли в нижней части спины с использованием препарата Фастум гель уже с 11го дня установлено достоверное уменьшение выраженности вертебрального болевого синдрома на момент обследования, минимального и максимального уровня боли — за последние две недели, а также уменьшение выраженности среднего уровня боли в поясничном отделе позвоночника (табл. 2). Достоверный анальгезирующий эффект сохранялся и под влиянием дальнейшего использования препарата (табл. 3).
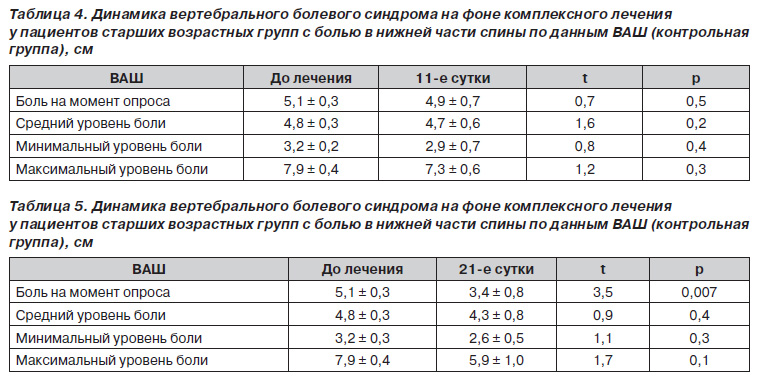
У пациентов контрольной группы на 11е сутки наблюдалась тенденция к уменьшению интенсивности болевого синдрома (табл. 4), а статистически достоверное снижение интенсивности боли отмечалось только через 3 недели с момента начала лечения (табл. 5).
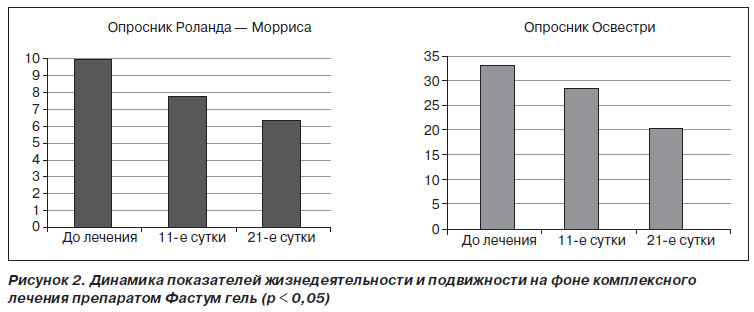
Установлено достоверное улучшение жизнедеятельности и увеличение двигательного режима по опросникам Роланда — Морриса и Освестри у пациентов старшего возраста с болью в нижней части спины, что обусловлено уменьшением выраженности болевого синдрома (рис. 2).
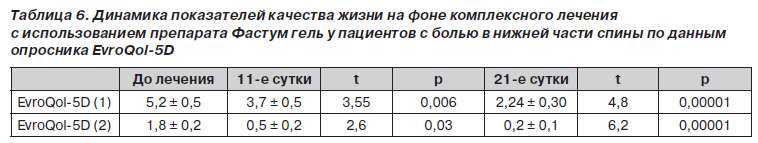
По результатам сравнения уровня общего состояния и жизненной активности пациентов основной группы наблюдалось достоверное улучшение состояния пациентов уже с 11го дня с момента лечения и оставалось достоверно стабильным вплоть до окончания проводимой терапии (табл. 6).
По результатам сравнения уровня общего состояния и жизненной активности пациентов старших возрастных групп до и после лечения отмечена тенденция к улучшению показателей опросников Цунга (25,5 ± 2,7 балла и 23,6 ± 2,7 балла соответственно, t = 1,36, р = 0,20) и EvroQol5D (6,1 ± 0,4 балла и 5,3 ± 0,5 балла соответственно, t = 1,74, р = 0,11).
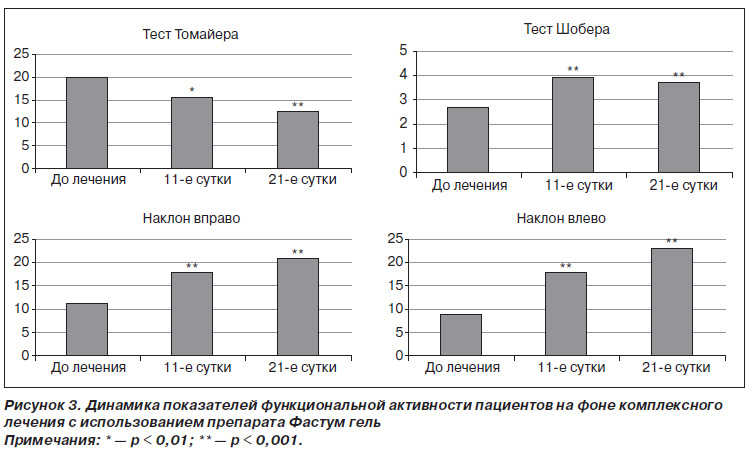
Параллельно с улучшением качества жизни у пациентов основной группы наблюдалось достоверное улучшение функционального состояния позвоночника (рис. 3).
За период наблюдения у больных как основной, так и контрольной группы не наблюдалось побочных эффектов, связанных с приемом препаратов.
Выводы
Таким образом, применение препарата Фастум гель в составе комплексного лечения боли в нижней части спины у пациентов старших возрастных групп приводит к уменьшению выраженности болевого синдрома, улучшению функциональных возможностей позвоночника и связанному с этим повышению уровня жизнедеятельности пациентов. Длительное применение локальной терапии в виде противовоспалительных гелей, в частности препарата Фастум гель, позволяет эффективно лечить болевой синдром без использования физиотерапевтических методов лечения. Это особенно важно у пациентов старших возрастных групп, которые в основном имеют если не противопоказания к физиотерапии, то как минимум увеличенный риск развития побочных эффектов от данного метода лечения.
- Ананьева Л.П., Подчуфарова Е.В. Современные противоболевые средства в аптеке. — М.: МЦФЭР, 2005. — 157 с.
- Бадокин В.В. Вольтарен как эталон НПВП в современной ревматологии // Русский медицинский журнал. — 2007. — T. 15, № 5. — C. 335340.
- Балабанова Р.М. Нимесулид — противовоспалительный препарат с селективным ингибированием ЦОГ2 //
- Русский медицинский журнал. — 2001. — T. 9, № 7–8. — C. 291294.
- Поворознюк В.В. Захворювання кістковом’язової системи у людей різного віку (вибрані лекції, огляди, статті). — К., 2004. — 519 с.
- Поворознюк В.В., Литвин В.О., Орлик Т.В. Боль в нижней части спины // Доктор. — 2003. — № 1. — С. 3137.
- Силин Л.Л., Бровкин С.В. Применение гелей в комплексном лечении закрытых повреждений мягких тканей // Медицинская помощь. — 2001. — № 2.
- Сhou R., Huffman L.H. Medications for acute and chronic low back pain: a review of the evidence for an American Pain Society/American College of Physicians clinical practice guideline // Ann. Intern. Med. — 2007. — 147(7). — 50514.
- Garcia Rodriguez L.A., Jick H. Risk of upper gastrointestinal bleeding and perforation associated with individual nonsteroidal antiinflammatory drugs // Lancet. — 1994. — V. 343. — P. 769772.
- Griffin G. Cochrane for clinicians: putting evidence into practice: do NSAIDs help in acute or chronic low back pain? // American Family Physician. — 2002. — Vol. 65, № 7. — P. 13191321.
- Harwood M.I., Smith B.J. Low Back Pain: A Primary Care Approach // Clinics in Family Practice. — 2005. — Vol. 7, № 2. — P. 279303.
- Innes G.D., Croskerry P., Worthington J., Beveridge R., Jones D. Ketorolac Versus AcetaminophenCodeine in the Emergency Department Treatment of Acute Low Back Pain // J. Emerg. Med. — 1998. — 16(4). — P. 549556.
- Kinkade S. Evaluation and Treatment of Acute Low Back Pain // American Family Physician. — 2007. — Vol. 75, № 8. — P. 11811188.
- Koleck M., Mazaux J.M., Rascle N. et al. Psychosocial factors and coping strategies as predictors of chronic evolution and quality of life in patients with low back pain: A prospective study // European Journal of Pain. — 2006. — Vol. 10. — P. 111.
- McCleane G. Topical analgesics // Medical Clinics of North America. — 2007. — Vol. 91, № 1. — P. 125139.
- Omololu B., Alonge T.O., Ogunlade S.O. et al. Double blind clinical trial comparing the safety and efficacy of nimesulide (100 mg) and diclofenac in osteoarthrosis of the hip and knee joints // West. Afr. J. Med. — 2005. — Vol. 24, № 2. — P. 128133.
- Pohjolainen T., Jekunen A., Autio L. et al. Treatment of acute low back pain with the COX2selective antiinflammatory drug nimesulide: results of a randomized, doubleblind comparative trial versus ibuprofen // Spine. — 2000. — Vol. 25, № 12. — P.15791585.
- Predel H.G., Koll R., Pabst H., Dieter R., Gallacchi G., Giannetti B., Bulitta M., Heidecker J.L., Mueller E.A. Diclofenac patch for topical treatment of acute impact injuries: a randomised, doubleblind, placebocontrolled, multicentre study // British Journal of Sports Medicine. — June 2004. — 38(3). — P. 318323.
- Rossignol M., Arsenault B., Dione C. et al. Clinic in low back pain in interdisciplinary practice (CLIP) guidelines. — 2007. — Direction de sante publique, Agence de la sante et des services sociaux de Montreal, Montreal. — 41 р.
- Schnitzer T.J., Ferraro A., Hunsche E. et al. A comprehensive review of clinical trials on the efficacy and safety of drugs for the treatment of low back pain // J. Pain Symptom Manage. — 2004. — Vol. 28. — P. 7295.
- Tassorelli C., Greco R., Sandrini G. et al. Central components of the analgesic/antihyperalgesic effect of nimesulide: studies in animal models of pain and hyperalgesia // Drugs. — 2003. — Vol. 63 (Suppl. 1). — P. 922.
- Van Tulder M., Becker А., Bekkering T. et al. European guidelines for the management of acute nonspecific low back pain in primary care // Eur. Spine J. — 2006. — Vol. 15 (suppl. 2). — S. 169191.
- Waddell G. The Back Pain Revolution / Еd. by G. Waddell. — 2nd ed. — Elsevier Edinburgh, 2004. — P. 221239.
- Wanek V., Brenner H., Novak P., Reime B. Back pain in industry: prevalence, correlation with the work conditions and requests for reassignment by employees // Gesundheitswesen. — 1998. — 60(8–9). — P. 513522.
- Williams D.A., Feuerstein M., Durbin D., Pezzullo J. Healthcare and indemnity costs across the natural history of disability in occupational low back pain // Spine. — 1998. — 23. — P. 23292336.