Журнал «Здоровье ребенка» 3 (38) 2012
Вернуться к номеру
Место цефалоспориновых антибиотиков в лечении инфекций мочевой системы у детей
Рубрики: Педиатрия/Неонатология
Разделы: Медицинские форумы
Версия для печати
5–6 апреля 2012 г. в г. Одессе состоялась научно-практическая конференция с международным участием, посвященная памяти академика НАМН Украины Б.Я. Резника. На конференции было рассмотрено множество вопросов, в том числе и проблемы антибактериальной терапии.
Один из докладов заведующего кафедрой госпитальной педиатрии Запорожского национального медицинского университета Геннадия Александровича Леженко был посвящен месту пероральных цефалоспоринов в лечении инфекций мочевой системы (ИМС). Докладчик отметил, что проблема антибактериальной терапии на сегодняшний день стоит очень остро, так как антибиотики используются нерационально. Данные ВОЗ говорят о том, что только 25–50 % больных получают адекватное рациональное антибактериальное лечение. Как образно отметил член-корреспондент НАМН Украины, профессор А.П. Волосовец: «Антибиотик для стартового лечения должен обладать оптимальным, а не просто широким спектром антимикробной активности».
Была приведена классификация инфекций мочевой системы:
— неосложненные, осложненные;
— острые: цистит, пиелонефрит, без определения топики;
— хронические (свыше 3 месяцев): цистит, пиелонефрит, без определения топики.
Критерии постановки диагноза инфекций мочевой системы (ИМС) у детей следующие. При острых неосложненных циститах — дизурия, частые мочеиспускания, болезненность в надлобковой зоне, отсутствие каких-либо симптомов в предшествующий месяц, лейкоцитурия ≥ 10/мм3, колониеобразующих единиц ≥ 103/мл. При острых неосложненных пиелонефритах — лихорадка, озноб, боль в пояснице при исключении других диагнозов и пороков развития, лейкоцитурия ≥ 10/мм3, колониеобразующих единиц ≥ 104–5/мл.
Осложненные ИМС: любые комбинации вышеприведенных симптомов при наличии факторов риска, лейкоцитурия ≥ 10/мм3, колониеобразующих единиц ≥ 104–5/мл (Иванов Д.Д., Кушниренко С.В. Рациональные подходы к антимикробной терапии инфекции мочевой системы у детей. — Киев, 2010).
При заболеваниях мочевой системы у детей основным этиологическим фактором развития является Е.сoli. По различным данным, кишечная палочка является возбудителем более чем в 50 % случаев.
В докладе была представлена структура возбудителей инфекций мочевой системы у детей в Запорожской области (рис. 1).
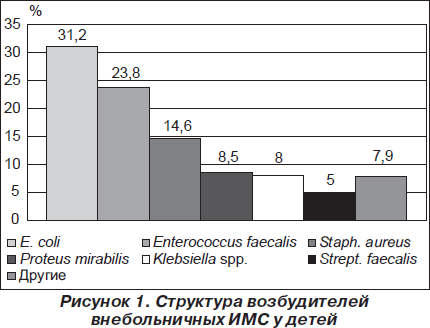
Из патогенов доминирует E.coli, далее идут другие грамотрицательные микроорганизмы.
Стартовыми антибиотиками в лечении ИМС на сегодня являются цефалоспорины III поколения.
Нерациональным является назначение следующих антибактериальных препаратов:
— ампициллина, ампиокса, так как наблюдается высокий уровень устойчивости уропатогенных штаммов E.сoli;
— цефалоспоринов I поколения в связи со слабой активностью против грамотрицательных бактерий, высокой резистентностью E.сoli;
— нитроксолина, так как не доказана его клиническая эффективность и наблюдается высокий уровень устойчивости возбудителей;
— хлорамфеникола из-за высокой токсичности;
— ко-тримоксазола в связи с ростом резистентности E.сoli.
Аминогликозиды целесообразно назначать в условиях стационара.
Для детей в качестве эмпирической антимикробной терапии ИМС рекомендованы пероральные формы защищенных аминопенициллинов и цефалоспоринов (цефиксим) (уровень доказательности Ib).
Цефалоспорины I и II поколения больше действуют на грамположительную флору, цефалоспорины III поколения — на грамотрицательную, на основании чего должен быть сделан выбор рациональной формы цефалоспорина.
Цефикс относится к цефалоспоринам III поколения. Данный препарат проявляет выраженную активность в отношении штаммов Enterobacteriaceae, продуцирующих плазмидные бета-лактамазы широкого и расширенного спектра (ESBL). Продукция бета-лактамаз наиболее характерна именно для возбудителей ИМС — штаммов кишечной палочки, клебсиеллы и протея.
Концентрация цефиксима в моче не уступает таковой в плазме крови. Препарат выделяется с мочой в концентрациях, превышающих МПК90 для значимых уропатогенов, что обеспечивает стабильность эрадикационного эффекта.
Была доказана высокая эффективность цефиксима при грамотрицательных и грамположительных аэробных инфекциях. При неосложненных инфекциях мочевой системы он является высокоэффективным как у детей, так и у взрослых, в том числе и в виде монотерапии (Fanos V., Cataldi L. Cefixime in Urinary Tract Infections with Special Reference to Pediatrics: Overview // Journal of Chemotherapy. — 2001. — V. 12, 2. — 112-117).
В докладе были приведены результаты нескольких исследований, свидетельствующих об эффективности цефиксима при ИМС.
Анализ 2812 детей в возрасте от 1 года до 18 лет показал, что цефиксим не только имеет высокий клинический и бактериологический рейтинг, но и предупреждает рецидивы заболевания. При тяжелых процессах цефиксим можно включать в схемы ступенчатой терапии после 3–4-дневного внутривенного введения других антибиотиков. Эффективность цефиксима при пиелонефритах у детей составляет не менее 92 % (Gok F., Duzova A., Baskin E. et al., 2001).
Еще в одном исследовании изучалась эффективность цефиксима (Цефикс) при инфекциях мочевыводящей системы у детей. В исследование было включено 60 детей в возрасте от 6 месяцев до 16 лет:
— 20 пациентов с острым необструктивным пиелонефритом, в активной стадии, без нарушения функции почек;
— 20 пациентов с хроническим необструктивным пиелонефритом, в активной стадии, без нарушения функции почек;
— 20 пациентов с хроническим циститом в стадии обострения.
По результатам этого исследования представители грамотрицательной флоры проявили высокую чувствительность in vitro к Цефиксу: E.coli — 100 %, Enterobacter spp. — 98 %, Kl.pneumoniae — 93 %. При этом 84 % штаммов Pr.mirabilis, 85 % St.aureus также были чувствительны к цефиксиму.
На фоне лечения Цефиксом у всех пациентов отмечалась положительная динамика. У 91,7 % пациентов эффективность лечения оценивалась как высокая, сопровождающаяся быстрой регрессией симптомов интоксикации и полной нормализацией показателей общего анализа крови и анализов мочи к 10-му дню лечения у пациентов с острым и хроническим пиелонефритом и ликвидацией мочевого синдрома у пациентов с хроническим циститом.
При этом наибольшая эффективность зарегистрирована у пациентов с острым пиелонефритом — 95 %, у пациентов с хроническим пиелонефритом и хроническим циститом — 90 %. (Иванов Д.Д., Кушниренко С.В., НМАПО им. П.Л. Шупика, 2007).
Инфекции урогенитального тракта относятся к заболеваниям, при которых на основании проведеных рандомизированных клинических исследований рекомендована ступенчатая терапия (FDA).
В стартовой терапии тяжелых ИМС следует использовать парентеральные цефалоспорины III поколения с последующим переходом на пероральный препарат III поколения. Проведено исследование эффективности применения Цефикса в ступенчатой терапии пиелонефрита у детей (Иванов Д.Д., Кушниренко С.В., НМАПО им. П.Л. Шупика, 2007). В исследование было включено 40 детей в возрасте от 6 месяцев до 18 лет: 20 пациентов с острым пиелонефритом, 20 пациентов с хроническим неосложненным пиелонефритом в стадии обострения без нарушения функции почек.
Пациенты І группы (n = 20) в первые 3–4 дня пребывания в стационаре получали в/в цефалоспорины ІІІ поколения (цефотаксим, цефоперазон, цефтриаксон, цефтазидим 75 мг/кг в сутки) с последующим переходом на пероральный прием Цефикса на протяжении 7 дней. Ступенчатая терапия назначалась при условии достижения позитивной динамики — нормализации температуры тела в течение 24–48 часов, тенденции к нормализации показателей общего анализа крови, улучшению/стабилизации клинической картины, возможности перорального приема пищи и жидкости, отсутствия нарушения всасывания в ЖКТ, низкой вероятности лекарственных взаимодействий.
Пациенты ІІ группы (контроль, n = 20) на протяжении 10 дней получали антибактериальный препарат внутримышечно (цефтриаксон, цефотаксим, цефоперазон, цефтазидим 75 мг/кг в сутки). Таким образом, длительность антибактериальной терапии в обеих группах составила 10 дней.
По результатам исследования были сделаны следующие выводы:
— уменьшение количества инъекций делает лечение более комфортным, устраняя психологический дискомфорт ребенка и уменьшая риск возникновения постинъекционных осложнений;
— как возможный вариант ступенчатой терапии может быть использовано в/м введения цефалоспорина III поколения в течение 3–4 дней, а затем переход на 7-дневный прием Цефикса.
В ходе проведенного исследования продемонстрирована высокая эффективность, безопасность и хорошая переносимость препарата Цефикс в ступенчатой терапии острого и хронического пиелонефрита у детей.
В соответствии с Национальной резолюцией участников круглого стола по рациональной антимикробной терапии распространенных заболеваний детского возраста от 24 марта 2010 г. (г. Киев):
— в амбулаторных условиях используют пероральное назначение цефиксима в течение 10 дней;
— в более тяжелых случаях рекомендована в стационаре ступенчатая антибактериальная терапия, например в течение 3–4 суток — цефтазидим, цефотаксим, цефоперазон или цефтриаксон парентерально, после улучшения клинического состояния пациента переводят на пероральный прием цефиксима или же используют цефуроксим парентерально с переходом на цефуроксима аксетил;
— после выписки детям младшего возраста, в анамнезе у которых уже имел место эпизод пиелонефрита, при наличии риска развития рубцов в паренхиме почек, при мочекаменной болезни, при наличии дизурических расстройств, а также девочкам с предварительным эпизодом инфекции мочевой системы назначают профилактику низкими дозами уроантисептиков сроком на 3–12 дней.
Препарат рекомендован протоколом лечения инфекций мочевой системы у детей (приказ МЗ Украины № 627 от 03.11.2008), и полученные данные позволяют использовать Цефикс в ступенчатой терапии цефалоспоринами III поколения на основе данных доказательной медицины.
Подготовила Татьяна Брандис

