Журнал «Здоровье ребенка» 2 (29) 2011
Вернуться к номеру
Результаты многоцентрового исследования ЦЕФ-ПРОСТО (ЦЕФподоксима ПРОксетил в Стартовой Терапии внебольничной пневмОнии у детей) в Украине
Авторы: Волосовец А.П.1, Абатуров А.Е.2, Беш Л.В.3, Боярская Л.Н.4, Каладзе Н.Н.5, Кривопустов С.П.1, Крючко Т.А.6, Сенаторова А.С.7, Юлиш Е.И.8 1Национальный медицинский университет имени А.А. Богомольца, г. Киев 2Днепропетровская государственная медицинская академия 3Львовский национальный медицинский университет имени Д. Галицкого 4Запорожский государственный медицинский университет 5Крымский государственный медицинский университет имени С.И. Георгиевского, г. Симферополь 6Украинская медицинская стоматологическая академия, г. Полтава 7Харьковский национальный медицинский университет 8Донецкий национальный медицинский университет имени М. Горького
Рубрики: Педиатрия/Неонатология
Версия для печати
Медико-социальная проблема острых респираторных заболеваний, в частности пневмонии, в педиатрической практике до настоящего времени остается актуальной. Именно пневмония является одной из основных причин смертности детей в возрасте до пяти лет: каждые 20 секунд от пневмонии в мире умирает ребенок.
В свое время всемирно известное открытие антибиотиков Э. Чейном, Г. Флори и А. Флемингом произвело революцию в терапевтических возможностях лечения инфекционных заболеваний, в том числе и пневмоний. Однако врач до настоящего времени вынужден стартовую антибиотикотерапию пневмонии выбирать эмпирически, базируясь лишь на знаниях этиологии заболевания в зависимости от возраста ребенка. При этом клиницистам недостает данных о распространенности ответственных патогенов в конкретном регионе и сведений о резистентности бактерий к применяемым лекарствам. Устойчивость к противомикробным препаратам — тема Всемирного дня здоровья в 2011 году, ведь ее глобальное распространение ставит под угрозу сохранение эффективности многих антибиотиков.
В стартовой терапии внебольничной пневмонии у детей в настоящее время доминируют бета-лактамные антибиотики — пенициллины и цефалоспорины. В частности, в детской практике особого внимания заслуживают цефалоспорины, что объясняется многими их положительными свойствами, среди которых: широкий спектр антимикробного действия; бактерицидный механизм действия; небольшая частота резистентности микроорганизмов; устойчивость к действию многих бета-лактамаз; хорошая переносимость, небольшая частота побочных эффектов; простота и удобство дозирования, что особенно характерно для у препаратов последних поколений.
В стартовой терапии нетяжелой пневмонии, а также в схемах ступенчатой антибиотикотерапии в последние годы широко применяются пероральные цефалоспорины ІІІ поколения, в частности цефподоксима проксетил (Цефодокс). Цефодоксу присуща хорошая биодоступность: максимальная концентрация в сыворотке крови достигается через 2–3 часа, он обладает хорошей способностью создавать эффективные концентрации в крови и очагах воспаления. Отличаясь длительным периодом полувыведения, он принимается 2 раза в сутки через 12 часов, что повышает комплайенс терапии. На украинском фармацевтическом рынке представлены различные педиатрические лекарственные формы данного перорального антибиотика: таблетки, покрытые пленочной оболочкой, содержащие цефподоксима проксетила 100 мг (200 мг), в одной упаковке 10 таблеток; суспензия 50 мл со вкусом лимона, в 5 мл 50 мг (100мг) цефподоксима проксетила.
Проспективное многоцентровое открытое исследование эффективности и переносимости цефалоспоринового антибиотика ІII поколения для перорального применения цефподоксима проксетила (Цефодокс) у детей с нетяжелой внегоспитальной пневмонией (ЦЕФ-ПРОСТО) было проведено в 2009–2010 годах в Украине на базе 8 клинических центров (Киев, Харьков, Донецк, Днепропетровск, Полтава, Запорожье, Львов, Симферополь) — клинических баз педиатрических кафедр высших учебных медицинских учреждений Украины. Главный исследователь и координатор в Украине — член-корреспондент НАМН Украины, доктор медицинских наук, профессор А.П. Волосовец.
Критерии включения пациента в исследование
1. Возраст ребенка 5 мес. — 18 лет на момент визита 1.
2. Включались пациенты обоих полов с наличием установленного диагноза внебольничной пневмонии на основании нижеперечисленных критериев:
а) признаки инфильтрации на рентгенограмме легких (прямая проекция);
б) плюс наличие не менее 2 из нижеперечисленных признаков:
— остро начавшаяся лихорадка;
— кашель;
— частота дыхания (ЧД) для детей 5–12 мес. — 50–60 в 1 мин, 1–5 лет — 40–50 в 1 мин, 5–14 лет — 30–40 в 1 мин, 14–18 лет — 20–30 дыханий в 1 минуту;
— перкуторные изменения — укорочение перкуторного тона и/или аускультативные изменения — локальные мелкопузырчатые хрипы, крепитация, локально выслушиваемое бронхиальное или ослабленное дыхание;
— лейкоцитоз > 15 Ч 109/л и/или сдвиг лейкоцитарной формулы влево;
— способность ребенка пить, есть, принимать лекарство;
— согласие родителей (законных представителей).
Критерии невключения пациента в исследование:
1. Возраст до 5 мес. и после 18 лет на момент первого визита.
2. Ребенок не может пить, есть, принимать лекарство внутрь.
3. Частота дыхания для детей 5–12 мес. — 60 в 1 мин и более, 1–5 лет — 50 в 1 мин и более, 5–14 лет — 40 в 1 мин и более, 14–18 лет — 30 дыханий в 1 минуту и более.
4. Втяжение нижней части грудной клетки.
5. Стонущее дыхание.
6. Наличие внутригоспитальной пневмонии.
7. Рентгенологические признаки сегментарной, лобарной пневмонии.
8. Острая сердечно-сосудистая недостаточность.
9. Острая почечная недостаточность.
10. Острая печеночная недостаточность.
11. Острая дыхательная недостаточность, требующая респираторной терапии, сепсис.
12. Некупируемая гипертермия.
13. Нарушение сознания.
14. Судороги.
15. Наличие легочных осложнений пневмонии — плеврита и др.
16. Известный иммунодефицит.
17. Врожденные или хронические заболевания бронхолегочной системы.
18. Бронхиальная астма.
19. Сахарный диабет.
20. Туберкулез.
21. Онкологические заболевания.
22. Заболевания системы крови, кроме анемии легкой степени.
23 Лечение глюкокортикоидами или цитостатиками.
24. Гастроэнтерологические заболевания с нарушением всасывания.
25. Наличие любых заболеваний, которые, по мнению врача, могли бы затруднить клинико-лабораторно-рентгенологическую оценку.
26. Пребывание в домах ребенка, интернатах.
27. Антимикробная терапия в предшествующие 3 мес.
28. Необходимость комбинированной антимикробной терапии.
29. Необходимость парентерального пути введения антибиотиков.
30. Беременность.
31. Участие в других любых клинических испытаниях.
Критерии исключения пациента из исследования:
1. Отказ от питья, еды, приема лекарства.
2. Частота дыхания для детей 5–12 мес. — 60 в 1 мин и более, 1–5 лет — 50 в 1 мин и более, 5–14 лет — 40 в 1 мин и более, 14–18 лет — 30 дыханий в 1 минуту и более.
3. Развитие втяжения нижней части грудной клетки.
4. Появление стонущего дыхания.
5. Развитие острой сердечно-сосудистой недостаточности.
6. Развитие острой почечной недостаточности.
7. Развитие острой печеночной недостаточности.
8. Развитие острой дыхательной недостаточности, требующей респираторной терапии.
9. Развитие сепсиса.
10. Появление нарушения сознания, появление судорог.
11. Развитие легочных осложнений пневмонии — плеврита и др.
12. Появление любых осложнений, указанных в инструкции к медицинскому применению препарата Цефодокс.
13. Необходимость смены антибиотика.
14. Необходимость перехода на парентеральный путь введения антибиотика.
15. Необходимость в комбинированной антимикробной терапии.
16. Беременность.
17. Отказ родителей (законных представителей).
Цель исследования ЦЕФ-ПРОСТО: оценка эффективности и переносимости цефалоспоринового антибиотика ІII поколения для перорального применения цефподоксима проксетила (Цефодокс) у детей с нетяжелой внегоспитальной пневмонией.
Материалы и методы исследования
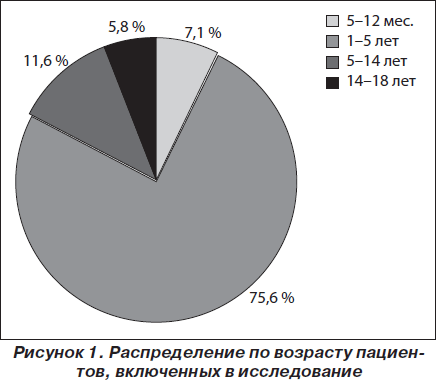
Всего в данное исследование в 8 центрах Украины было включено 225 пациентов в возрасте от 5 месяцев до 18 лет, госпитализированных в педиатрические отделения стационаров с диагнозом нетяжелой внебольничной пневмонии. Из них мальчиков — 109 (48,4 %), девочек — 116 (51,6 %). Распределение по возрасту: 5–12 мес. — 16 (7,1 %), 1–5 лет — 170 (75,6 %), 5–14 лет — 26 (11,6 %), 14–18 лет — 13 (5,8 %) детей, т.е. преобладали дети до 5-летнего возраста (рис. 1).
С момента госпитализации в педиатрическое отделение стационара и при соответствии вышеуказанным критериям включения/невключения использовался Цефодокс для приема внутрь в дозе 10 мг/кг/сутки в 2 приема. На этом этапе дополнительные антибактериальные препараты не применялись, кроме случаев исключения пациента из исследования, а продолжительность лечения определялась индивидуально лечащим врачом. После включения пациента в исследование проводились: оценка клинического состояния больного, установление степени выраженности дыхательной недостаточности и интоксикационного синдрома, определение ЧД, ЧСС, общеклинические лабораторные исследования крови и мочи, биохимическое исследование крови, ЭКГ, рентгенологическое исследование легких в прямой проекции. Спустя 2 недели после завершения лечения Цефодоксом, уже на амбулаторном этапе, также имел место визит пациента к врачу.
Методы исследования
Проводили клинический осмотр, лабораторные общеклинические и биохимические исследования, рентгенологическое исследование органов грудной клетки. Исследуемые параметры: динамика температуры тела, динамика выраженности интоксикационного синдрома, динамика выраженности респираторного синдрома, динамика уровней ЧД, ЧСС, динамика количества лейкоцитов, СОЭ, лейкоцитарной формулы, динамика уровней билирубина, трансаминаз, креатинина по показаниям, динамика рентгенологических данных по показаниям.
Пациенты, вошедшие в исследование, могли принимать муколитические, противогрибковые, антигистаминные, витаминные, спазмолитические, жаропонижающие препараты по показаниям, а при необходимости и препараты других групп, разрешенные к использованию при лечении внегоспитальных пневмоний в соответствии с Приказом МЗ Украины от 13.01.2005 № 18, кроме других антибиотиков, а также препараты, которые показаны больному для лечения сопутствующих поражений и не противопоказаны при лечении внегоспитальной пневмонии.
Эффективность лечения оценивалась на основании комплекса клинико-лабораторных, а в ряде случаев и рентгенологических критериев по шкале:
— 3 балла — высокая эффективность;
— 2 балла — умеренная эффективность;
— 1 балл — низкая эффективность;
— 0 баллов — отсутствие эффективности.
Оценивалась переносимость и безопасность терапии. Так, клиническая оценка переносимости Цефодокса осуществлялась при каждом осмотре больного. Лабораторная оценка переносимости препарата (общеклинические и биохимические анализы) проводилась при завершении его приема. Переносимость препарата оценивалась на основании субъективных симптомов и ощущений, сообщаемых пациентом, и объективных данных, полученных исследователем в процессе лечения. Учитывались частота возникновения и характер побочных эффектов.
Переносимость препарата оценивалась исследователем по объективным данным и пациентом по субъективным ощущениям в баллах по следующей шкале:
— 3 балла — очень хорошая (не отмечаются побочные эффекты);
— 2 балла — хорошая (наблюдаются незначительные побочные эффекты, не причиняющие серьезных проблем пациенту и не требующие отмены препарата);
— 1 балл — удовлетворительная (отмечаются побочные эффекты, оказывающие влияние на состояние пациента, но не требующие отмены препарата);
— 0 баллов — неудовлетворительная (имеет место нежелательный побочный эффект, оказывающий значительное отрицательное влияние на состояние больного и требующий отмены препарата).
Статистическая обработка данных проведена с использованием электронных таблиц Eхcel 5.0 и пакета статистических программ Statistica 6.0 for Windows.
Результаты исследования и их обсуждение
Очаговая левосторонняя бронхопневмония была установлена у 74 (32,9 %), очаговая правосторонняя бронхопневмония — у 107 (47,6 %), двусторонняя пневмония — у 40 (17,8 %), правосторонняя нижнедолевая пневмония — у 4 (1,8 %) детей.
Длительность приема Цефодокса в среднем составила 7 дней. Получали данный пероральный антибиотик 5 дней 39 (17,3 %) пациентов, 10 дней — 49 (21,8 %) пациентов.
Общее состояние детей в начале терапии расценено как среднетяжелое у 199 (88,4 %) и легкой степени тяжести у 26 (11,6 %) больных. Следует указать, что тяжелое течение пневмонии исключало включение ребенка в исследование ЦЕФ-ПРОСТО согласно соответствующим критериям включения/невключения/исключения.
Заслуживает внимания динамика клинического состояния детей на фоне антимикробного лечения Цефодоксом. Уже на 2-й день лечения состояние улучшилось у 98 (43,6 %) детей, еще у 27 (12 %) — на 3-й день, а к концу курса лечения оно нормализовалось на фоне лечения Цефодоксом у 221 (98,2 %) ребенка.
4 (1,8 %) ребенка были исключены из исследования в соответствии с критериями исключения. Так, 1 (0,4 %) ребенок — вследствие ухудшения состояния, увеличения ЧД, указанных в критериях исключения, нарастания одышки, 1 (0,4 %) ребенок — вследствие развития осложнения пневмонии в виде плеврита и 2 (0,9 %) ребенка — из-за ухудшения общего состояния, усиления интоксикационного синдрома и наличия рвоты, требующей парентерального пути введения лекарственных средств. Все эти дети были переведены на внутривенный путь введения антибиотиков, в первых двух случаях — с использованием комбинированной антибиотикотерапии. Спустя 2 недели после завершения лечения, уже на амбулаторном этапе, у всех детей, получивших Цефодокс, и у 4 детей, переведенных на другие антимикробные средства, общее состояние не было нарушенным.
Таким образом, у 221 (98,2 %) ребенка лечение пневмонии Цефодоксом оказалось успешным. Так, утренняя температура тела составляла 37,5 ± 0,2 °С до лечения и 36,4 ± 0,3 °С в конце курса, вечерняя — 37,9 ± 0,4 °С и 36,5 ± 0,2 °С соответственно. При этом у подавляющего большинства детей — 125 (55,6 %) — она уже была в норме на протяжении всех суток начиная с 3-го дня лечения без использования антипиретиков.
Бледность кожи на момент начала лечения отмечалась у 188 (83,6 %) пациентов, цианоз носогубного треугольника — у 12 (5,3 %). Цианоза на 3-и сутки не было ни у одного ребенка, а бледность удерживалась у части детей, отмечаясь в легкой степени к концу терапии у 30 (13,3 %) больных. Спустя 2 недели после завершения лечения, на амбулаторном этапе, цианоза не было ни у одного ребенка, а легкая бледность отмечалась у 14 (6,2 %) детей, из анамнеза было известно о наличии анемии у этих детей в качестве преморбидного фона.
Одышка в виде нарушения глубины дыхания имела место у 25 (11,1 %) больных на момент начала лечения и не отмечалась ни у одного из 221 ребенка на 3-й день лечения Цефодоксом. Большое внимание в оценке критериев включения/невключения/исключения и в анализе динамики состояния ребенка уделялось частоте дыхания. Так, средняя ЧД на момент начала терапии составила 34 в 1 мин, в конце — 23 в 1 мин, однако различный возраст детей не позволяет объективно анализировать средние значения. Принципиально, что учащенное дыхание, не превышающее критические значения в соответствии с критериями включения/невключения, при осмотре на 3-и сутки не отмечалось ни у одного из 221 ребенка. Коррелировали с этим и значения ЧСС (средняя ЧСС в начале — 112 в 1 мин, в конце — 92 в 1 мин) с нормализацией ее у всех детей при осмотре на 3-и сутки. Следует отметить, что уже через 48 часов лечения у подавляющего числа пациентов значения ЧД и ЧСС соответствовали возрастной норме — 202 (89,8 %). Спустя 2 недели после завершения лечения, на амбулаторном этапе, ЧД и ЧСС были в норме у всех пациентов.
Кашель в начале как сухой был расценен у 86 (38,2 %) детей, влажный малопродуктивный — у 125 (55,6 %) и влажный продуктивный — у 14 (6,2 %). Частый кашель отмечался у 185 (82,2 %), редкий — у 33 (14,7 %), единичный — у 7 (3,1 %) детей. На 3-й день лечения кашель как продуктивный был расценен у 132 (58,7 %) пациентов, на 5-й день — у 157 (69,8 %) детей. Единичные покашливания, не приносящие дискомфорта ребенку, к концу терапии регистрировались у 32 (14,2 %) пациентов, а у остальных детей кашель не отмечался. Спустя 2 недели после завершения лечения Цефодоксом, уже на амбулаторном этапе, кашля не было ни у одного ребенка. Следует указать, что пациенты, вошедшие в исследование, по показаниям принимали муколитические препараты (гвайфеназин и др.).
При физикальном исследовании в начале лечения укорочение перкуторного тона имело место у 212 (94,2 %) больных, нормализация перкуторных данных произошла на 5-е сутки у 152 (67,6 %), а к концу лечения — у всех детей. Аускультативно вначале отмечалось ослабленное дыхание у 197 детей, локальные мелкопузырчатые хрипы — у 128 (56,9 %), крепитация — у 97 (43,1 %). Нормализация аускультативной картины происходила постепенно, отмечалось уменьшение выраженности хрипов/крепитации с наиболее отчетливой динамикой на 5–7-й день, при этом к концу терапии хрипов/крепитации ни у одного из детей не было. Спустя 2 недели после завершения лечения Цефодоксом, уже на амбулаторном этапе, перкуторный тон был в норме и дыхание было везикулярным в 100 % случаев.
Данные гемограммы: до лечения средние цифры гемоглобина — 122,5 ± 3,7 г/л, лейкоцитов — 12,9 ± 0,6 Ч 109/л, СОЭ — 21,6 ± 1,6 мм/ч; в конце терапии гемоглобин — 136,0 ± 2,8 г/л, лейкоциты — 6,1 ± 0,5 Ч 109/л, СОЭ — 8,9 ± 0,8 мм/ч. При этом сдвиг лейкоцитарной формулы влево отмечался у 205 (91 %) детей с нормализацией в конце курса лечения у всех пациентов. Изменений со стороны общеклинического анализа мочи, биохимических показателей крови у детей в начале терапии (протеинограмма, трансаминазы, билирубин, мочевина, азот мочевины, креатинин, электролиты крови) не было. Повторное их исследование было проведено у 15 (6,7 %) детей и также не выявило патологических сдвигов.
Следует отметить, что в начале терапии рентгенография органов грудной клетки была выполнена всем детям, включенным в исследование. Она объективизировала диагноз пневмонии: очаговая левосторонняя бронхопневмония была установлена у 74 (32,9 %), очаговая правостороння бронхопневмония — у 107 (47,6%), двусторонняя пневмония — у 40 (17,8 %), правосторонняя нижнедолевая пневмония — у 4 (1,8 %) детей. Контрольная рентгенография была проведена лишь по показаниям у 19 (8,4 %) пациентов в конце лечения Цефодоксом и во всех случаях констатировала нормализацию рентгенологической картины. У 2 (0,9 %) детей с ухудшением клинического состояния контрольная рентгенография была проведена на 3-и — 4-е сутки, и эти дети были переведены на другое лечение согласно критериям исключения пациента из исследования (одышка с соответствующими цифрами ЧД, плеврит).
Стандартная ЭКГ в 12 отведениях в начале курса терапии регистрировала соответствующие изменения ЧСС, а также незначительно выраженные нарушения внутрижелудочковой проводимости у 68 (30,2 %) больных и незначительные нарушения ST-T у 47 (20,1 %) детей. Гипертрофии и/или перегрузки отделов сердца не было. ЭКГ повторялась в динамике по показаниям, и к концу курса терапии у лиц, которым она была выполнена, отмечалось улучшение или нормализация ST-T.
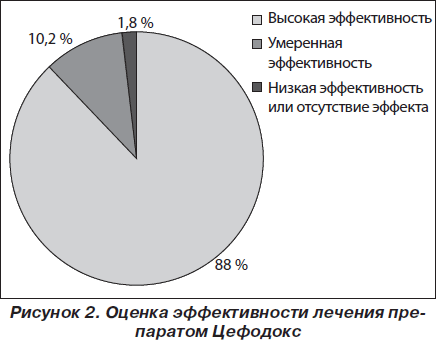
В целом эффективность лечения Цефодоксом была оценена в 3 балла (высокая эффективность) у 198 (88 %) детей, в 2 балла (умеренная эффективность) — у 23 (10,2 %) детей, а у 4 (1,8 %) детей потребовалась замена препарата (рис. 2).
Анализируя профиль безопасности Цефодокса, следует отметить, что он хорошо переносился подавляющим большинством больных детей как в виде суспензии, так и в виде таблеток. Тошнота без рвоты зарегистрирована у 1 (0,4 %) ребенка, рвота — у 7 (3,1 %) детей, диарея — у 2 (0,9 %) детей. Рвота у 5 (2,2 %) детей была однократной, а диарея (неоформленный или жидкий стул чаще, чем обычно) была непродолжительной и не сопровождалась дегидратацией. В целом гастроинтестинальные проявления зарегистрированы у 10 пациентов из 221 (4,5 %). Аллергических реакций не было выявлено ни в одном случае. Спустя 2 недели после завершения лечения Цефодоксом, уже на амбулаторном этапе, стул был в норме у всех детей, что подтверждает высокий профиль гастроинтестинальной безопасности Цефодокса как пролекарства.
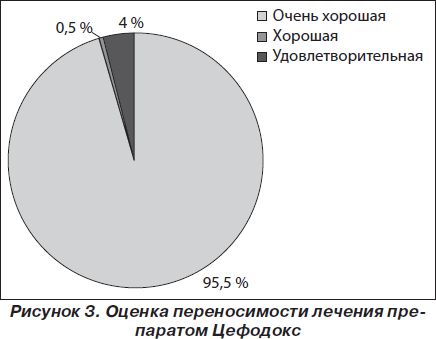
Переносимость Цефодокса оценена в 3 балла (очень хорошая) у 211 из 221 ребенка (95,5 %), в 2 балла (хорошая) — у 1 (0,5 %) пациента, в 1 балл (удовлетворительная) — у 9 (4,0 %) детей (рис. 3).
Таким образом, проспективное многоцентровое открытое исследование эффективности и переносимости цефалоспоринового антибиотика ІII поколения для перорального применения цефподоксима проксетила (Цефодокс) у детей с нетяжелой внегоспитальной пневмонией (ЦЕФ-ПРОСТО), проведенное в 2009–2010 годах в Украине на базе 8 клинических центров (Киев, Харьков, Донецк, Днепропетровск, Полтава, Запорожье, Львов, Симферополь) с участием 225 пациентов в возрасте от 5 месяцев до 18 лет, показало:
— высокую (88 %) и умеренную (10,2 %) эффективность цефподоксима проксетила (Цефодокса) в лечении детей, госпитализированных в педиатрические отделения стационаров с диагнозом нетяжелой внебольничной пневмонии;
— высокий профиль безопасности цефподоксима проксетила (Цефодокса): очень хорошая переносимость отмечена у 95,5 % пациентов, гастроинтестинальные проявления, не требующие отмены препарата, зарегистрированы у 4,5 % детей.
1. Абатуров А.Е., Герасименко О.Н. Применение цефподоксима проксетила при лечении внебольничных пневмоний у часто болеющих детей раннего возраста // Современная педиатрия. — 2008. — № 2(19).
2. Боярская Л.Н., Котлова Ю.В., Герасимчук Т.Г., Тав–рог М.Л., Подлианова Е.И., Берлимова Н.В. Побочные действия цефалоспоринов третьего поколения при лечении детей младшего возраста с респираторными заболеваниями // Современная педиатрия. — 2008. — № 5(22).
3. Волосовец А.П., Кривопустов С.П. Цефалоспорины в практике современной педиатрии. — Харьков: Прапор, 2007.
4. Волосовец А.П., Кривопустов С.П., Дзюба О.Л., Мягкая Н.Н., Мороз Т.С. Опыт применения перорального цефалоспорина Цефодокс у детей с пневмонией // Здоровье ребенка. — 2007. — № 5(8).
5. Волосовец А.П., Кривопустов С.П., Дзюба О.Л., Мягкая Н.Н., Мороз Т.С. Возможности применения препарата «Цефодокс» в схеме ступенчатой терапии пневмонии у детей // Современная педиатрия. — 2007. — № 4(17).
6. Волосовец А.П., Кривопустов С.П., Юлиш Е.И. Современные взгляды на проблему антибиотикорезистентности и ее преодоление в клинической педиатрии // Новости медицины и фармации. — 2008. — № 236.
7. Волосовец А.П., Кривопустов С.П. Пероральный цефалоспориновый антибиотик ІІІ поколения Цефодокс (цефподоксима проксетил) в практике современной педиатрии: Методические рекомендации. — К., 2007.
8. Волосовець О.П. Диференційоване застосування пероральних цефалоспоринів у практиці сучасної педіатрії // Педіатрія, акушерство та гінекологія. Мат-ли V Конгресу педіатрів України «Сучасні проблеми клінічної педіатрії» 14–16 жовтня 2008 року, м. Київ. — 2008. — № 4.
9. Кривопустов С.П. Антимикробная терапия инфекций респираторного тракта у детей: проблемы, с которыми мы сталкиваемся в повседневной практике (мастер-класс для врачей) // Здоров’я України. — 2009. — № 4(1).
10. Кривопустов С.П. Вопросы эмпирической антибиотикотерапии в педиатрии с позиций доказательной медицины // Мистецтво лікування. — 2007. — № 9–10.
11. Кривопустов С.П. Оптимізація лікування пневмоній у дітей в умовах стаціонару // Педіатрія, акушерство та гінекологія. Матеріали V Конгресу педіатрів України «Сучасні проблеми клінічної педіатрії» 14–16 жовтня 2008 року, м. Київ. — 2008. — № 4.
12. Крючко Т.А., Бастаногова О.В., Ткаченко О.Я., Шпехт Т.В. Опыт применения Цефодокса в терапии внегоспитальных пневмоний // Современная педиатрия. — 2008. — № 3(20).
13. Юлиш Е.И., Волосовец А.П. Антибиотики в поликлиническом и начальном стационарном этапе лечения бактериальных поражений дыхательной системы у детей. — Донецк: Регина, 2002.
14. Ann Van den Bruel et al. Diagnostic value of clinical features at presentation to identify serious infection in children in developed countries: a systematic review // Lancet. — 2010. — 375.
15. Cevey-Macherel M., Galetto-Lacour A., Gervaix A. et al. Etiology of community-acquired pneumonia in hospitalized children based on WHO clinical guidelines // Eur. J. Pediatr. — Feb 24, 2009.
16. Guideline. Cincinnati Children’s Hospital Medical Center. Evidence based care guideline for community acquired pneumonia in children 60 days through 17 years of age. — Cincinnati (OH): Cincinnati Children’s Hospital Medical Center. Jul 2006.
17. Integrated management of childhood illness. IMCI chart booklet — standard. World Health Organization; UNICEF. — 2008.
18. Juven T., Mertsola J., Waris M. et al. Etiology of community-acquired pneumonia in 254 hospitalized children // Pediatr. Infect. Dis. J. — Apr 2000. — 19(4).
19. Michelow I.C., Olsen K., Lozano J. et al. Epidemiology and clinical characteristics of community-acquired pneumonia in hospitalized children // Pediatrics. — Apr 2004. — 113(4).
20. Rudan I., Tomaskovic L., Boschi-Pinto C., Campbell H. Global estimate of the incidence of clinical pneumonia among children under five years of age // Bull. World Health Organ. — Dec 2004. — 82(12).
21. Shah S., Bachur R., Kim D., Neuman M.I. Lack of Predictive Value of Tachypnea in the Diagnosis of Pneumonia in Children // Pediatr. Infect. Dis. J. — Dec, 21 2009.
22. The Sanford Guide to Antimicrobial Therapy / David N. Gilbert, Robert C. Moellering, George M. Eliopoulos, Henry F. Chambers, Michael S. Saag. — 40th edition. — Saag, 2010.
