Журнал «Травма» Том 11, №1, 2010
Вернуться к номеру
Експериментальні аспекти застосування нових композитних матеріалів для пластики дефектів кісток
Авторы: І. Г. Герцен - ДУ «Інститут травматології та ортопедії АМН України», Київ, Україна
Рубрики: Травматология и ортопедия
Разделы: Клинические исследования
Версия для печати
В статті проаналізовані сучасні матеріали для пластики порожнинних дефектів кісток. Експериментально доведені перспективні напрямки по заміщенню дефектів кісток фосфорно-кальцієвим композитом.
В статье проанализированы современные материалы для пластики полостных дефектов костей. Экспериментально доказаны перспективные направления по замещению костных дефектов фосфорно-кальциевым композитом.
In article were analyzed modern materials for bone defects substitution. Perspective directions on replacement of bone defects with phosphorus-calcic are experimentally proved to composite.
дефекти кісток, методи остеопластики, кальцій-фосатний композит
дефекты костей, методы остеопластики, кальций-фосфатный композит
bone defetcs, methods of osteoplasty, calcium-phosphates compositum
Відомо, що перша зареєстрована імплантація кісткової тканини була виконана в 1668 році [6]. Проте, незважаючи на багатовікову історію, проблема заміщення дефектів кісток не тільки не втратила актуальність, а й з науковими досягненнями набула нових напрямків. Це сприяло появі матеріалів з високими пластичними можливостями.
Необхідність застосування кісткових трансплантатів в ортопедії та травматології виникає при лікуванні різних ушкоджень і захворювань. Передусім це: посттравматичні дефекти кісток, уповільнене зрощення, псевдоартрози, пухлини і пухлиноподібні захворювання; кісткові дефекти внаслідок остеомієліту та дегенеративно-дистрофічних захворювань [3].
Пошуки оптимальних матеріалів для кісткової пластики тісно пов’язані з намаганнями розкрити механізми фізіологічної та репаративної регенерації, а також можливістю керувати фізико-хімічними властивостями імплантатів. Тому в дослідженнях з цієї проблеми тісно переплітаються не тільки хірургічні аспекти трансплантації, а й гістоморфологічні, лабораторні та експериментальні методи [1].
Аутокістка – матеріал, що найбільш часто використовується для остеопластики. Аутотрансплантати здатні забезпечити структурну підтримку, мають остеоіндуктивні та остеокондуктивні властивості, ремоделюються в результаті нормальних фізіологічних механізмів, перетворюючись на здорову кістку. На сьогоднішній день жоден з відомих матеріалів за своїми остеоіндуктивними (остеогенними) властивостями не відповідає аутокістці. Проте аутопластика кісткових дефектів має недоліки, пов’язані з унеможливленням заміщення великіх дефектів, додатковою хірургічною травмою: збільшення часу операції, складність взяття у дітей, відсутність повноцінної аутокістки при системному остеопорозі та ін.
Алогенна кістка, в тому числі її сучасний варіант – тутопласт, частково зберігає структурну міцність, остеоіндуктивні та остеокондуктивні властивості аутотрансплантата. Однак методика використання алотрансплантатів має ряд значних недоліків: потрібен відбір донорів, для одержання і збереження потрібне технічне та законодавче забезпечення, можливість запалення, відторгнення трансплантата, мала швидкість біодеградації матеріалу [3].
Перспективними імплантатами для кісткової хірургії на сьогодні є кальцій-фосфатні біоматеріали. Серед них в наш час широко застосовуються синтетичний та біологічний керамічні апатити [2]. Керамічний гідроксіапатит – штучно синтезовані кристали неорганічного матриксу кістки. Остеопатит керамічний – комбінований матеріал, що отримують шляхом поєднання склофази з біологічним апатитом тваринного походження. Дані матеріали наділені остеокондуктивними та біодеградаційнними властивостями і є абсолютно біосумісними.
Недоліками цих імплантатів є спірні остеоіндуктивні властивості, а також зменшення компресійної стійкості зі збільшенням пористості імплантата.
Вищезазначене обумовило широке розповсюдженню в кістково-пластичній хірургії композитних матеріалів. Це пов’язано з тим, що жоден з синтетичних компонентів, що використовуються при виготовленні імплантатів, не наділений усіма властивостями кісткової тканини. Цільні ж фрагменти біологічних матеріалів мають обмежений набір пластичних властивостей. Тому композити дають можливість отримати кістково-пластичний матеріал, який за хімічними та механічними властивостями наближається до «золотого стандарту» - аутоостеопластики.
Групою зарубіжних вчених [4] синтезований кальцій-фосфатний композит (КФК).
КФК – синтетичний замісник кісткової тканини, який повторює кристалічну структуру мінерального матриксу кістки та має здатність до біодеградації. Композит імплантується у вигляді пасти, яка під впливом температури тіла твердіє, набуваючи густини компактної кісткової тканини. Ця речовина має здатність до біорезорбції з утворенням нової кісткової тканини [5].
Мета роботи - в експерименті визначити можливості заміщення дефектів кісток фосфорно-кальцієвим композитом та провести порівняльну характеристику імплантаційних властивостей кальцій-фосфатного композиту з синтетичним та біологічним апатитами.
Матеріал та методи
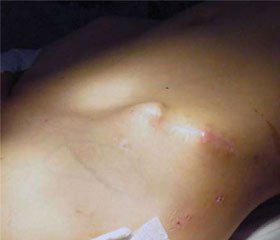
Експериментальне дослідження виконане на 72 дорослих кроликах породи шиншила масою 2,7-2,9 кг. Оперативне втручання виконували в стерильних умовах (операційна віваріуму) під комбінованою анестезією. Внутрішньом’язово вводили 2 мл 3% розчину кетаміну, місцево – 5 мл 0,5% розчину новокаїну. Дефект кістки нами змодельований шляхом перфорації проксимального епіметафіза великогомілкової кістки хірургічним кортикальним свердлом діаметром 3 мм. Отвір мав довжину близько 6 мм і проходив через обидва кортикальні шари кістки. Порожнину, що штучно утворили, у тварин першої групи заповнювали фосфорно-кальцієвим композитом (21 кролик). У тварин другої групи - 21 кролик - біологічним гідроксіапатитом (пористий ОСТАП); у тварин третьої групи - 21 кролик - синтетичним гідроксіапатитом (пористий КЕРГАП).
Дев’яти прооперованим тваринам остеопластику не виконували - група контролю. Післяопераційну рану пошарово зашивали шовковими нитками. Іммобілізацію прооперованої кінцівки не проводили. Строки спостереження за кроликами становили: 7, 14, 28, 60, 90, 180 та 360 діб після оперативного втручання. Досліджували по 3 кролика на кожний строк спостереження (таблиця).
Експерименти на тваринах проводили відповідно до правил «Європейської конвенції захисту хребетних тварин, що використовуються в експериментальних та інших наукових цілях». У динаміці спостерігали загальні реакції тварин, а також були виконані рентгенологічні та гістоморфологічні методи дослідження.
Результати та обговорення
В експерименті не визначено загальних та місцевих проявів реактивності на фосфорно-кальцієвий композит, а також на ОСТАП та КЕРГАП. Аналіз даних рентгенологічного дослідження показує відносно швидшу остеоінтеграцію в зоні імплантованого кальцій-фосфатного композиту (межа «імплантат-кістка» у першій групі не відмічалась вже на 14 добу після операції).
Морфологічні дослідження показали, що навколо імплантованого в дефект матеріалу КФК виникало активне ендостальне та періостальне кісткоутворення, яке супроводжувалось формуванням молодих кісткових перекладок. Останні щільно прилягали до імплантата.
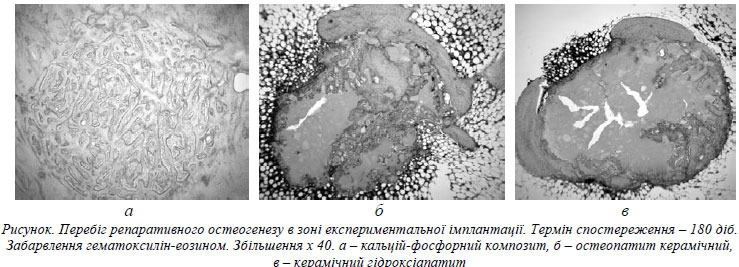
З 60-ї доби спостерігали крайову резорбцію імплантата. Резорбційні порожнини заповнювались новоутвореною кістковою тканиною або ретикулярним кістковим мозком. З часом, через 180 та особливо через 360 діб (рис. а) – регенерат набував будови компактної кісткової тканини. Ендостальний регенерат практично повністю перебудовувався з формуванням у кістковій порожнині жовтого кісткового мозку.
Аналіз морфологічних даних в інших досліджуваних групах показав відносно сповільнену біодеградацію. Навіть через 360 діб після імплантації визначали наявність гранул ОСТАПу та КЕРГАПу в кістці (рис. б,в). Реакція кісткової тканини на травму була аналогічною тій, що ми спостерігали при пластиці КФК.
Висновки
Встановлено, що імплантований в губчасту кісткову тканину кальцій-фосфатний композит також, як і синтетичний (КЕРГАП) та біологічний (ОСТАП) апатити, не викликає після імплантації патологічної реакції в оточуючій кістковій тканині і кістковому мозку, не порушує кісткоутворюючу функцію ендоста, поступово піддає біодеградації та заміщенню новою кістковою тканиною.
Порівняльний аналіз даних рентгенологічного та гістологічного досліджень свідчить, що кальцій-фосфатний композит піддається більш активній перебудові (на 180-й день після імплантації він не виявляється або визначаються тільки його залишки). Біодеградація ОСТАПу та КЕРГАПу відбувається дещо повільніше, ніж кальцій-фосфатного композиту.
- Лузин В.И., Ивченко В.К., Ивченко Д.В., Скоробогатов А.Н., Панкратьев А.А. // Травма, Т. 6, №3, 2005, - С. 272-277.
- Слуцкий Л.И. // Биологические вопросы биоматериаловедения, 2002, С. 95-109.
- Філипенко В.А., Зиман З.З., Мезенцев В.А. // Збірник наукових праць 12 з¢ізду ортопедів-траваматологів України, Донецьк, 2001. - С. 144-147.
- Driessens FCM, Boltong M.G., Wenz R./ 12th Conference of the European Society of Biomechanics, Dublin, Ireland, 27-30th August 2000.
- Ooms EM, Wolke JGC, van der Waerden JPSM, Jansen JA. // Trabecular bone Response to injectable Ca-P Cement, 2002, 61: 9-18.
- Operative orthopaedics. / Edited M.W. Chapman. – 2 edition – J.B. Lippincott Company, Philadelphia, 1993. – Vol. 1. – P.1-1030.