Международный эндокринологический журнал 4 (36) 2011
Вернуться к номеру
Применение метформина пролонгированного высвобождения у больных сахарным диабетом 2-го типа: новые возможности достижения компенсации
Авторы: Панькив В.И., Украинский НПЦ эндокринной хирургии, трансплантации эндокринных органов и тканей МЗ Украины
Рубрики: Эндокринология
Версия для печати
Метформин является одним из старейших препаратов, и многие его свойства достаточно хорошо изучены, однако данный препарат по праву занимает сегодня лидирующую позицию в лечении сахарного диабета (СД) 2-го типа. Клинические исследования продолжаются, и, возможно, будут открыты многие новые полезные его свойства. Недаром метформин называют «бестселлером, который не прочитан до конца»!
В клинической практике используется и новая лекарственная форма метформина продленного действия, которая предназначена для преодоления таких побочных действий, как расстройства функции желудочно-кишечного тракта (ЖКТ), упрощения схемы приема препарата для лиц пожилого возраста, для повышения комплайентности и сохранения эффективности проводимого лечения. Препарат прошел испытания в международных многоцентровых исследованиях и доказал свою эффективность и безопасность.
Вначале напомним об известном. На сегодняшний день метформин — единственный представитель группы бигуанидов, рекомендованный в качестве стартовой терапии при СД 2-го типа всеми ведущими профессиональными сообществами диабетологов. Препарат не вызывает столь опасной для пожилых пациентов гипогликемии, не способствует прибавке массы тела и даже умеренно ее снижает. За счет улучшения чувствительности тканей к инсулину он снижает уровень атерогенных липидов: уменьшает содержание общего холестерина, триглицеридов и липопротеинов низкой плотности.
Бигуаниды используются в медицинской практике более 50 лет. Ведущие медицинские организации рекомендуют сегодня начинать лечение СД 2-го типа с комбинации изменения образа жизни и назначения метформина. В связи с этим представляют особый интерес новые результаты, касающиеся вновь открытых свойств метформина.
Метформин снижает как исходный уровень глюкозы в плазме крови, так и уровень глюкозы в крови после приема пищи. В отличие от производных сульфонилмочевины (ПСМ) не стимулирует секрецию инсулина и не приводит к гипогликемическому эффекту у здоровых лиц. Метформин обладает тройным механизмом действия: вызывает снижение выработки глюкозы в печени за счет ингибирования глюконеогенеза и гликогенолиза; улучшает захват и утилизацию глюкозы крови в мышцах за счет повышения чувствительности к инсулину; задерживает всасывание глюкозы в кишечнике.
Метформин был введен в клиническую практику для лечения СД 2-го типа в 1957 г. в Европе и в 1995 г. в США. В настоящее время метформин является наиболее часто назначаемым пероральным сахароснижающим препаратом в Европе, США и других странах (R.A. DeFronzo, 2007). Механизм антигипергликемического действия метформина достаточно хорошо изучен. В многочисленных исследованиях установлено, что метформин не влияет на секрецию инсулина b-клеткой, а оказывает экстрапанкреатическое действие. Он вызывает: снижение всасывания углеводов в кишечнике; повышение превращения глюкозы в лактат в ЖКТ; усиление связывания инсулина с рецепторами; экспрессию гена транспортера ГЛЮТ-1; усиление транспорта глюкозы через мембрану в мышцах; транслокацию ГЛЮТ-1 и ГЛЮТ-4 из плазменной мембраны к поверхностной мембране в мышцах; снижение глюконеогенеза; снижение гликогенолиза; снижение уровня триглицеридов и липопротеинов низкой плотности; повышение содержания липопротеинов высокой плотности.
Основной механизм действия метформина направлен на преодоление резистентности периферических тканей к действию инсулина, в особенности это касается мышечной и печеночной ткани. Опубликован ряд клинических исследований с разным дизайном, подтвердивших действие метформина на печеночный метаболизм глюкозы.
Клинические эффекты метформина, помимо его антигипергликемических свойств, достаточно хорошо изучены. Впервые они были представлены после завершения многолетнего исследования UKPDS (United Kingdom Prospective Diabetes Study) в 1998 г. Основными выводами были следующие: терапия метформином у тучных лиц снижает риск осложнений: сосудистых осложнений — на 32 %; cмертности от диабета — на 42 %; общей смертности — на 36 %; инфаркта миокарда — на 39 %. Эти данные были настолько убедительны, что метформин был полностью реабилитирован как безопасный и полезный сахароснижающий препарат. В дальнейшем были доказаны многочисленные кардиопротективные свойства метформина. Полагают, что именно наличием этих свойств объясняется дополнительный позитивный и профилактический эффект метформина при СД 2-го типа.
Метформин обладает прямыми ангиопротекторными эффектами, которые не зависят от сахароснижающего эффекта препарата. Эти эффекты уникальны. Двойное действие метформина объясняет результаты по снижению смертности, которые были получены в UKPDS. Полученные в последующие годы данные подтвердили позитивное влияние метформина. Так, лечение метформином в сравнении с любым другим лечением было ассоциировано с более низкой смертностью от всех причин, более низкой частотой инфаркта миокарда, симптомов стенокардии или любых кардиоваскулярных проявлений.
Одним из актуальных направлений в изучении возможностей иного использования метформина являются работы, связанные с возможностью лечения неалкогольной жировой болезни печени (НАЖБП). Неалкогольная жировая болезнь печени — это распространенное хроническое заболевание печени, характеризующееся патологическим накоплением жировых капель, не связанное с употреблением алкоголя. НАЖБП является компонентом метаболического синдрома, СД 2-го типа, ожирения.
Установлено, что ткани-мишени для препаратов, уменьшающих резистентность периферических тканей к инсулину, различны. Метформин в большей степени действует на уровне печени. Поэтому для лечения НАЖБП в первую очередь целесообразно использовать метформин.
Продолжая изучать этот медикаментозный «бестселлер» нашего времени, исследователи обнаруживают его многообещающие возможности в лечении не только СД 2-го типа, но и других серьезных заболеваний. Так, немецкие ученые из научно-исследовательского центра нейродегенеративных заболеваний (DZNE) выяснили, что метформин может быть эффективен при болезни Альцгеймера, которая поражает преимущественно пожилых людей (в той же Германии примерно 700 тысяч человек страдают этой болезнью).
Еще одним важным и весьма перспективным направлением в изучении свойств метформина является его антионкогенный эффект. Опубликован ряд клинических исследований, в которых было показано снижение роста онкологических заболеваний среди пациентов, применяющих метформин. S.L. Bowker и соавт. провели популяционное ретроспективное когортное исследование с использованием базы данных провинции Саскачеван (Канада, 1995–2006 гг.). Целью исследования было изучение смертности от рака и взаимосвязь с антидиабетической терапией при СД 2-го типа. Обследовали 10 309 пациентов с СД 2-го типа с впервые назначенными метформином, производными сульфонилмочевины (сульфониламиды — СА) и инсулином. Средний возраст больных составил 63,4 ± 13,3 года, среди них 55 % были мужчины. Метформин назначен 1229 больным в виде монотерапии, ПСМ — 3340 больным в виде монотерапии, комбинированная терапия — 5740, инсулин добавлен 1443 больным. Длительность наблюдения — 5,4 ± 1,9 года.
Всего смертность от рака составила 4,9 % (162 из 3340) у лиц, получавших СА, 3,5 % (245 из 6969) — метформин и 5,8 % (84 из 1443) — инсулин. Представленные данные демонстрируют двукратное увеличение частоты возникновения онкологических заболеваний в группе пациентов на инсулинотерапии по сравнению с группой метформина — 1,9 (95% ДИ 1,5–2,4, p < 0,0001). В группе пациентов, находящихся на терапии препаратами СА, риск возникновения раковых опухолей был также значительно выше показателей в группе метформина и составлял 1,3 (95% ДИ 1,1–1,6, p = 0,012).
C.J. Currie и соавт. также изучали риск развития злокачественных образований у больных СД 2-го типа в зависимости от вида проводимой терапии. В исследование было включено 62 809 пациентов с СД 2-го типа старше 40 лет, которые были разделены на четыре терапевтические группы: монотерапия метформином или СА, комбинированная терапия метформином и СА и инсулинотерапия. Группа пациентов, получающих инсулин, была разделена на подклассы: монотерапия инсулином гларгин, НПХ-инсулином, двухфазным инсулином и его аналогами. Также оценивались данные о манифестации или прогрессировании за период лечения (инсулинотерапия с 2000 г.) любых злокачественных образований; особое внимание уделялось раку молочной железы, толстого кишечника, поджелудочной и предстательной желез.
При анализе полученных данных было выявлено, что в группе пациентов, получающих метформин, отмечалось значительное снижение риска развития рака толстого кишечника и поджелудочной железы (однако подобной закономерности не наблюдалось в отношении рака предстательной и молочной желез). Редуцирование роста злокачественных клеток на фоне монотерапии метформином составило 0,54 (95% ДИ 0,43–0,66). Даже в случае добавления к любой сахароснижающей терапии метформина риск малигнизации снижался до 0,54 (95% ДИ 0,43–0,66).
Одним из последних опубликованных исследований является ZODIAC-16 (Zwolle Outpatient Diabetes project Integrating Available Care), завершенное в Нидерландах и опубликованное в 2010 г. Целью исследования являлось изучение ассоциации между специфическим лечением СД 2-го типа и смертностью от рака. В данном случае изучали ассоциацию между использованием метформина и смертностью от рака в проспективной когорте. Набор пациентов проводился с 1998 по 1999 г. Было включено 1353 пациента с СД 2-го типа. Исследование завершено в 2009 г. Характеристика пациентов: на метформине — 289; без метформина — 1064; средний возраст 67,8 ± 11,7 года; длительность СД — 6,0 года; ИМТ — 28,9 ± 4,8 кг/м2; HbA1c — 7,5 ± 1,2 %; CКФ — 73,9 ± 28,1 мл/мин; инсулинотерапия — 16,5 %; СА — 55,0 %; только диета — 13,0 %; исключены лица с активными формами рака, когнитивными расстройствами и очень маленькой предполагаемой продолжительностью жизни.
При оценке через 9,6 года умерло всего 570 пациентов (42 %). Из них 122 (21 %) умерли от рака, среди них 26 (21 %) — от рака легких, 21 (17 %) — от рака абдоминальной локализации. 238 больных (41 %) умерли от сердечно-сосудистых заболеваний. Причины смерти 541 (94 %) больного известны. У пациентов, получавших метформин, в сравнении с пациентами, не получавшими метформин, относительный риск (ОР) смертности от рака составил 0,43 (95% ДИ 0,23–0,80). ОР повышался при увеличении дозы метформина — при добавлении каждого грамма метформина ОР был 0,58.
Стоит упомянуть, что назначение метформина при синдроме поликистозных яичников, характеризующемся ИР и выступающем в качестве фактора риска развития рака тела матки, также способствует нивелированию возможной атипической гиперплазии эндометрия. Безусловный интерес представляют исследования российских ученых, в которых бигуаниды, наряду с гиполипидемическими препаратами и диетой, назначались на длительный срок более чем 300 больным раком молочной железы и толстой кишки, подвергавшимся оперативному лечению. В итоге к 3–7 годам наблюдения было обнаружено повышение кумулятивной выживаемости, а также некоторое уменьшение частоты выявления первично-множественных опухолей и метахронных опухолей второй молочной железы.
В настоящее время в отношении взаимосвязи СД и злокачественных новообразований остается еще много нерешенных вопросов. Тем не менее, как свидетельствуют накопленные на сегодняшний день сведения, метформин может оказывать благоприятное воздействие на эффективность проводимой терапии и продолжительность жизни пациентов. Таким образом, клиническая судьба метформина — тот редкий случай, когда с увеличением опыта применения открываются новые плюсы, а не минусы лекарственного средства. Границы его терапевтического потенциала имеют явную тенденцию к расширению.
Эффективность новой формы метформина с пролонгированным высвобождением
После приема внутрь в форме таблетки с пролонгированным высвобождением всасывание метформина значительно замедляется по сравнению с таблеткой с быстрым высвобождением. Время достижения максимальной концентрации в сыворотке крови составляет 7 ч. В то же время для таблетки с быстрым высвобождением это время составляет 2,5 ч.
После однократного приема внутрь 2000 мг метформина в форме таблеток пролонгированного действия площадь под кривой «концентрация/время» (AUC) аналогична наблюдаемой после приема 1000 мг метформина в форме таблеток с обычным высвобождением два раза в сутки. Колебания максимальной концентрации метформина (Cmax) и AUC у отдельных пациентов в случае приема метформина в форме таблеток пролонгированного действия сравнимы с теми же показателями, что и в случае приема таблеток с обычным профилем высвобождения.
Всасывание метформина из таблеток пролонгированного высвобождения не изменяется в зависимости от приема пищи. Не наблюдается кумуляции при многократном приеме до 2000 мг метформина в форме таблеток пролонгированного действия. Метформин выводится из организма в неизменном виде с мочой. Метаболитов у человека не выявлено. Почечный клиренс составляет > 400 мл/мин, это указывает на то, что метформин выводится за счет клубочковой фильтрации и канальцевой секреции. После перорального приема дозы период полувыведения составляет около 6,5 ч. При снижении функции почек почечный клиренс уменьшается пропорционально клиренсу креатинина, и поэтому период полувыведения увеличивается, что приводит к повышению уровня метформина в плазме крови.
Препарат метформина пролонгированного действия назначают во время ужина (1 раз в день) или во время завтрака и ужина (2 раза в день). Доза препарата подбирается путем титрования от минимальной до эффективной лечебной (максимальной) в течение 10–15 дней, в зависимости от целевых значений гликемии. Возможно проведение как монотерапии, так и комбинированной терапии с другими гипогликемизирующими средствами.
Обычная начальная доза 500 мг: 1 таблетка 1 раз в день во время ужина. При переходе с метформина с обычным высвобождением активного компонента на пролонгированный препарат начальная доза препарата метформина пролонгированного действия должна быть равной суточной дозе метформина с обычным высвобождением активного компонента.
Максимальная суточная доза метформина пролонгированного действия составляет 2000 мг 1 раз в день во время ужина. Если контроль содержания глюкозы не достигается при максимальной суточной дозе, принимаемой 1 раз в день, то можно рассмотреть возможность разделения этой дозы на два приема в день по следующей схеме: метформин пролонгированного действия 500 мг — 2 таблетки во время завтрака и 2 таблетки во время ужина. За рубежом препараты метформина пролонгированного действия выпускаются в дозировках по 500, 750 и 1000 мг в 1 таблетке.
Таким образом, применение метформина пролонгированного высвобождения у больных сахарным диабетом 2-го типа позволяет улучшить контроль уровня глюкозы крови на протяжении суток, безопасность лечения, а также создает удобство применения для пациента.
1. Маньковський Б.М. Застосування метформіну в лікуванні пацієнтів з цукровим діабетом 2 типу / Б.М. Маньковський // Нова медицина. — 2006. — № 3. — С. 72-74.
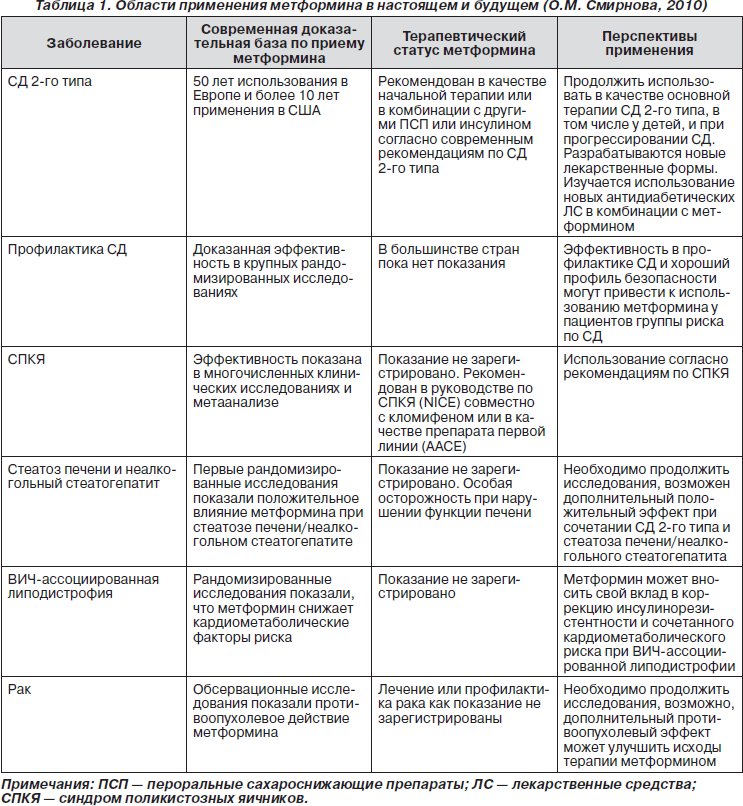
2. Смирнова О.М. Место метформина в современном лечении и профилактике сахарного диабета 2-го типа // Cахарный диабет. — 2010. — № 3. — С. 83-90.
3. Берштейн Л.М. Метформин и онкологическая заболеваемость // Cахарный диабет. — 2010. — № 3. — С. 66-71.
4. Древаль А.В., Мисникова И.В., Триголосова И.В., Тишенина Р.С. Влияние метформина на углеводный и липидный обмен у лиц с ранними нарушениями углеводного обмена // Cахарный диабет. — 2010. — № 2. — С. 63-68.
5. Горбенко Н.И. Метформин — средство выбора для предупреждения и уменьшения выраженности сердечно-сосудистой патологии у больных сахарным диабетом 2-го типа / Н.И. Горбенко, М.Ю. Горшунская // Український медичний часопис. — 2005. — № 4. — С. 29-36.
6. De Fronzo R.A. Metformin. The Gold Standard. A Scientific Handbook / Ed. by Bailey C.J., Campbell J.W., Chan J.C.N. — Wiley, 2007.
7. Bailey C.J., Howlett H.C.S. Defining patient populations not indicated for metformin. Metformin. The Gold Standard. A Scientific Handbook / Ed. by Bailey C.J., Campbell J.W., Chan J.C.N. — Wiley, 2007. — P. 193-198.
8. Eurich D.T., Majumdar S.R., McAlister F.A. et al. Improved clinical outcomes associated with metformin in patients with diabetes and heart failure // Diabetes Care. — 2005. — Vol. 28. — P. 2345-2351.
9. McDonald A., Eurich D.T., Mayumidar S.R. Treatment of type 2 diabetes and outcomes in patients with heart failure: A nested case-control study from UK General Practice Research Datebase // Diabetes Care. — 2010. — Vol. 33. — P. 1210-1219.
10. Landman G.W.G., Kleefstra N., Van Haleren K.J.J. Metformin associated with lower cancer mortality in type 2 diabetes // Diabetes Care. — 2010. — Vol. 33. — P. 322-326.